Метаболитни измервания
След 15 часа без храна глюкозата на гладно се измерва в кръв, събрана чрез едно убождане върху мандибуларните вени (позволяваща само една капка да се отдели) с помощта на глюкомер (Accu-Chek Performa, Roche, Meylan, Франция) [29]. Тестът за толерантност към орална глюкоза (OGTT) е направен на възраст от 13 седмици и е описан по-рано [11]. Плазма от кръвна проба на OGTT се получава след центрофугиране при 2000 g за 5 минути. След това плазмата се замразява и съхранява при - 80 ° C преди по-нататъшен анализ. Концентрацията на инсулин се оценява върху тези плазмени проби, използвайки ELISA методи (Insulin Elisa от плъх, ALPCO, Eurobio, Courtaboeuf, Франция). Отговорите на глюкозата и инсулина са изразени като AUC, изчислена по трапецовиден метод и Net AUC, изчислена след изваждане на изходната концентрация.
Въз основа на резултатите от OGTT и концентрациите на инсулин бяха определени три показателя за инсулинова резистентност и чувствителност: оценката на хомеостатичния модел за инсулинова резистентност (HOMA 2-IR), индекс на инсулинова резистентност на черния дроб (HIRI) и индекс на мускулна инсулинова чувствителност (MISI). HOMA 2-IR беше изчислена с помощта на софтуер за калкулатор HOMA 2 IR [30] (софтуер, достъпен на https://www.dtu.ox.ac.uk/homacalculator, Оксфордски университет) и с използване на данни от OGTT, т.е. инсулинемия на гладно и гликемия на гладно бяха взети в т = 0 минути (преди поглъщането на висока доза глюкоза (1 g/kg т.т.). HIRI е продуктът на нетната AUC за кръвната глюкоза, умножена по нетната AUC за плазмения инсулин през първите 30 минути на OGTT. MISI е скоростта на разпадане на концентрацията на глюкоза в кръвта от нейната пикова стойност до най-ниската стойност, разделена на средната плазмена концентрация на инсулин по време на OGTT [31, 32].
Концентрациите на адипонектин и лептин бяха оценени на плазмени проби, използвайки ELISA методи (Плъх Adiponectin Elisa, ALPCO, и “Mouse and Rat Leptin ELISA” BioVendor®, Eurobio, Courtaboeuf, Франция). След това се изчислява LAR.
Кръвна биохимия
Измерванията на кръвната химия бяха направени в лаборатория Koné 20 (Thermo Scientific), като се използва адаптиран комплект за: активност на ASpartate AminoTransferase (ASAT) (Biomerieux), активност на ALanine AminoTransferase (ALAT) (Biomerieux), креатинин (метод на Jaffé, Fisher Brahms), албумин ( Бромокрезолов зелен метод, Biomerieux), неестерифицирана мастна киселина (NEFA) (Wako), триглицериди (TG) (PAP методи, Biomerieux), общ холестерол (Cholesterol RTU, Biomerieux). След това се изчислява съотношението ASAT/ALAT. Различни моларни съотношения бяха изчислени като част от оценката на нивата на липидите: съотношение NEFA към холестерол [33], съотношение NEFA към албумин [34] и съотношение холестерол към TG [35]. Теоретичният креатининов клирънс е изчислен с помощта на формулата Cockcroft and Gault [36], която вече е използвана в модел на плъхове [37].
Активност на цитрат синтаза (CS)
50 mg или лява камера, или ляв солеус се хомогенизират в 4 ° C Tris HCl буфер (0,1 М, рН 8,1) с Polytron. След това хомогенатът се събира и се използва незабавно за анализ. Измерванията на активността на CS се извършват по индиректен метод [28], използвайки 5,5-дитио-бис-2-нитробензоена киселина (DTNB). По този начин активността на CS беше измерена при 412 nm (Evolution 201, Thermo-Scientific).
Чернодробна хистология
Малки порции от черния дроб се вземат и веднага се поставят във фиксиращ разтвор (Bouin) за поне 48 часа. След това пробите бяха вградени в парафин и напречните филийки от 5 μm бяха нарязани и оцветени с еозин/хематоксилин за откриване на евентуална стеатоза. Класификацията на еволюцията на стеатоза се определя, както следва: резултат 0: липса на липидна капчица, оценка 1: по-малко от 10 микровезикули липидни капчици, оценка 2: повече от 10 микровезикули липидни капчици, оценка 3: макро и микровезикули липидни капчици> 30, резултат 4: стеатоза.
Статистика
Всички резултати са изразени като средни стойности ± стандартна грешка на средната стойност (SEM). Всички статистически данни са извършени с помощта на софтуера Statistica v. 12 (StatSoft, Франция). Нормалността на популацията беше тествана с помощта на теста Shapiro-Wilk. След това бяха извършени адаптирани тестове (Kruskal-Wallis, Mann и Whitney U тест, двупосочен дисперсионен анализ (ANOVA) и ANOVA за повторни измервания). ANOVA бяха последвани от post-hoc тест (HSD за n различни). Значителни разлики (стр
Резултати
Персонализиран протокол за умерено упражнение
За да се оцени ефективността на тренировъчното упражнение, нивата на активност на CS са измерени както в мускула на солеуса, така и в миокарда на лявата камера като маркер на митохондриалното съдържание в 4-те експериментални групи (Таблица 1). И в двете тъкани ET повишава активността на CS (стр Таблица 1 Активност на цитрат синтазата в две различни тъкани на 15 седмици
MAS се измерва редовно при обучени животни (Ex, ExFF), както за оценка на ефективността на ET, така и за нормализиране на индивидуалното обучение. Резултатите са обобщени в таблица 2. Преди началото на тренировката на бягащата пътека и двете групи (Ex и ExFF, възраст: 9 седмици) имат сходни MAS стойности: съответно 31,00 ± 0,67 и 29,50 ± 0,83 m/min. В групата Ex, MAS се увеличава непрекъснато на възраст 12 и 14 седмици, съответно след 3 и 5 седмици ET (стр Таблица 2 Ефект от умереното обучение върху MAS (m/min)
Морфометрични и метаболитни измервания
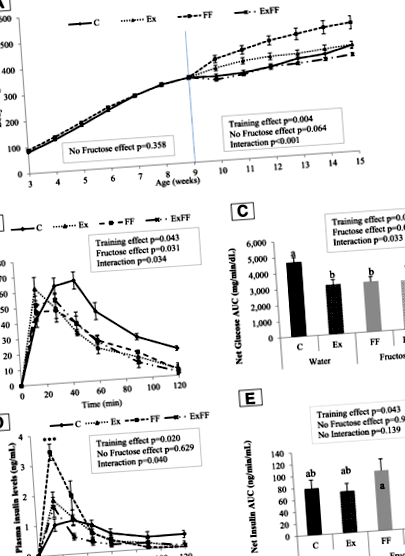
Фиг. 1а показва развитието на телесното тегло на експериментални групи. През шестте първи седмици телесното тегло е сходно между C и FF. След 9-та седмица ефектът от обучението беше значителен (стр = 0,004) и се наблюдава взаимодействие (ефект на фруктоза x тренировка) (стр Фиг. 1
Анализът на Anova 2 на кривите на OGTT (фиг. 1b) и нетната AUC на глюкоза (фиг. 1в) на възраст 13 седмици, показва, че обогатената с фруктоза диета има ефект върху нивата на глюкозата (стр = 0,031 и стр = 0,026 съответно) и ET са имали аналогов ефект (стр = 0,043 и стр = 0,020 съответно). Изненадващо, след хок тест показа по-висока нетна AUC на глюкоза за C група в сравнение с останалите (стр 0,001). Що се отнася до лептин, адипонектин и LAR, фруктозата не показва ефект и упражненията намаляват плазмените нива (стр Таблица 4 Ефекти от умерено упражнение и добавяне на фруктоза върху биохимични кръвни маркери
Чернодробна хистология
Съотношението ASAT/ALAT (фиг. 2а) е значително променено от обогатената с фруктоза диета (стр = 0,021). Взаимодействие между диетата и ЕТ (стр Фиг. 2
Еволюция на чернодробните усложнения. а - Количествено определяне на съотношението ASAT/ALAT. C: контрол (н = 7). Пример: Упражнявайте стандартна диета (n = 7). FF: добавена фруктоза (н = 8). ExFF: Упражнение с добавена фруктоза (n = 8). Стойностите са средни стойности ± SEM. Статистически разлики се наблюдават, когато малки букви (а, б) са различни. б - Оцветяване на хематоксилин и еозин в черния дроб (× 40 и × 100) за един плъх от С група и един плъх от FF група. Скала = 50 μm. Стрелка = липидна капчица. Малки липидни капчици могат да бъдат намерени само в групата на FF. ° С - Класификация на развитието на стеатоза. Скалата се определя като: Резултат 0: няма липидна капчица. Резултат 1: по-малко от 10 микровезикули от липидни капчици. Резултат 2: повече от 10 микровезикули липидни капчици. Резултат 3: макро- и микровезикули липидни капчици> 30. Резултат 4: стеатоза. Наблюдението беше извършено върху диапозитиви на всеки плъх от C (n = 8), Ex (n = 8), FF (n = 8), ExFF (н = 10). Резултатите показват процента на плъхове за всеки резултат
Дискусия
Целта на това проучване е да се оценят ефектите на персонализирания умерен ЕТ в модел на плъх с добавка на фруктоза непосредствено след отбиването, върху различни параметри, включително метаболитни измервания и биохимия на кръвта.
Предишни проучвания показват, че диета, обогатена с фруктоза (20-25% w/v в питейна вода в продължение на 12 седмици) индуциран ранен стадий на T2D, без да предизвиква затлъстяване при плъхове Wistar [12]. Със същата добавка за 21 седмици, този модел индуцира MetS без стеатоза и не винаги T2D и затлъстяване [11]. Това проучване е в съответствие с предишните ни открития относно обогатената с фруктоза диета. Всъщност, след 12 седмици обогатена с фруктоза диета, плъховете развиват повишена гликемия на гладно (Таблица 3) и IR (показана с HOMA 2-IR> 1,85), повишено телесно тегло (осигурено от увеличен общ прием на калории) и сърдечно тегло само при FF група (Таблица 3). По отношение на биохимичните маркери, теоретичния клирънс на креатинина, нивата на TG (Таблица 4) и ASAT/ALAT съотношение (Фиг. 2а) също е засегнат, без чернодробна стеатоза (фиг. 2б, в).
В нашето проучване първо оценихме ефективността на нашия персонализиран ET, използвайки активността на CS като маркер на митохондриалното съдържание [28, 39]. За двете изследвани мускули протоколът за тренировка е подобрил CS активността. Това е в съответствие с предишна констатация [40] и доказва ефективността на нашия тренировъчен протокол (Таблица 1). Освен това, MAS (Таблица 2) беше подобрена при всяко измерване, независимо от диетата, което е още едно доказателство за ефективността на нашия тренировъчен протокол [28]. Трябва да се отбележи, че производителността е била по-висока при контролните плъхове (Ex група: + 52%), отколкото при добавките с фруктоза (ExFF: + 31%, стр
Заключение
Настоящото проучване изследва влиянието на ET върху маркерите на MetS. След 6 седмици ЕТ се бори с негативните ефекти от обогатената с фруктоза диета. Нашите данни предоставиха доказателства, че ЕТ намалява телесното тегло при плъхове, хранени с фруктоза, и подобрява метаболизма на глюкозата. В действителност, хипергликемията и IR са намалени чрез повишаване на мускулната чувствителност към инсулин. Много е вероятно ЕТ да допринесе за намаляване на дисфункцията на хранената с фруктоза мастна тъкан. Въпреки това е възможно излишъкът от TG de novo синтез, индуциран от фруктоза, да не може да се компенсира от ЕТ и да допринесе за поддържане на хипертриглицеридемия. Machado и колеги (2017) [70] наскоро предложиха, че честотата и продължителността на аеробните упражнения са определящи фактори за обръщане на метаболитните нарушения в експерименталния модел на MetS, индуциран от фруктозна диета. Нашите резултати показват, че положителните ефекти върху здравето са постигнати чрез персонализирано умерено обучение от 300 минути на седмица (1 час/ден и 5 дни в седмицата) в продължение на 6 седмици. Така че е разумно да се приеме, че продължителността на нашето персонализирано обучение (6 седмици) трябва да бъде по-висока, за да се подчертаят положителните ефекти на ET.
- Обучение за упражнения при максимална интензивност на окисляване на мазнините при жени с наднормено тегло или затлъстяване в по-напреднала възраст
- Ефект на диета за елиминиране на фруктоза и лактоза при пациенти със синдром на раздразненото черво
- Ефект от 12-седмични интервенции, включващи упражнения за скандинавско ходене и модифицирана диета върху
- Ефект от консумацията на мляко с ниско съдържание на мазнини в сравнение с ябълковия сок и водата върху приема на енергия сред
- Влияние на диетата и наличността на вода върху разпространението на Rattus norvegicus (Rodentia Muridae)