Лиза Джей Роуз-Джоунс
1 Център за сърдечни и съдови грижи, Университет на Северна Каролина в Chapel Hill, САЩ
Валерия V Маклафлин
2 Сърдечно-съдови заболявания, Университет на Мичиган, САЩ
Резюме
Белодробната артериална хипертония (БАХ) е панваскулопатия, която засяга дисталните белодробни артерии и води до ограничен кръвоток. Това повишено допълнително натоварване води до адаптивни механизми на дясната камера, с евентуален отказ, след като вече не може да компенсира. Белодробната хипертония от свързани състояния, най-важното заболяване на лявото сърце, т.е. сърдечна недостатъчност, също може да доведе до същото последствие. Пациентите често изпитват ранни неясни симптоми на диспнея и непоносимост към упражнения и по този начин PH може да избегне клиницистите, докато симптомите на дясната сърдечна недостатъчност преобладават. Налични на доказателства възможности за лечение с белодробни вазодилататори са на разположение за тези с БАХ и трябва да бъдат използвани по-рано. От съществено значение е пациентите да бъдат категоризирани точно според тяхната етиология на PH, тъй като терапевтичните стратегии се различават и могат да бъдат опасни, ако се използват в грешен клиничен сценарий.
ВЪВЕДЕНИЕ
Белодробната хипертония (PH), определена като средно налягане в белодробната артерия> 25 mm Hg, все повече се разпознава и диагностицира. Това комплексно разстройство има приблизително разпространение от 10-20% сред общата популация [1]. Наблюдението на PH, независимо дали активно търсено или случайно открито при ехокардиограма или катетеризация на дясно сърце, заслужава търсене на етиологията, разбиране на патофизиологията и оценка на възможностите за лечение. Левосърдечно заболяване, усложнено от PH, има приблизително разпространение от 3-4 милиона в Съединените щати и води до двукратно повишен риск от смърт, когато настъпи десния вентрикуларен (RV) отказ [2, 3]. Докато симптомите на десностранна сърдечна недостатъчност често подтикват много клиницисти да започнат лечение или насочване, целта на този преглед е да се подобри ранната точна класификация на PH и подобрено разбиране на различните терапевтични подходи, така че те да могат да бъдат използвани по-рано в хода на заболяването.
КАТЕГОРИЗАЦИЯ И ПАТОФИЗИОЛОГИЯ
Спонсорираната от Световната здравна организация схема за клинична класификация Dana Point от 2008 г. категоризира PH в пет групи въз основа на етиологии, водещи до подобни хистопатологични промени.
СЗО група 1: Белодробна артериална хипертония (PAH)
С приблизително 15 до 25 случая на милион, истинският PAH обхваща множество етиологии и предвещава 1-годишна смъртност от около 15% при традиционна терапия [4, 5]. Той се определя като хемодинамично като средна белодробна артерия (PAP) ≥ 25 mm Hg плюс налягане на белодробен капилярен клин (PCWP) или крайно диастолично налягане в лявата камера (LVEDP) ≤ 15 mm Hg с белодробно съдово съпротивление (PVR)> 3 дървени единици [6]. Въпреки че е най-рядко срещаната форма на PH, група 1 PAH е най-широко проучваната.
По-рано известен като първичен PH, тази група включва идиопатична, фамилна предимно поради мутации в гена BMPR2, който кодира костен морфогенен протеинов рецептор, индуциран от анорексиген PH, портална хипертония, HIV, заболяване на съединителната тъкан, вродено сърдечно заболяване, милеопролиферативни нарушения и шистозомоза . PAH обикновено се причинява от васкулопатия, засягаща предимно дисталните белодробни артерии. Съдовите аномалии се характеризират с пролиферация на интимата и фиброза, съчетани с медиална хипертрофия и засилена вазоконстрикция на белодробната артерия [7]. С течение на времето се развиват сложни плексиформни лезии и васкулопатията може допълнително да се усложни от тромб на място. Тези процеси се дължат на дисбаланс в производството на ендотелин и тромбоксан А2, както мощни вазоконстриктори, така и инициатори на клетъчна пролиферация [8]. Вазоконстрикцията се засилва допълнително чрез бърза хидролиза на цикличен GMP до неактивен GMP от фосфодиестераза-5, като по този начин се нарушава вазодилататорният ендотелен отговор на азотен оксид.
СЗО група 2: Белодробна венозна хипертония (PVH) поради заболяване на лявото сърце
Белодробната венозна хипертония (PVH), дължаща се на заболяване на лявото сърце, е най-често срещаната вторична форма на PH [9]. Това е резултат от хронично повишено налягане в лявото предсърдие като последица от заболяване на лявото сърце: систолна или диастолна дисфункция на лявата камера (LV) и клапна болест. Той се определя като хемодинамично като средно белодробна артерия (PAP) ≥ 25 mm Hg плюс налягане на белодробен капилярен клин (PCWP) или крайно диастолично налягане в лявата камера (LVEDP) ≤ 15 mm Hg.
Относително малко се знае за първоначалните белодробни съдови промени, които са в основата на PVH. Предполага се, че повишеното налягане в белодробната артерия (БА) е резултат от „резервно копие“ на венозно налягане, вторично на лявопредсърдната хипертония. При подгрупа от тези пациенти получената венозна хипертония може да бъде усложнена от допълнителен „реактивен“ феномен на вазоконстрикция и ремоделиране в дисталните белодробни артерии [10]. Това съдово ремоделиране е идентифицирано в проби от аутопсии от пациенти с митрална стеноза, които разкриват типични белодробни артериални васкулопатични промени като тези, срещани в група 1 [11].
СЗО група 3: Белодробен HTN поради белодробна болест/хипоксемия
Група 3 на СЗО най-често се наблюдава в условията на хронична обструктивна белодробна болест (ХОББ), интерстициална белодробна болест (ILD) и нарушено сънно дишане. Точната честота на PH при ХОББ и ILD е неизвестна; обаче при една серия от пациенти с тежка ХОББ честотата на PH надвишава 50% [12].
СЗО група 4: Хронична тромбоемболична белодробна хипертония (CTEPH)
Група 4 на СЗО представлява PH, който е резултат от хронични белодробни тромбоемболични събития. Pengo et al. са изчислили кумулативната честота на CTEPH при пациенти с остра ПЕ и без други анамнези за венозна тромбоемболия на 3,8% след 2 години в проспективно, надлъжно проучване [13]. Белодробната артериална хипертонична артериопатия се явява движещата сила зад наблюдаваните микровазуларни промени [1]. Интралуминалният тромб води до класическа артериопатия както на малки мускулни артерии, така и на артериоли, точно дистални от частично или напълно запушен съд. Това се случва и при незатруднените съдове, които са пощадени, вероятно в резултат на високо напрежение на срязване [14].
СЗО група 5: PH поради неясни многофакторни механизми
Група 5 на СЗО е категория различни причини за белодробна хипертония с неясна патогенеза. Саркоидната белодробна болест, заболяването за съхранение на гликоген и нарушенията на щитовидната жлеза са само няколко примера, които попадат в този клас.
ПРЕЗЕНТАЦИЯ
Диспнеята е най-честият проявяващ се симптом при представяне на PH и PH винаги трябва да се включва в диференциалната диагноза за задух и непоносимост към упражнения. Срещат се оток на долните крайници и синкоп, макар и по-рядко и обикновено в по-напреднали стадии на заболяването [15]. Болката в гърдите често се пренебрегва като последица от прогресиращото PH. Ангината, дължаща се на PH, е резултат от увеличената потребност от кислород в миокарда на дясната камера (RV) поради висок стрес на стената, както и спад в систоличния кръвен поток в коронарните клони към RV и понякога компресия на лявата основна коронарна артерия от разширена главна белодробна артерия.
Тежестта на симптомите се класифицира според функционалния клас на СЗО, модифицирана форма на класификацията на Нюйоркската асоциация за сърдечна недостатъчност [16]. Функционален клас 1 на СЗО показва пациенти с PH, които нямат ограничения във физическата активност, докато клас II показва леко ограничение. Такива пациенти изпитват диспнея, умора, болка в гърдите или почти синкоп с обикновена активност, но им е удобно в покой. Маркираното ограничение определя клас III със симптоми, които предизвикват по-малко от обичайната активност. Пациентите от клас IV често имат симптоми дори в покой и проявяват признаци и симптоми на дясна сърдечна недостатъчност. Синкопът се счита за симптом от клас IV. Функционалната класификация на СЗО прогнозира прогнозата и насочва лечението.
Физикалният преглед и рентгенографията също могат да предполагат възможна диагноза на PH. При напреднал PH може да присъстват признаци на десностранна сърдечна недостатъчност. Те включват повишено югуларно венозно налягане, хепатоюгуларен рефлукс, асцит, хепатомегалия или оток на долните крайници. Аускултацията може да разкрие шум от трикуспидална регургитация, повишен пулмоничен компонент на втория сърдечен звук (P2) или галоп на дясната камера. Палпацията на прекордия може да разкрие и повдигане на RV. Прегледът на рентгенографията на гръдния кош може да разкрие разширени белодробни артерии, увеличено дясно предсърдие и контур на RV и периферна резитба.
ДИАГНОСТИЧНА ОЦЕНКА
Ехокардиография: Трансторакалната ехокардиография е първоначалният диагностичен инструмент, ако се подозира PH след анамнеза и физически преглед. Препоръчва се и скринингова ехокардиограма за клинични състояния, свързани с висока вероятност за предтестова PAH, включително известна BMPR2 мутация и системна склероза. Състояния с известен риск от БАХ, включително портална хипертония и вродени сърдечни заболявания, също трябва да имат периодични ехокардиограми, особено ако се появят симптоми, предполагащи PH [1]. Повишените прогнозни систолични налягания в белодробната артерия често се откриват случайно на ехокардиограмите и рационалният подход към такива пациенти е фокус на този преглед.
Ехокардиограмата е от основно значение за диагностиката и лечението на PH. Той предоставя оценка на систолното налягане в белодробната артерия и оценка на размера и функцията на дясното предсърдие (RA) и дясната камера (RV). Използването на възбуден физиологичен контраст може да изключи наличието на интракардиален шънт и се препоръчва като част от PH оценка [17]. От еднакво значение ехокардиограмата може също да предупреди клинициста за други често срещани състояния, свързани с PH - най-често заболяване на лявото сърце.
Няколко отделни ехо констатации могат да помогнат да се разграничи PH 2 на група 2 (PVH) от други категории. Ехокардиографските характеристики на PVH включват разширено ляво предсърдие (LA) или вентрикул (LV) и хипертрофия на лявата камера [18]. Важното е, че фракцията на изтласкване на лявата камера (LVEF) може да бъде намалена или запазена. Митралната регургитация често се визуализира и трансметралният доплер-приток разкрива бързо ранно диастолично подаване (скорост на E вълна> скорост на вълна). За разлика от това, констатациите, по-подкрепящи PAH, включват нормален размер на LA и LV с нормален до висок LVEF. Размерът на RV: LV обикновено е по-голям от 1.0 и RV „поема“ върха [19]. Моделът на трансмитралния приток е E20]. С напредването на PH и разширяването на дясната камера с течение на времето, интервентрикуларното септално изравняване може да стане изразено в съответствие с претоварването на обема на дясната камера и налягането.
Допълнително неинвазивно тестване: Систоличното налягане в белодробната артерия (PASP) може да бъде повишено по множество причини, различни от увеличеното белодробно съдово съпротивление. По този начин първоначалното тестване трябва да се съсредоточи върху идентифицирането на основната етиология. Левопредсърдната хипертония, причинена от левостранно сърдечно заболяване (клапна, систолна или диастолна дисфункция/сърдечна недостатъчност) често може да бъде открита на ехокардиограма. Сърдечните състояния с висок изход трябва да бъдат изключени, включително анемия, бременност, цироза, AV фистули или хипертиреоидизъм. Повишеното системно кръвно налягане (т.е. хронично бъбречно заболяване) също може да доведе до увеличаване на белодробния кръвен поток, което води до повишено белодробно налягане. Ако тези често срещани причини за повишен PASP са изключени, е необходимо допълнително тестване.
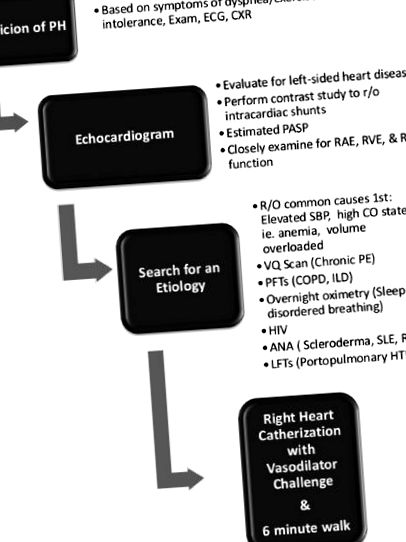
Тестът за 6 минути ходене е лесен начин за оценка на хипоксемия и силно предсказва оцеляването в популацията PAH [21]. Трябва да се получи и лабораторна оценка с антинуклеарни антитела, ХИВ и тест за чернодробна функция. Тестовете за белодробна функция, оксиметрия през нощта и сканиране за вентилация/перфузия също могат да помогнат при определянето на етиологията. Спиралната компютърна томография (CT) не се препоръчва вместо VQ сканирания поради възможността да се пропусне тромбоемболично заболяване в по-малките, по-дистални съдове [1]. (вижте фиг. 1 1 за алгоритъм).
Алгоритъм на първоначалния диагностичен подход за белодробна хипертония. Адаптиран от декларацията за консенсус за белодробна хипертония на ACCF/AHA от 2009 г.
Инвазивното хемодинамично изследване е златният стандарт в диагностиката на PH. PH е широк термин, който отразява чисто повишеното налягане на PA, конкретно дефинирано като среден PAP> 25. Катетеризацията на дясното сърце (RHC) е следващата стъпка в диагностичния алгоритъм за пациенти, за които се смята, че имат вероятно PAH, форма на PH, за да разкрие дали е налице истинска съдова обструкция. Ключовата характеристика е повишено белодробно съдово съпротивление (PVR)> 3 дървесни единици [1]. RHC също е жизненоважен за разграничаването на PAH (PCWP ≤ 15) от PVH (PCWP> 15) [22]. Основните измервания включват насищане с кислород (в горната и долната куха вена, както и PA и системната артерия), RA и RV налягане, систолично/диастолично/средно PAP, PCWP, сърдечен дебит и PVR. Трябва да се използват стандарти за качество по време на измерване на хемодинамиката [23]. Формите на вълната под налягане трябва да се измерват в края на изтичането. Ако PCWP е изобщо несигурен, трябва да се измери диастоличното налягане в края на НН [24]. RHC обикновено се понася много добре с докладван 1,1% риск от нежелани събития, включително аритмии, хематоми и пневмоторакс [25]. В голям многоцентров регистър от 7 218 процедури общата смъртност, свързана с процедурите, е 0,055%.
RHC не само предоставя потвърждаваща диагноза, но помага за определяне на прогнозата и позволява оценка на белодробната вазореактивност. Вазодилататорните предизвикателства са съществен компонент на инвазивната хемодинамика за лица с БАХ от група 1. Положителният отговор на белодробното вазодилататорно предизвикателство се определя като намаляване на средното налягане на PA от поне 10 mmHg до абсолютна средна стойност по-малко от 40 mmHg [26] без намаляване на сърдечния обем. Положителният тест предсказва безопасността на реакцията към блокерите на калциевите канали, по-често наблюдавана в групата на идиопатичните ПАХ. Пациентите без данни за „реактивна“ белодробна васкулатура обикновено имат по-напреднало заболяване и трябва да се обърне сериозно внимание за по-агресивно лечение [27].
Инхалираният азотен оксид обикновено е предпочитаният агент за тестване на остри вазодилататори, като се има предвид лекотата на употреба и ограничените неблагоприятни ефекти. Интравенозният епопростенол и аденозин са алтернативи, въпреки че те са по-тромави за прилагане и могат да имат допълнителни неблагоприятни ефекти. Трябва да се внимава при прилагането на тези средства при пациенти със съпътстващо заболяване на лявото сърце, тъй като белодробният оток може да бъде предизвикан евентуално чрез селективна артериална вазодилатация, водеща до наводняване на капилярното легло от повишено ляво предсърдно налягане [28].
PH: Прогресивна болест
С напредването на PH PVR продължава да се повишава, отразявайки текущите анормални структурни промени в белодробното артериално легло. Повишеният PVR се увеличава след натоварване към RV, което е тънкостенна структура, по-подходяща за система с много по-ниско налягане. Първоначално налягането в белодробната артерия се повишава, докато RV започне да отпада, което води до намаляване на ударния обем на дясната камера. Тогава налягането на PA може да започне да намалява и налягането на RA може да се повиши, като и двете са зловещи прогностични признаци [29].
Оценката на хемодинамиката е от съществено значение за стратифициращите риска пациенти с PH, до голяма степен, защото отпадането на RV драстично влошава прогнозата. В регистъра REVEAL, съвременно наблюдение на PAH, средното дясно предсърдно налягане (RAP) е обратно свързано с преживяемостта [30]. Налягане в дясното предсърдие по-малко от 10 mmHg със сърдечен индекс над 2,5 L/min/m2 предоставя нисък риск. Напротив, дясното предсърдно налягане над 20 mmHg и сърдечният индекс под 1,0 L/min/m2 поставят пациента в по-висок риск [31]. Клиничните данни за десностранна сърдечна недостатъчност, значително повишен BNP, функционален клас IV на СЗО и бързо прогресиране на симптомите показват необходимостта от агресивно лечение [1]. Тестът за 6 минути ходене на по-малко от 300 метра трябва да предизвика безпокойство. Тестовете за сърдечно-белодробни упражнения могат да бъдат полезни прогностично, а пикът на VO2 над 10,4 ml/kg/min предполага по-леко заболяване [32].
Ехокардиографската оценка на RV помага да се класифицират и пациентите. Минималната дисфункция на RV съответства на ниския риск, докато значително увеличаване и дисфункция предполага пациент с по-висок риск [33]. С напредването на PH геометрията на RV се променя като компенсаторен механизъм за продължително увеличаване на допълнителното натоварване. RV първоначално се удължава надлъжно и след това в диаметъра на напречното си сечение. В крайна сметка последното причинява поклон в НН, тъй като RV придобива по-овална форма [32]. Идентифицирането на деснокамерна недостатъчност е наложително, тъй като е основен определящ фактор за заболеваемост и смъртност [33].
ТЕРАПЕВТИЧНИ ВАРИАНТИ
СЗО група 1: PAH
Блокери на калциевите канали (CCB), включително амлодопин, дилтиазем и дългодействащ нифедипин, могат да се използват при пациенти, които показват остър отговор на вазодилататорно предизвикателство. Истинските отговорили обикновено са необичайни. В едно проучване само 6,8% от общия IPAH са имали положително предизвикателство и са поддържали дългосрочния си отговор на CCB [34]. Системната хипотония обикновено е най-често срещаният неблагоприятен ефект. Пациентите, започнали лечение с CCB, трябва да бъдат внимателно наблюдавани, за да се наблюдава устойчива ефикасност.
Интравенозният епопростенол е първият агент, който увеличава преживяемостта в допълнение към подобряването на хемодинамиката и симптомите при пациенти с тежка БАХ [42]. Типичната начална доза епопростенол е 2 ng/kg/min с титруване нагоре до 20-40 ng/kg/min. През последните няколко години са одобрени и други аналози на простациклин. Iloprost се вдишва шест до девет пъти дневно в доза от 2,5 или 5 µg/доза. Treprostinil се предлага в множество формулировки, включително интравенозно, подкожно и инхалирано (3 до 9 инхалации четири пъти дневно). Употребата на простациклини обикновено е запазена за най-болните пациенти с БАХ, които не реагират на други лекарствени терапии. Неблагоприятните ефекти включват главоболие, зачервяване, обрив, диария и болка в челюстта. Трябва да се внимава, тъй като прилагането на тези средства при пациенти с повишено ляво налягане на пълнене вляво може да доведе до светкавичен белодробен оток [43]. Ако PAH-специфичните терапии се считат за оправдани при пациенти с основно белодробно заболяване, трябва да се внимава, тъй като увеличеният приток на кръв към невентилирани алвеоли може да влоши диспнея и хипоксемия чрез това V/Q несъответствие [1].
Трансплантацията на белите дробове остава единственото окончателно лекарство за БАХ и се разглежда при тези, които не се подобряват въпреки оптималната медицинска терапия. Предсърдната септостомия може да се използва палиативно при пациенти в краен стадий с БАХ, които не са кандидати за трансплантация, или при такива, които очакват трансплантация [44, 45].