Кореспонденция на: Габрио Басоти, професор, Секция по гастроентерология и хепатология, Отделение по клинична и експериментална медицина, болница Санта Мария дела Мизерикордия, Пиацале Менгини, 1, 06153 Сан Систо (Перуджа), Италия. ti.nit@tossabag
Телефон: + 39-75-5784423 Факс: + 39-75-5847570
Резюме
Възпалителните заболявания на червата (IBD) представляват важни хронични състояния, засягащи стомашно-чревния тракт при човека. Подобни нарушения обаче се откриват при няколко животински вида и IBD, засягащи кучетата, са особено важни. Те са обхванати от чадър от вероятно няколко различни образувания с общи симптоми, някои от които изглежда споделят поразителни прилики с човешките условия. Този преглед ще се съсредоточи върху действителното познаване на IBD при кучета и ще се опита да идентифицира разликите и приликите със състоянията на IBD при хора.
ВЪВЕДЕНИЕ
Възпалителните заболявания на червата (IBD) са добре известни стомашно-чревни разстройства при хората; тези нарушения обаче също присъстват и често се изследват при животни [1]. IBD при човека [болест на Crohn (CD) и улцерозен колит (UC)] може да се определи като хронични идиопатични мултифакторни заболявания [2,3]. CD обикновено е заболяване на илеума и дебелото черво, но може да засегне и други области на храносмилателния тракт [4], образува грануломи и обхваща цялата чревна стена, докато UC е язвено и възпалително заболяване, обикновено ограничено до повърхностни слоеве (лигавица, повърхностни част от субмукозата) на дебелото черво [5].
Кучетата също могат да развият IBD [6], като част от хроничните ентеропатии, ако продължават повече от три седмици [7], и са правилно дефинирани, когато има хистологична демонстрация на възпаление на лигавицата и всички други възможни причини за ентерит/инфилтрати са изследвани и изключени [7-10]. Ентеритът се класифицира в зависимост от това кои преобладаващи клетки инфилтрират чревната стена и къде се извършва тази инфилтрация [11].
По този начин, хроничните заболявания на тънките черва, които могат да бъдат включени сред IBD, са лимфоцитно-плазмоцитен ентерит (LPE), еозинофилен ентерит и еозинофилен гастро-ентерит (EGE) [10]. По отношение на дебелото черво при IBD се признават четири основни състояния: лимфоцитно-плазмоцитен колит, еозинофилен колит, хистиоцитен улцерозен колит (HUC) (главно PAS-положителни макрофаги) и регионален грануломатозен колит (главно PAS-отрицателни макрофаги) [10,12-16]. Струва си обаче да се отбележи, че подобни заболявания често могат да включват както тънките, така и дебелите черва, или дори да включват стомаха: лимфоцитно-плазмоцитен ентероколит, еозинофилен ентероколит (ЕИО) или гастроентероколит (EGEC) и грануломатозен гастроентерит [8,10,13,15].
При кучетата друг важен хроничен ентерит, чиито причини все още не са ясно определени, но са широко изследвани и за които са изложени хипотези на основните алергични фактори, е така наречената диария, отговаряща на храните (FRD) [6]. Това заболяване е особено важно, тъй като често се включва в диференциалната диагноза на IBD.
Счита се, че IBD има еднаква честота при мъже и жени, а кучетата на средна възраст изглежда са по-засегнати [10]. По отношение на предразположението към порода, това се предполага за някои специфични форми на IBD, като имунопролиферативна ентеропатия при Basenjis, ентеропатия, губеща протеини и свързана нефропатия, губеща протеини, при меко покрити пшенични териери и HUC при боксьори [10,11]. Въпреки това, въпреки че HUC проявява по-висока предразположеност при боксьорите [17], той е описан и при други породи кучета като френски булдог, доберман пинчер, мастиф и аляски маламут [16,18].
ПАТОГЕНЕЗА
Информация при кучета
Смята се, че при кучетата развитието на IBD възниква в резултат на дерегулация на лигавичния имунитет при предразположени животни [14]. Загубата на толерантност към антигени (храна, чревни бактерии и др.) Е един от най-изследваните механизми, които биха могли да оправдаят развитието на хронично чревно възпаление [8,11,19]. Имуно-медиираната основа на заболяването може да се изведе от отговора на приложението на имуномодулиращи лекарства; присъствието на повишени IgE положителни клетки при болни кучета е допълнителен аспект, който също предполага участието на реакции на свръхчувствителност в патогенезата на кучешки IBD [20], както и повишената концентрация на еозинофили и мастоцити при много кучета с EGE [8]. Прекъсването на лигавичната бариера, независимо от основната причина (бактериална, химическа и др.), Може също да доведе до по-нататъшно излагане на антиген, позволявайки на процеса да стане хроничен [21] и се налага от намалена апоптоза на лимфоцитите, както е показано кучета с IBD в сравнение с контролни кучета [22].
Хомеостазата вътре в храносмилателния тракт се поддържа от равновесието между реакциите към патогени и коменсални бактерии или други неотвратителни луминални антигени (толерантност), медиирани от различни молекули [23]. Наличието на лигавична толерантност към безвредни антигени е много важно, тъй като в зависимост от липсата му последващият възпалителен отговор може да бъде преувеличен и дори вреден. Подобна толерантност вероятно се основава на факта, че антигенът е представен или не, в контекста на други сигнали за опасност [10,24]. Разликата между толерантността и реакцията се основава също и на рецепторите за разпознаване на образци (PRR) [25], които са способни да разпознават микрофлората според техните молекулярни модели, свързани с патогени или молекулни модели, свързани с микроби [26].
Подобно на хората, изследването на IBD при засегнати кучета доведе до хипотезата, че генетичните фактори и ентеричните бактерии могат да играят ключова роля в патогенезата на тези нарушения, поради анормалния чревен отговор на коменсалната микрофлора [26]. Веднъж стимулирани, PRR като Toll-подобни рецептори (TLR) [27] започват своята противовъзпалителна активност, а скорошно проучване показа, че три TLR (2, 4 и 9), стимулирани от бактерии, се регулират нагоре при кучета с IBD [26]. Тези резултати са подобни на тези след активирането на TLR4, което е демонстрирано при хора, страдащи от IBD [28]. При тези пациенти както генетичната предразположеност, така и факторите на околната среда се считат за важни елементи в развитието на заболяването. Освен това, както вече е добре известно при хората [29,30], скорошно проучване показа, че при кучетата с IBD тънките чревни бактерии се различават от тези при здрави кучета [31], засилвайки идеята за корелация между микрофлората и IBD.
По този начин, дори при малки животни и подобно на това при човека, разпределението на подгрупата на чревните лимфоцити и основните антигени от клас II на хистосъвместимост, както и експресията на цитокинен ген и други маркери, са дали интересни и понякога припокриващи се резултати [9,32-36] . Например, едно проучване показа, че кучетата с IBD показват по-голям брой IgE положителни клетки от здравите кучета, по начин, подобен на този за експресията на интерлевкин 4 (IL-4) при човек с IBD [20]. В допълнение, модулацията на експресията на чревна ламина propri лимфоцити P гликопротеин (P-gp) изглежда играе подобна роля както при IBD при хора, така и при кучета. В действителност, при пациенти с IBD, слабо реагиращи на лечение със стероиди, P-gp е силно експресиран, а при кучета, показващи добър отговор на лечение, този протеин е слабо представен [37].
Както беше документирано по-рано при хора, при кучета с IBD изследването на специфични подгрупи на клетъчни популации доведе до демонстрация на намален брой мастоцити (MC) и до увеличаване както на CD3 + клетките, така и на IgG + плазмените клетки [38].
Във ветеринарната медицина обнадеждаващи резултати произхождат и от изследването на ядрени рецептори (NRs, вероятно също участващи в генезиса на IBD при човека), като свързан с пероксизомен пролифератор рецептор α (PPARα) и особено на NR целеви гени [като мулти -лекарствен резистентност ген-1 (MDR1)], множество протеини, свързани с лекарствена резистентност (MRP2), цитохром P450 (CYP3A12) и фенолсулфатираща фенолсулфотрансфераза (SULT1A1) [39,40]. В скорошно проучване беше подчертано, че MRP2, CYP3A12, SULT1A1 и PPARα са по-изразени при кучета FRD и/или IBD и че MDR1 може също да прави разлика между тях [21]. Освен това, в проучване върху немски овчарски кучета с IBD, експресията на mRNA на много цитокини като IL-2, IL-5, IL-12p40, интерферон-γ (IFN-γ), фактор на туморна некроза-α (TNF-α ), а трансформиращият растежен фактор -β1 (TGF-β1) е доказано по-висок при болните животни в сравнение с контролите [34]; трябва да се има предвид обаче, че други проучвания преразглеждат повишената експресия на някои цитокини при кучета с IBD [35,36].
Информация при хората
IBD при човека, особено CD, вероятно разпознава генетично предразположение и много гени като NOD2/CARD15, HLA и IL-1-Ra гени са изследвани и се смята, че са замесени в развитието на CD [41-43]. Въпреки това, факторите на околната среда [44,45] и чревната микробиота също могат да бъдат включени в IBD [46-49], както е показано от факта, че антибактериалните лекарства могат да помогнат за контролиране на симптомите [50-52]. Важен момент за продължаване на увреждането при IBD при хора е, че веднъж стимулирани, лимфоцитите са склонни да се натрупват в собствената ламина, тъй като изглеждат по-устойчиви на апоптоза [53]. Освен това дисбалансът между провоспалителните и противовъзпалителните цитокини също може да играе роля [54].
При човека ядреният фактор κB (NF-κB) също е свързан с IBD [55] и е показано, че IL-23 може да доведе до диференциация на Th17 лимфоцитите, произвеждащи IL-17 с последващо активиране на NF-kB провъзпалителни сигнали [56]. В скорошно проучване връзката между IBD и NF-κB също е хипотезирана при кучета, където биопсични проби от кучета с IBD показват, че наличието на активиране на NF-κB в макрофагите на lamina propria е по-високо, отколкото в контролната група [23].
Разлики между видовете
Важно развитие в хуманната медицина показва различното участие на подтиповете на лимфоцитите (Th1 и Th2) в IBD, като Th1 е замесен главно в CD, докато Th2 преобладава в UC [57], с последващо различно активиране на цитокини [23]. При кучета, различни от човека, има смесено активиране на Th1 и Th2 при IBD [6,23,38], което води до различна експресия на някои цитокини, въпреки че наскоро беше изказана хипотезата, че различни Th клетки могат да участват в различни IBD видове [8]. Някои автори са показали, че MC може да бъде увеличен или намален в зависимост от преобладаващия клетъчен инфилтрат и че те са предимно редуцирани в LPE и увеличени в EGE, като по този начин предполагат възможен различен генезис за двата вида IBD (Th1 за LPE и Th2 за EGE) [8].
Въпреки че горните проучвания означават активен интерес към патогенезата на IBD, също така е очевидно, че механизмите, които стоят зад болестта, далеч не са разбрани, както при хора, така и при кучета. HUC, особено състояние, при което централната роля на бактериите е предложена поради наличието на интралезионални микроби и PAS + макрофаги, подобно на болестта на Whipple при човека [7].
КЛИНИЧНИ И ДИАГНОСТИЧНИ АСПЕКТИ
Клиничните прояви на IBD при кучета са многобройни и неспецифични; най-честите клинични признаци са загуба на тегло, постоянно или повтарящо се повръщане и/или диария [8], често свързани със симптоми, които са израз на евентуални усложнения, като асцит (ако има хипоалбуминемия) или бледност на лигавиците (в случай на хронично стомашно-чревно кървене) [11,58].
Преди да се постави диагноза IBD е важно да се изключат всички други възможни причини за хроничен ентерит [6,59] чрез пълен клиничен преглед, лабораторни изследвания и инструментални изследвания, включително биопсични проби за хистологична оценка. Корекцията на диетата също е важен инструмент за изключване или евентуално потвърждаване на FRD [23].
Тъй като при кучета диагнозата IBD е чрез изключване, очевидно е, че много тестове, извършени по време на диагностичния итер (например изследвания на кръв, урина и фекалии), са необходими за изключване на други причини за възпаление и рядко са специфични за IBD, поради което без да надценява честотата на такава диагноза [10]. Този аспект е много важен, тъй като ако причината за хроничния ентерит е неправилно диагностицирана и се третира като IBD, е малко вероятно да се разреши [58].
При диагностицирането на IBD инструменталната диагностика е важна и често от първостепенно значение, въпреки че от трите най-използвани техники, т.е. рентгенология (XR), ултрасонография (US) и ендоскопия, само последната дава по-конкретна информация за диагностицирането на IBD (Фигура (Фигура 1), 1), особено тъй като позволява биопсични проби, които са необходими за разграничаване на различните подтипове на лигавичната инфилтрация [60]. XR и US (които дават важна информация за натрупването на червата и дебелината на стените) изглеждат по-полезни за изключването на други възможни причини [61] и тъй като значението на удебеляването на чревната стена при кучета с IBD наскоро беше преоценено [10, 62,63].
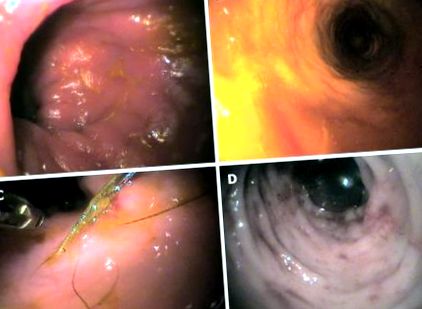
Представителни ендоскопски изображения при кучето. A: Лимфоцитно-плазмоцитен колит; Б: Макрофоликуларен и дифузен интерстициален лимфоцитен колит; С: Хистиоцитен колит; D: Неутрофилен-еозинофилен колит.
След като са изключили най-честите причини за хронични ентеропатии, чревните биопсии, получени хирургически или ендоскопски в зависимост от обстоятелствата (ендоскопията е по-малко инвазивна, но вземането на проби е ограничено по отношение на мястото на изпълнение и/или измерението), могат да позволят диагностицирането на IBD [10] (Фигура (Фигура2). 2). Важно е обаче да се подчертае, че биопсичните проби не могат да бъдат недвусмислено интерпретирани [6,10,64], въпреки че неотдавнашната работа помогна за изясняването на тази интерпретация, като предостави хистопатологичен резултат за промени в лигавицата при кучета [65].
Представителни хистологични изображения при кучето (HE, бар = 50 μm). О: Лимфоцитно-плазмоцитен колит. Обърнете внимание на интерстициалния дифузен модел на инфилтрат, представен от голямо количество лимфоцити, смесени с плазмени клетки и някои макрофаги; Б: Лимфоцитно-плазмоцитен колит (фоликуларен вариант); C: Хистиоцитен колит. Тежки аномалии на лигавицата със загуба на крипти и дифузна инфилтрация от големи макрофаги (стрелки), които във вложката (PAS петно) са показани като основни клетки, инфилтриращи ламина проприа; D: Еозинофилен колит. Обърнете внимание на наличието на голям брой еозинофили (стрелки).
При хората, за диагностициране и/или за наблюдение на IBD, серологични маркери като анти-неутрофилни цитоплазматични антитела (p-ANCA), анти-Saccharomyces cerevisiae (ASCA), антитяло на порина С на външната мембрана (anti-OmpC), анти-ламинарибиозид антитяло, анти-манобиозидно антитяло и анти-хитобиозидно антитяло, анти-панкреас Ab и анти-калициформни чревни клетки Ab, фекален калпротектин, лактоферин и полиморфно-ядрена неутрофилна еластаза са налични и са тествани, въпреки че не всички те се използват в клиничната практика [66-68].
Ако диагностиката на заболяването изисква дълъг и пълен диагностичен план, важни инструменти за клинична оценка на IBD са индексът на кучешката хронична ентеропатия и индексът на кучешка IBD активност (CIBDAI) (подобен на индекса на активността на болестта на Crohn при човек [74] ), което също позволява проследяване на пациента по време на лечението [75-77], въпреки че CIBDAI изглежда не корелира с хистопатологичната степен [73]. Един важен аспект при управлението на IBD е, че е много трудно да се предвиди изходът на пациента; за щастие, много важни маркери наскоро бяха проучени като прогностични показатели, като имунореактивност на кучешката панкреатична липаза (cPLI), концентрация на кобаламин и албумин [78-80].
ЛЕЧЕНИЕ
Както и в хуманната медицина, основните трудности при лечението на кучета с IBD произхождат от непълно разбиране на патофизиологичната основа на тези заболявания; по този начин не е изненадващо, че в много случаи терапевтичните протоколи са частично заимствани от приетите при човека [23,78]. Обикновено избраните терапевтични протоколи за IBD при кучета зависят от сериозността на заболяването и в крайна сметка от резистентността към някои лекарства. Някои пациенти, като тези с FRD, могат да подобрят или дори да разрешат състоянието си след простото прилагане на специфична диета, като тези на базата на хидролизирани протеини [58].
Като цяло първият подход при кучета с IBD обикновено включва някаква диетична модификация, използването на пребиотици-пробиотици [10,11], антимикробни средства и в крайна сметка кортикостероиди (преднизолон или, напоследък, будезонид) [58]. Метронидазолът представлява важно терапевтично средство поради едновременното му антимикробно и имуномодулиращо действие [10,58]. Други имуномодулиращи или противовъзпалителни лекарства, като азатиоприн, циклоспорин, хлорамбуцил, циклофосфамид и 5-аминосалицилати, могат да се прилагат като алтернатива или заедно със стероидите, в зависимост от молекулата [10,12,58,78]. При лечение на куче с IBD е важно също така да се добавят симптоматични терапевтични мерки като гастропротектори, антиеметици, модулатори на подвижността и др. И да се коригира всеки възможен дисбаланс (например чрез добавяне на кобаламин или електролит) [10,58].
Като се има предвид, че познаването на моделите на цитокините, участващи при пациенти с IBD при хора, е важен инструмент при разработването на нови терапевтични стратегии [61], това може да предостави и нови терапевтични инструменти във ветеринарната медицина [10,58]; резултатите от скорошно проучване върху чревни биопсии от кучета с IBD, оценяващо рецептора на растежен хормон и експресия на mRNA, подобен на инсулиновия растежен фактор (IGF-1/-2), дават допълнителни перспективи за лечение на IBD [82].
ЗАКЛЮЧЕНИЕ
Към днешна дата връзката между IBD при хора и кучета не е напълно дефинирана, особено по отношение на патофизиологията и терапевтичните протоколи; по този начин от аспектите, изследвани при човека, само няколко вероятно биха могли да бъдат успешно преведени на кучета. Всъщност IBD в последния показва няколко и някои поразително различни форми по отношение на хората, при които тези заболявания показват по-стандартизирани клинични, ендоскопски и патологични аспекти.
Както обаче предлагат някои автори [83,84], паралелното изследване на IBD при животни също може да доведе до важна информация за човека [85] и да се надяваме да разработим по-добри терапевтични мерки за облекчаване на тези проблеми при нашите кучешки приятели и другари.
Бележки под линия
Рецензент: д-р Пингчанг Янг, д-р, катедра по пахтология и молекулярна медицина, Университет Макмастър, BBI-T3330, 50 Charlton Ave East, Хамилтън, L8N 4A6, Канада
S- редактор Tian L L- редактор Webster JR E- редактор Lin YP
- Възпалителна болест на червата Котка лекар
- Клиника по възпалителни заболявания на червата, Храносмилателни услуги UW Health Madison, WI
- Възпалително заболяване на червата Причини, симптоми и лечение
- Възпалително заболяване на червата, свързано с нездравословни храни MinnPost
- Възпалителна болест на червата (IBD)