Липолизата се определя като хидролитично разцепване на естерни връзки в триглицериди (TG), което води до генериране на мастни киселини (FA) и глицерол.
Свързани термини:
- Инсулинова резистентност
- Глюконеогенеза
- Глюкоза
- Липиди
- Мастна киселина
- Ензим
- Протеин
- Инсулин
- Затлъстяване
- Мастна тъкан
Изтеглете като PDF
За тази страница
Липолиза
Тъй като глицеролът, освободен чрез липолиза, не може да бъде рефосфорилиран в адипоцитите, обяснете как се образува глицерол 3-P за образуване на TG.
Идентифицирайте транспортера на глюкозата в клетъчните мембрани на адипоцитите, както и вътреклетъчните пътища, достъпни за глюкозата.
Знаете как инсулинът, епинефринът, тироксинът и глюкокортикоидите влияят върху липолизата на мастните клетки и/или отлагането на TG.
Идентифициране и обсъждане на ендокринния контрол на LPL, аденил циклаза, HSL, циклично-AMP-зависима активност на фосфодиестераза и протеин киназа.
Обяснете как и защо голяма част от FFA, отделена по време на липолиза на адипоцити, се използва при реестерификацията на глицерол 3-P по време на глад.
Обсъдете предложените роли на лептин, грелин и обестатин в поведението при хранене.
Посочете как метаболизмът на кафявата мастна тъкан спомага за терморегулацията.
Идентифицирайте и обсъдете факторите, действащи в или върху мастната тъкан, които помагат за регулиране на плазмената концентрация на FFA.
Невробиологията на циркадното време
Риан ван дер Спек,. Андрис Калсбик, в Напредък в изследванията на мозъка, 2012 г.
Липолиза
Липолизата е катаболният процес, водещ до разграждането на триацилглицеролите (TAGs) до FFAs и глицерол. След освобождаване в кръвта, FFAs се транспортират и поемат от други тъкани, за да се използват за β-окисление и последващо генериране на АТФ. Някои FFA не напускат мастната клетка и се реестерифицират във вътреклетъчен TAG. По време на липолизата вътреклетъчната TAG се подлага на хидролиза чрез действието на три основни липази: мастна триглицеридна липаза (ATGL/деснутрин/фосфолипаза A2ζ), HSL и моноацилглицерол (MGL) липаза. ATGL хидролизира TAG в диацилглицерол (DAG) и един FA, последван от HSL, превръщайки DAG в моноацилглицерол (MAG) плюс един FA, след което MGL хидролизира MAG, за да произведе глицерол и трети FA (Ahmadian et al., 2010; Lafontan and Langin, 2009 ).
Липолизата се регулира от ANS (Bartness et al., 2010a) и от няколко хуморални фактора, като катехоламини (фосфорилиране на HSL), глюкокортикоиди (повишаване на ATGL), натриуретични пептиди и растежен хормон (Ahmadian et al., 2010; Лафонтан и Лангин, 2009). Докато системната регулация на липолизата е относително добре характеризирана, остава много да се проучи по отношение на местната регулация на липолизата в адипоцитите от (автокринни/паракринни) фактори. Адипоцитите секретират няколко фактора, способни да регулират локално липолизата, като TNFα, който стимулира липолизата, и аденозин, който инхибира липолизата (Ahmadian et al., 2010).
Методи за биология на мастните тъкани, част Б
Мартина Швайгер,. Ахим Лас, в Методи в ензимологията, 2014
Резюме
Липолизата се определя като хидролитично разцепване на естерни връзки в триглицериди (TG), което води до генериране на мастни киселини (FA) и глицерол. Двата основни TG пула в тялото на гръбначните животни включват вътреклетъчни TG и плазмени/хранителни TG. Съответно, това води до дискриминация между вътреклетъчна и интраваскуларна/стомашно-чревна липолиза, съответно. Тази глава се фокусира изключително върху вътреклетъчната липолиза, наричана тук липолиза. Липолитичното разцепване на TG се осъществява по същество във всички клетки и тъкани на тялото. Във всички тях получените ФА се използват ендогенно за производство на енергия или биосинтетични пътища с едно изключение, бяла мастна тъкан (WAT). WAT освобождава FAs и глицерол, за да доставя неадипозни тъкани по време на лишаване от хранителни вещества. Основната роля на липолизата в липидната и енергийната хомеостаза изисква точното измерване на липазната активност и липолитичните нива. Неотдавнашното откритие на нови ензими и регулатори, които медиират хидролизата на TG, направи тези измервания по-сложни. Тук описваме подробна методология за измерване на липолизата и специфичните ензимни активности в клетките, органите и съответните им екстракти.
Чернодробна токсикология
9.10.5.1 Източник на мастни киселини за чернодробна стеатоза чрез липолиза
Липолизата в адипоцитите е под строг хормонален контрол. Катехоламините, взаимодействащи с β-адренергичните рецептори, стимулират липолизата и инсулинът противодейства на това, за да потисне липолизата (Holm et al. 2000). Пациентите с NAFLD проявяват неспособност за инсулин да потиска периферната липолиза, допринасяйки за повишена FFA в кръвообращението (Sanyal et al. 2001). Проучванията in vivo за стабилни изотопи при пациенти с NAFLD също предполагат, че неподходящата липолиза в мастната тъкан допринася за триглицеридите, натрупани в черния дроб (Donnelly et al. 2005).
Въпреки че няма налични данни от хора с ALD, при животински модели хроничното хранене с етанол води до нарушаване на липолизата в мастната тъкан. Хроничният етанол уврежда способността на инсулина да потиска мастната липолиза, което води до намаляване на скоростта на поява на глицерол в кръвообращението (Kang et al. 2007a). Тази инсулинова резистентност се наблюдава както при адипоцити, изолирани от плъхове, хранени с етанол, така и in vivo при контролирани условия на хиперинсулинемично-евгликемична скоба (Kang et al. 2007a). В проучвания, използващи 2 H2O като индикатор, скоростта на оборота на триглицеридите в мастната тъкан на епидидима се увеличава след хранене с етанол (Kang et al. 2007a). Хроничното хранене с етанол увеличава разграждането на триглицеридите с 2,3 пъти в сравнение с плъховете, хранени с двойки, но няма ефект върху синтеза на триглицериди (Kang et al. 2007a). Взети заедно, тези данни показват, че дълбоката дисрегулация на липолизата в мастната тъкан вероятно допринася за прогресирането на чернодробната стеатоза както при NAFLD, така и при ALD.
Адипоцити в нормалната биология на тъканите
Регулиране на липолизата
Липолизата се предизвиква от активирането на аденил циклаза, която превръща аденозин трифосфат (АТФ) в цикличен аденозин монофосфат (сАМР). Катехоламините, действащи чрез бета-адренергични рецептори (βADR), стимулират аденил циклазата, но това действие се противодейства чрез активиране на алфа-адренергичния рецептор (αADR). Следователно нетният ефект от адренергичната стимулация на адипоцитите се определя от броя и афинитета на αADR и βADR върху мембраната на адипоцитите. На гладно глюкокортикоидите усилват регулацията на транскрипцията на ATGL, докато в състояние на хранене инсулинът активира фосфодиестераза 3В, която намалява сАМР и по този начин инхибира липолизата. Чрез алтернативни пътища, включващи цикличен гуанозин монофосфат и PKA сигнализиране, предсърдният натриуретичен пептид и мозъчният натриуретичен пептид могат да стимулират липолизата.
В допълнение към тези неврологични и ендокринни контролери, липолизата е под местен контрол и от автокринните/паракринните действия на няколко адипокини, като фактор на туморна некроза (TNF) -α, който стимулира липолизата, и аденозин и специфична за мастната тъкан фосфолипаза А2, които инхибира го. Те са описани по-нататък в разделите за тумор некрозис фактор алфа и други адипоцитокини.
Адипоцитите от различни видове и от различни депа в едно и също животно се различават в отговора си на липолитичния ефект на адренергичната стимулация. При хората висцералната абдоминална WAT показва по-голям липолитичен отговор на катехоламини, отколкото подкожната WAT (вижте раздела „ Депо-специфични разлики в биологията на мастната тъкан и адипоцитите ’). Дори в рамките на подкожното депо има специфични за мястото разлики, например при възрастни жени адипоцитите в глутеалната WAT демонстрират по-малко липолиза в сравнение с адипоцитите в коремната подкожна WAT.
Промени в храненето и телесната маса при сърдечна недостатъчност
Мастна тъкан (вж. Също глава 20)
Липолизата се контролира главно от ензим-хормон-чувствителната липаза. Той се активира главно от катехоламини чрез -адренорецептори. Натриуретичните пептиди (предсърдни, В-тип и С-тип натриуретични пептиди) наскоро бяха идентифицирани, че участват в метаболизма на мастните клетки. 128 Натриуретичните пептиди контролират липидната мобилизация и липидното окисление чрез увеличаване на вътреклетъчния cGMP и липолиза. 129 Те също така намаляват производството на лептин, увеличават циркулиращите свободни мастни киселини и увеличават инсулиновата резистентност. 130
Инсулинът е основното антилиполитично вещество. Загубата на мастна тъкан при пациенти с кахексия може да бъде медиирана от повишена липолиза или намалена липогенеза. 131 Данни от проучвания на пациенти с ракова кахексия сочат факта, че преобладаващият механизъм е повишената липолиза. Всъщност плазмените нива на глицерол на гладно, които отразяват разграждането на триглицеридите, са по-високи при пациенти с рак със загуба на тегло, отколкото при тези без. 132 133 Това не е доказано при пациенти със сърдечна кахексия или пациенти с ХСН; въпреки това е изкушаващо да се предположи, че повишените нива в катехоламините и евентуално натриуретичните пептиди могат да бъдат отговорни за загубата на мастна тъкан, която се наблюдава при такива пациенти. 119 TNF-α, който също е свръхекспресиран както в CHF 134, така и в сърдечната кахексия, 90 играе основна роля в липолизата на мастните клетки и инхибирането на инсулиновата сигнализация. Последното е важен аспект при развитието на инсулинова резистентност.
Методи за биология на мастните тъкани, част Б
Емилио П. Мотилио,. Джеймс Г. Граннеман, в Методи в ензимологията, 2014
Резюме
Вътреклетъчната липолиза е важен клетъчен процес в ключови метаболитни тъкани и макар да се знае много за ензимната основа на липолизата, нашето разбиране за това как тези процеси са организирани и регулирани в клетките е непълно. Липолизата се извършва на повърхността на вътреклетъчни липидни капчици, които сега са разпознати като добросъвестни органели и е установено, че голям брой протеини променят асоциациите си с липидни капчици в отговор на липолитична стимулация. Вътреклетъчната липолиза има критични пространствени и времеви домейни, които могат да бъдат изследвани с помощта на изображения с висока разделителна способност на фиксирани и живи клетки. Тук описваме техники за изобразяване с висока разделителна способност на естествени липидни капчични протеини, на динамичен трафик и взаимодействие на тези протеини в моделни системи и на вътреклетъчно производство на мастни киселини, използвайки флуоресцентни репортери в живи адипоцити.
Диагностика, класификация, епидемиология и биохимия
Sujoy Ghosh MD (обща медицина) DM (ендокринология) MRCP (Великобритания) MRCPS (Глазгоу), Andrew Collier BSc MD FRCP (Глазгоу и Единбург), в Pocketbook of Diabetes на Чърчил (второ издание), 2012
Липолиза
Липолизата е хидролиза на липиди (фиг. 1.4). Метаболитно е разграждането на триглицеридите до свободни мастни киселини в клетките. Когато мазнините се разграждат за енергия, процесът е известен като β-окисление: кетоните се произвеждат и се намират в големи количества в кетоза (състояние в метаболизма, настъпващо, когато черният дроб превръща мазнините в мастни киселини и кетонни тела, което може да се използва от тялото за енергия). Ленти за тестване на липолиза като Ketostix се използват за разпознаване на кетони в урината.
Следните хормони индуцират липолиза: норадреналин (епинефрин), норадреналин (норепинефрин), глюкагон, растежен хормон и кортизол (въпреки че действията на кортизола все още не са ясни). Те задействат рецептори, свързани с G-протеин, които активират аденилат циклаза. Това води до повишено производство на сАМР, който активира протеин киназа А, която впоследствие активира липази, открити в мастната тъкан.
Триглицеридите се транспортират през кръвта до подходящи тъкани (мастна, мускулна и др.) От липопротеини като хиломикрони. Триглицеридите, присъстващи в хиломикроните, се подлагат на липолиза от клетъчните липази на целевите тъкани, които дават глицерол и свободни мастни киселини. Тогава свободните мастни киселини, освободени в кръвта, са достъпни за клетъчно усвояване. Свободните мастни киселини, които не се поемат веднага от клетките, могат да се свържат с албумин за транспортиране до околните тъкани, които изискват енергия. Серумният албумин е основният носител на свободни мастни киселини в кръвта. Глицеролът също попада в кръвта и се абсорбира от черния дроб или бъбреците, където се превръща в глицерол 3-фосфат от ензима глицерол киназа. Чернодробният глицерол 3-фосфат се превръща най-вече в дихидроксиацетон фосфат (DHAP) и след това глицералдехид 3-фосфат (GA3P), за да се присъедини отново към пътя на гликолизата и глюконеогенезата.
Докато липолизата е триглицеридна хидролиза, процесът, при който триглицеридите се разграждат, естерификацията е процесът, при който се образуват триглицеридите. Естерификацията и липолизата са по същество обрати един на друг.
Хипогликемия
Плазмен β-хидроксибутират (β-OHB)
Липолизата е много чувствителна към циркулиращите концентрации на инсулин. По време на гладуване нормалните индивиди ще показват постепенно намаляване на концентрацията на инсулин и прогресивно увеличаване на липолизата и следователно кетонни тела, например β-OHB (фиг. 17.3). При пациенти с хипогликемия, дължаща се на хиперинсулинемия, липолизата се потиска и концентрациите на β-OHB са ниски. Концентрация на β-OHB в плазмата ≤2,7 mmol/L по време на продължително бързо и когато плазмената концентрация на глюкоза е
СИРЕНА | Производство на твърди и полутвърди сортове сирена
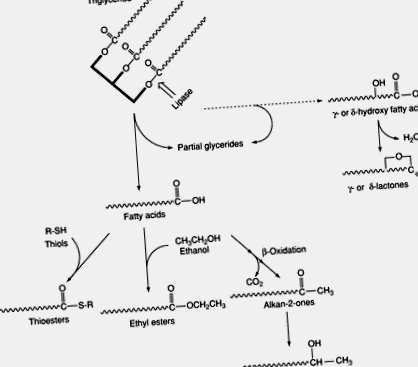
Липолиза
Фигура 3. Общ път за производство и катаболизъм на мастни киселини в сиренето по време на узряването.