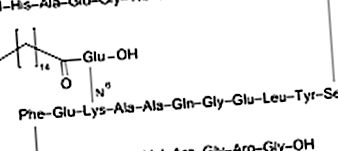Лираглутид е противопоказан при пациенти с лична или фамилна анамнеза за MTC и при пациенти със синдром на множествена ендокринна неоплазия тип 2 (MEN 2).
Свързани термини:
- Глюкагоноподобен пептид-1
- Exendin 4
- Пептид
- Инсулин
- Глюкоза
- Метформин
- Агонист на рецептора на глюкагон като пептид 1
- Захарен диабет
- Неинсулинозависим захарен диабет
Изтеглете като PDF
За тази страница
Захарен диабет - общ преглед
Thundiparambil Azeez Sonia, Chandra P. Sharma, в орална доставка на инсулин, 2014
Лираглутид
Лираглутидът е аналог на човешки GLP-1 веднъж дневно с 97% хомология с човешки GLP [189]. Модификациите на лираглутида, като прикрепване на верига на мастна киселина с глутамоилен дистанционер към лизинов остатък и заместване на аминокиселини, забавят абсорбцията и забавят разграждането на лираглутид чрез DPP-4, удължавайки полуживота до 13 часа [190 ]. Пътят на елиминиране на лираглутид изглежда се обобщава от протеолиза, при която, тъй като нито една органна система не демонстрира значително участие, не е необходима корекция на дозата при пациенти с тежко бъбречно или чернодробно увреждане. Клиничната ефикасност на лираглутид, човешки аналог на GLP-1, при лечението на T2D доведе до одобрението на лираглутид от Европейската агенция по лекарствата през 2009 г. и FDA през 2010 г. [191]. В допълнение към неговите понижаващи глюкозата ефекти, данните от клинични проучвания сега установяват, че лечението с лираглутид води до подобряване на различни рискови фактори, като телесно тегло, кръвно налягане и липидни панели [190, 192].
Международен преглед на клетъчната и молекулярна биология
2.1.1.1.2.1 Лираглутид
Нови терапии при затлъстяване
Лираглутид 3 mg
Лираглутидът е глюкагоноподобен пептид-1 (GLP-1) рецепторен агонист (RA). GLP-1RA съдържат клас пептиди, които свързват и активират рецепторите за ендогенния инкретинов хормон GLP-1. Те усилват секрецията на инсулин и намаляват секрецията на глюкагон по глюкозозависим начин, за да понижат кръвната захар, особено след хранене, и носят незначителен риск от интерпрандиална или гладна хипогликемия. GLP-1RA забавят изпразването на стомаха, което може да причини временно гадене при някои пациенти. Тези агенти също оказват ефекти на ситост, които улесняват загубата на тегло (фиг. 26.1). 13
Лираглутид 0,6, 1,2 или 1,8 mg/ден (Victoza) е лицензиран в Европа през 2009 г. и в САЩ през 2010 г. за лечение на пациенти с диабет тип 2 с наднормено тегло (ИТМ ≥27) с ≥1 коморбидно състояние (напр. Хипертония ) или със затлъстяване (ИТМ ≥30) - т.е. те имат затлъстяване. 14.
За разлика от други средства за затлъстяване, лираглутид 3 mg (Saxenda) се доставя като подкожна инжекция веднъж дневно (доставя се в предварително напълнена писалка, съдържаща 18 mg лираглутид в 3 ml), приложена по всяко време на деня независимо от храната, но се препоръчва редовност на времето . Поради проблеми със стомашно-чревната поносимост (главно гадене), дозирането трябва да започне с 0,6 mg дневно и да се увеличава всяка седмица на стъпки от 0,6 mg до поддържащата доза от 3 mg/ден. Терапията с инкретин трябва да се избягва при пациенти с анамнеза за панкреатит, проблеми с жлъчния мехур и предразполагащи обстоятелства, като алкохолизъм. В проучванията с лираглутид 3 mg фаза III сърдечната честота се е увеличила (2,5 удара/мин), но това е било обърнато при спиране на лечението. В дългосрочните клинични проучвания е имало 6 и 10 големи нежелани сърдечно-съдови събития (MACE) при пациенти, лекувани съответно с лираглутид 3 mg и плацебо. 11.
SCALE е заглавието на изследването, дадено на четирите рандомизирани двойно-слепи плацебо-контролирани проучвания с лираглутид 3 mg, представени за регулаторно одобрение, и те са обобщени в таблица 26.1. Всички пациенти са били с наднормено тегло (ИТМ ≥27 с ≥1 коморбидност) или със затлъстяване (ИТМ ≥30). В проучванията SCALE всички пациенти консумират нискокалорична диета с увеличаване на физическата активност и лираглутидът се повишава до „доза за лечение“ от 3 mg за период от 4 седмици. 14–18
Ефект и действие на лираглутид при диабет: Оценка на резултатите от сърдечно-съдови резултати (LEADER) е проучване за безопасност при 9340 души с диабет тип 2 (HbA1c ≥7%) с висок сърдечно-съдов риск. 19 Над 60% от пациентите са имали ИТМ ≥30, а лечението с лираглутид (средна доза 1,78 mg/ден) за медиана от 3,8 години е довело до по-малко смъртни случаи от каквато и да е причина (8,2% срещу 9,6%, P = .02 ) и сърдечно-съдови причини (4.7% спрямо 6%, P = .007), и нефатален инфаркт на миокарда, нефатален инсулт и хоспитализация за сърдечна недостатъчност са били незначително по-ниски при пациентите на лечение с лираглутид спрямо плацебо. Лираглутид подобрява индексите на повишен сърдечно-съдов риск (напр. Тегло, HbA1c); обаче сърдечната честота се увеличава с 3 удара/минута; ракът на панкреаса е по-висок, отколкото при плацебо (13 срещу 5 пациенти), както и острата жлъчно-каменна болест (145 срещу 90 пациенти), но остър панкреатит се наблюдава само при 18 пациенти в групата на лираглутид в сравнение с 23 в групата на плацебо. Основните нежелани събития са от стомашно-чревен характер. 19 Въпреки че дозата на лираглутид за лечение на затлъстяване (3 mg/ден) е по-висока от диабет (0,6, 1,2 или 1,8 mg/ден), има надежда, че проучването LEADER ще успокои проблемите около употребата на лираглутид при затлъстяване.
Глава за фармакологични агенти за коремно затлъстяване
Лираглутид
Лираглутид е лекарство, което е одобрено за лечение на диабет тип 2 от няколко години и получи индикация за лечение на затлъстяване с по-висока доза от 3 mg под търговското наименование Saxenda през 2014 г. Принадлежи към GLP-1 клас лекарства и се предлага чрез инжектиране веднъж дневно. Лираглутидът е приблизително 97% хомоложен на ендогенния човешки GLP-1 хормон и е известен със своите ефекти върху загубата на тегло в продължение на няколко години, което води до компанията да проучи използването му при лечението на затлъстяване. Смята се, че неговите ефекти върху загубата на тегло се дължат на централната активност в хипоталамуса и други апетитни центрове в мозъка, както и на директните ефекти върху червата, за да забавят изпразването на стомаха и да намалят приема на храна чрез сигнализиране през блуждаещия нерв, причинявайки ситост. 42,43
Има три SCALE проучвания, които са били използвани за получаване на одобрение от FDA на лираглутид за хронично лечение на затлъстяване: SCALE диабет, SCALE поддържане и SCALE затлъстяване и prediabetes. 44–46 Всяко от тези проучвания е проведено в продължение на 56 седмици, като първоначалното седмично титриране е нараснало с 0,6 mg/седмица до пълната доза от 3,0 mg до седмица 5. В тези три проучвания пациентите са загубили средно 6,5% от изходното си тяло маса след 56 седмици, в сравнение със средно 1,6% намаление в плацебо групите. Бенчмарк ≥ 5% загуба на тегло е постигната от приблизително 56% от пациентите, използващи лираглутид, като 28% са постигнали ≥ 10% референтна стойност, в сравнение с 23% и 8%, съответно, при плацебо. По време на клиничните изпитвания 9,8% от пациентите, използващи лираглутид, и 4,3% от пациентите на плацебо се оттеглят поради нежелани събития. 47
Лечение: Нови лекарства
Лираглутид
Еволюцията на лекарствата за понижаване на глюкозата при диабет тип 2
Лираглутид
Лираглутид е GLP-1 миметик, който е устойчив на DPP-4. Лекарството има 97% последователност, идентифицирана с естествения GLP-1, който съдържа модифицирана GLP-1 пептидна последователност, която е прикрепена към палмитоилова верига (Фигура 36.4). 43 Това позволява нековалентно свързване с албумин след подкожно инжектиране. Функцията на островните β-клетки се подобрява с повишено усилване на свързаната с храненето секреция на инсулин. Нивата на глюкагон в кръвта след хранене са намалени, в съответствие с гореспоменатите действия на GLP-1.
ФИГУРА 36.4. Химична структура на лираглутид.
Свързването с албумин забавя бъбречното елиминиране, давайки полуживот на лираглутид приблизително 12 часа. Бавната абсорбция на лираглутид от подкожните тъкани води до максимална концентрация в кръвта след 8–12 часа, като по този начин позволява инжектиране веднъж дневно. Предполага се, че избягването на пиковете на лекарството помага за намаляване на характерните стомашно-чревни странични ефекти.
В Обединеното кралство лираглутидът е одобрен за лечение на възрастни с диабет тип 2 в комбинация с метформин или сулфонилурея, в комбинация с метформин и сулфонилурея или добавен към метформин и тиазолидиндион.
Лираглутид е формулиран като разтвор за подкожно инжектиране в предварително напълнени писалки, доставящи 0,6, 1,2 или 1,8 mg на доза. Препоръчителната начална доза е 0,6 mg дневно, като се увеличава след не по-малко от седмица до поддържащата доза от 1,2 mg дневно. След поне още една седмица дозата може да бъде увеличена до 1,8 mg, ако е необходимо, въпреки че тази доза не се препоръчва от Националния институт за здраве и клинични постижения в Обединеното кралство (NICE). 42 Агенцията също така е посочила критерии, които трябва да подтикнат отказ от терапия въз основа на комбинация от намаляване на теглото и гликемични ефекти; тези ограничения важат и за екзенатид във Великобритания. Ако се наблюдава неадекватен отговор след 6-месечно лечение, трябва да се обмислят алтернативни лекарства за понижаване на глюкозата. Употребата на лираглутид не се препоръчва при пациенти с умерена степен на бъбречно увреждане, т.е. където креатининовият клирънс е 30–60 ml/min. Лираглутид не е проучван при пациенти с тежко увредена бъбречна функция и данните при пациенти с чернодробно увреждане са ограничени.
При пациенти с диабет тип 2 лираглутид може значително да понижи HbA1c със съпътстващи подобрения в нивата на кръвната захар на гладно и след хранене. Телесното тегло се намалява в зависимост от дозата с приблизително 1–3 kg. Основните нежелани събития са гадене и диария, въпреки че честотата на стомашно-чревните странични ефекти често намалява с течение на времето. Наблюдавани са също понижаване на триглицеридите и намаляване на кръвното налягане.
В предклинични проучвания се наблюдават С-клетъчни тумори на щитовидната жлеза при модели на гризачи. При клинична употреба при ≤ 1% от пациентите, лекувани с лираглутид, са наблюдавани повишени нива на клинични нежелани събития, свързани с щитовидната жлеза, включително новообразувания, повишени нива на калцитонин в кръвта и гуша. Съобщава се за образуване на антитела в
ЦНС, болка, метаболитен синдром, сърдечно-съдови, тъканна фиброза и уринарна инконтиненция
7.12.6.4 Лираглутид
Лираглутид е структурно подобен на естествения GLP-1 (7–37) с 97% идентични аминокиселинни остатъци с естествения хормон ( Фиг. 6 ). Той се различава в позиция 28 с Arg вместо Lys и в допълнение палмитиновата киселина се конюгира чрез дистанционер на глутамат при Lys в позиция 20. Това конюгиране на мастните киселини осигурява удължената продължителност на действие, улеснено от свързването със серумния албумин, както и само асоциацията в подкожната пространство. Освен това, стягащото албумин свързващо действие предпазва лираглутидната последователност от DPP-4 и NEP ензимно разграждане. Средният плазмен полуживот при хората е 11–13 часа. Веднъж дневно дозата от 1,2 mg при хора осигурява добър гликемичен контрол и с увеличаване на дозите до 1,8 mg показва значителни подобрения в намаляването на HbA1c в сравнение с екзенатид (1,1% срещу 0,79%). По-нататъшното увеличаване на дозата до 3 mg лираглутид дава ∼ 6% намаление на теглото при диабетици с наднормено тегло тип 2 в сравнение с плацебо.
Фиг. 6. Последователност и структура на лираглутид.
Интегративен подход към затлъстяването
Д-р Джеймс П. Николай,. Andrew J. Wolf MEd, по интегративна медицина (четвърто издание), 2018
Лираглутид
Лираглутидът е глюкагоноподобен пептид-1 (GLP-1) хормон, който се секретира след хранене. Тъй като се освобождава чрез ядене на храна, GLP-1 увеличава инсулина, за да съхранява енергия, намалява глюкагона, за да спре производството на глюкоза от черния дроб и забавя изпразването на стомаха. Имитирането на ефектите на този хормон с агонисти на GLP-1 понижава глюкозата и може да доведе до загуба на тегло, като кара хората да се чувстват сити и по-малко гладни. Лираглутид не повлиява метаболитните енергийни разходи. Лираглутид е едно от малкото лекарства за диабет, които също са одобрени за лечение на затлъстяване.
Дозировка
Съобщава се, че количеството на загуба на тегло и тежестта на страничните ефекти зависят от дозата, като по-големи количества са и двете при дозирането от 3,0 mg. Въпреки това, няма значителна разлика в промените на HbA1 C между дозирането от 3,0 mg и 1,8 mg (разлика от 0,19%). Съответно, ако лираглутид се използва главно за контрол на диабета, дозирането на 1,8 mg вероятно ще постигне сладкото място с най-малко странични ефекти с най-голямо намаляване на HbA 1C. Ако обаче се използва за постигане на най-голяма загуба на тегло, титрирането до 3,0 mg е по-вероятно да постигне тази цел. Започнете с 0,6 mg подкожно дневно и увеличавайте с 0,6 mg всяка седмица, докато постигнете желаната доза, която би била 3 седмици за постигане на 1,8 mg и 5 седмици за постигане на 3,0 mg.
Предпазни мерки
Както може да се очаква чрез неговия механизъм на действие, стомашно-чревната непоносимост е основната грижа за лираглутид. Най-честият симптом, гаденето, зависи от дозата, което може да обясни как влияе върху загубата на тегло. Другите най-чести нежелани реакции са повръщане, диспепсия, диария, запек и коремна болка. В проучване с 846 субекти, следващи в продължение на 56 седмици, не е имало случаи на панкреатит; обаче повишенията на серумните нива на амилаза и липаза са често срещани и отзвучават с прекратяване на лечението. 77 Налице е обратно повишаване на теглото, когато лекарството е спряно в горното проучване и дългосрочните странични ефекти от лечението не са оценени. При проучвания с животни е установено, че лираглутидът увеличава риска от рак на щитовидната жлеза и съществува опасение относно повишения риск от рак на дебелото черво. Необходими са по-дълги проучвания, за да се установи безопасността на лираглутид при хронична употреба.
Захарен диабет
Дерек Г. Уолър, бакалавър (HONS), DM, MBBS (HONS), FRCP, Антъни П. Сампсън, доктор по медицина, FHEA, FBPhS, по медицинска фармакология и терапия (Пето издание), 2018 г.
- Високо приемане на натрий - общ преглед на ScienceDirect теми
- Диета с високо съдържание на фруктоза - общ преглед на темите на ScienceDirect
- Възпалително заболяване на червата - общ преглед на ScienceDirect теми
- Лимфоидна хиперплазия - общ преглед на ScienceDirect теми
- Mallory Body - общ преглед на ScienceDirect теми