Джи-Хюн Юн
1 Hurum Central Research Institute Co., Ltd., Seogwipo, 63608 Република Корея
Парк Сунг-Хван
1 Hurum Central Research Institute Co., Ltd., Seogwipo, 63608 Република Корея
Goo-Hee Choi
1 Hurum Central Research Institute Co., Ltd., Seogwipo, 63608 Република Корея
In-Jae Park
1 Hurum Central Research Institute Co., Ltd., Seogwipo, 63608 Република Корея
Джин-Ха Ли
2 Департамент по хранителни науки и биотехнологии, Национален университет Kangwon, Chuncheon, 24341 Република Корея
Ок-Хван Лий
2 Департамент по хранителни науки и биотехнологии, Национален университет Kangwon, Chuncheon, 24341 Република Корея
Юнг-Хьон Ким
3 Департамент по кулинарни изкуства, Университет по туризъм в Чеджу, Чеджу, 63063 Република Корея
Юн-Хи Со
4 EBO Co., Ltd., Cheongju, 28116 Република Корея
Джу-Хюн Чо
1 Hurum Central Research Institute Co., Ltd., Seogwipo, 63608 Република Корея
Резюме
Целта на това проучване беше да се определи антидиабетният ефект на екстракт от хранителен Brassica napus, съдържащ ванадий (BECV). BECV се приготвя след отглеждане на B. napus с воден ванадиев концентрат Jeju за 7 дни. BECV се прилага на db/db мишки в продължение на 8 седмици в различни дози (0,028, 0,14 и 0,7 μg/kg; като концентрация на ванадий в BECV). След 8 седмици резултатите от BECV показват, че концентрациите на глюкоза в мишката значително намаляват, в зависимост от дозата, в сравнение с резултатите за контролни мишки. В допълнение, концентрациите на триглицериди, общ холестерол и гликиран хемоглобин са значително по-ниски след 8 седмици на приложение от 0,7 μg/kg BECV. Следователно BECV може да има защитни ефекти срещу диабет тип 2.
Въведение
Трябва обаче да се извършат повече изследвания, за да се изясни точният механизъм на действие на лечебните растения с антидиабетни ефекти. Обикновено се смята, че растителните лекарствени продукти са безопасни, но много растителни материали са опасни за хората; по този начин трябва да се предприемат изследвания на токсичността на такива растения, преди да се предположи консумация на някои растителни материали или продукти.
Въпреки впечатляващата им антидиабетна активност, ванадиевите съединения са свързани с няколко токсични ефекти (Domingo et al., 1995). Най-честите токсични ефекти са диария, намалено усвояване на течности и храна, дехидратация и намалено наддаване на телесно тегло, което обаче може да бъде коригирано чрез добавяне на NaCl към питейната вода, регулиране на рН на разтвора до неутралност и чрез постепенно увеличаване на доза ванадий (Bendayan and Gingras, 1989; Bollen et al., 1990; Ramanadham et al., 1989; Sakurai et al., 1990; Sekar et al., 1989; Strout et al., 1990). Сравнително проучване показа, че органичните ванадиеви съединения са много по-безопасни като антидиабетни средства, отколкото неорганичните ванадиеви соли (Reul et al., 1999). В тези експерименти диабетичните плъхове, получаващи органични съединения, не показват стомашно-чревни странични ефекти и не развиват диария.
Остров Чеджу, най-големият остров в Корея, е вулканичен остров, разположен на около 140 км южно от Корейския полуостров. Напоследък се съобщава, че водата Jeju, съдържаща ванадий, има благоприятни ефекти при лечението на диабет чрез активиране на АМР-активирана протеин киназа (Hwang и Chang, 2012) и инхибира диференциацията на преадипоцитите и адипогенезата при модели на животни със затлъстяване (Park et al., 2013 ).
За настоящото изследване, B. napus е подхранван с ванадий-съдържаща вода Jeju. По време на този процес, B. napus биоакумулира ванадий от водно-ванадиевия концентрат на Jeju. Настоящото проучване се фокусира върху антидиабетните ефекти на BEVC, за да оцени потенциала му като функционален източник на хранителни съставки.
Материали и методи
Екстракция на B. napus, съдържащ ванадий
Животински модел и експериментални групи
Преди тестване на антидиабетния ефект, 6-седмични db/db мъжки мишки, закупени от DH Biolink (Chungbuk, Корея), бяха аклиматизирани за 1 седмица. Всички експериментални протоколи са одобрени от Институционалния комитет по грижа и употреба на животните от Националния университет Чунгбук (CBNUA-306-11-02). Три мишки на клетка бяха настанени при контролирани условия на околната среда (22 ± 3 ° C, 50 ± 10% относителна влажност, 200–300 Lux). Db/db мишките бяха разделени на пет групи (n = 6 във всяка група). На контролната група се прилага дестилирана вода, на положителната контролна група - метформин (30 mg/kg телесно тегло), а на трите експериментални групи се прилага BEVC, съдържащ различни концентрации на ванадий. Всички прилагания се извършват ежедневно чрез орален сондаж. Концентрациите на ванадий в трите групи, прилагани от BECV, са 0,028, 0,14 и 0,7 μg/kg телесно тегло на мишка. Телесното тегло, приема на храна и приема на вода на мишките се проверяват ежеседмично. Нивата на глюкоза в кръвта на мишките се проверяват на всеки 2 седмици през 8-седмичния период на изследване. Нивата на гликиран хемоглобин (HbA1c) бяха измерени след края на 8-седмичния период на изследване.
Тест за интраперитонеален глюкозен толеранс
Db/db мишките са гладували 12 часа преди началото на експеримента с толерантност и BECV (0,028, 0,14 или 0,7 μg/kg; като концентрация на ванадий в BECV) се прилага интраперитонеално 30 минути преди предизвикване на глюкоза. Глюкозата (2 g/kg) се прилага интраперитонеално след 0 минути и нивата на кръвната глюкоза се измерват на 0, 30, 60, 90, 120 и 180 минути след прилагане на глюкоза.
Нива на кръвната глюкоза и гликирания хемоглобин (HbA1c)
На всеки 2 седмици по време на 8-седмичния експеримент се измерват нивата на глюкоза в кръвта, след като животните са гладували в продължение на 3 часа. Нивата на кръвната глюкоза се определят в кръвни проби, получени от опашната вена, с помощта на глюкомер Accu-Chek Performa (Roche, Mannheim, Германия).
Използвайки кръвни проби, събрани от db/db мишки в края на 8-седмичния период на изследване, процентните нива на HbA1c бяха определени с помощта на анализатор на HbA1c (EasyA1c, Infopia, Anyang, Корея).
Биохимично изследване на кръвта
Използвани са серумни проби за определяне на нивата на общия холестерол (TC), триглицеридите и липопротеините с висока плътност (HDL) на холестерол чрез прилагане на ензимни методи и автоматичен анализатор (Hitachi 7080 Clinical Analyzer, Hitachi, Токио, Япония).
Статистически анализ
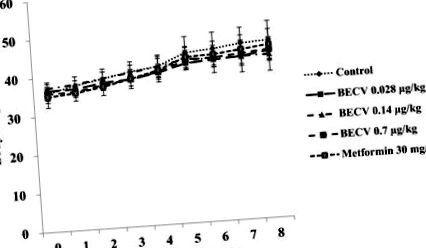
Всички данни бяха анализирани със статистически софтуер SPSS 12.0 (SPSS, Чикаго, IL, САЩ). Данните са изразени като средни стойности ± стандартно отклонение. Статистическите разлики бяха изследвани независимо чрез прилагане на t-тест на Student и корелационен тест на Pearson. Стойност p 1). Телесното тегло на всички мишки нараства подобно по време на 8-седмичния период на изследване. Значителни разлики в приема на храна и приема на вода от трите експериментални групи (групи, лекувани с BECV), положителната контролна група (група, третирана с метформин) и контролната група изглеждаха невидими (данните не са показани).
Седмични промени в телесното тегло на db/db мишки, прилагани перорално BECV, метформин или вода (контрол). Точките за данни показват средна стойност ± SD (n = 6 във всяка група)
Ефекти на BECV върху глюкозния толеранс
Изследван е интраперитонеален глюкозен толеранс, за да се определи ефектът от еднократна перорална доза BECV върху глюкозния толеранс при db/db мишки (Таблица 1). Глюкозното предизвикателство драстично повишава нивата на кръвната глюкоза при мишките от контролната група, докато лечението с метформин в положителната контролна група значително предотвратява покачването на нивата на кръвната глюкоза, особено 30 минути след натоварването с глюкоза. Промените в нивата на кръвната глюкоза при трите групи, лекувани с BECV, не се различават от тези в контролната група.
маса 1
Резултати от теста за глюкозен толеранс при db/db мишки, прилагани BECV, метформин или вода (контрол)
| Контрол a | 322 ± 37 | 583 ± 22 | 600 ± 0 | 600 ± 0 | 600 ± 0 | 600 ± 0 |
| Метформин 30 mg/kg | 260 ± 57 | 472 ± 58 ** | 581 ± 24 * | 529 ± 18 ** | 468 ± 35 ** | 395 ± 52 ** |
| BECV 0,028 μg/kg | 322 ± 29 | 570 ± 45 | 600 ± 0 | 600 ± 0 | 600 ± 0 | 600 ± 0 |
| BECV 0,14 μg/kg | 303 ± 27 | 580 ± 18 | 600 ± 0 | 600 ± 0 | 600 ± 0 | 594 ± 8 |
| BECV 0,7 μg/kg | 322 ± 29 | 570 ± 45 | 600 ± 0 | 600 ± 0 | 600 ± 0 | 567 ± 27 |
Данните са изразени като средната стойност ± SD (n = 6)
BECV: Екстракт от хранителен Brassica napus, съдържащ ванадий
a Отрицателен контрол: без екстракт; третирани с асептична вода
* p 2). За разлика от това, нивото на кръвната глюкоза в групата, лекувана с BECV от 0,7 μg/kg, е подобно на тази при групата с положителен контрол (473 ± 70 срещу 430 ± 16 mg/L).
Таблица 2
Двуседмично ниво на глюкоза в кръвта при db/db мишки, прилагани с BECV, метформин или вода (контрол)
| Контрол a | 323 ± 57 | 365 ± 48 | 419 ± 11 | 486 ± 34 | 600 ± 0 |
| Метформин 30 mg/kg | 350 ± 82 | 361 ± 47 | 365 ± 54 | 372 ± 29 ** | 430 ± 16 ** |
| BECV 0,028 μg/kg | 303 ± 18 | 369 ± 44 | 400 ± 39 | 480 ± 34 | 542 ± 38 |
| BECV 0,14 μg/kg | 313 ± 12 | 372 ± 42 | 424 ± 79 | 455 ± 65 | 487 ± 44 ** |
| BECV 0,7 μg/kg | 320 ± 10 | 318 ± 79 | 377 ± 38 | 408 ± 56 | 473 ± 70 ** |
Данните са изразени като средната стойност ± SD (n = 6)
BECV: Екстракт от хранителен Brassica napus, съдържащ ванадий
a Отрицателен контрол: без екстракт; третирани с асептична вода
** p 2). Също така, нивата на HbA1c в групата, лекувана с BECV от 0,7 μg/kg, е подобна на тази в групата с положителна контрола (8,40 ± 0,36% срещу 8,36 ± 0,38%).
Нива на гликиран хемоглобин (HbA1c) при db/db мишки, прилагани с BECV, метформин или вода (контрол) в края на 8-седмичния период на лечение. Точките с данни показват средната стойност ± SD (n = 6 във всяка група). ** стр. 3). Серумната концентрация на триглицериди в групата, лекувана с BECV с 0.7 μg/kg, е по-ниска от тази в контролната група (106.5 ± 14.3 срещу 161.1 ± 29.8 mg/L). В допълнение, нивата на TC и на трите групи, лекувани с BECV (0,028, 0,14 и 0,7 μg/kg групи), са значително по-ниски от тези на контролната група (172,3 ± 7,5, 174,6 ± 8,7 и 177,1 ± 4,9 спрямо 206,1 ± 15,3 mg/L, съответно). Въпреки това, разликите в нивата на HDL холестерол при третирани с BECV мишки не се различават значително от тези в контролната група.
Таблица 3
Нива на серумни липиди при db/db мишки, прилагани с BECV, метформин или вода (контрол) в края на 8-седмичния период на лечение
| Контрол a | 206,1 ± 15,3 | 161,1 ± 29,8 | 109,4 ± 8,6 |
| Метформин 30 mg/kg | 149,1 ± 35,6 ** | 94,0 ± 14,3 ** | 100,0 ± 11,7 |
| BECV 0,028 μg/kg | 172,3 ± 7,5 ** | 153,1 ± 19,9 | 108,0 ± 4,6 |
| BECV 0,14 μg/kg | 174,6 ± 8,7 ** | 146,7 ± 27,7 | 107,9 ± 5,9 |
| BECV 0,7 μg/kg | 177,1 ± 4,9 * | 106,5 ± 14,3 ** | 104,4 ± 7,9 |
Данните са изразени като средната стойност ± SD (n = 6)
BECV: Екстракт от хранителен Brassica napus, съдържащ ванадий
a Отрицателен контрол: без екстракт; третирани с асептична вода