Източник: Център за диабет Joslin
Учени от центъра за диабет в Джослин казват, че са разработили доказателство за концепция за нова клетъчна терапия срещу затлъстяване. Потенциалната терапия за затлъстяване би трансплантирала HUMBLE (човешки кафяви) мастни клетки, човешки бели мастни клетки, които са генетично модифицирани, за да станат подобни на генериращите топлина кафяви мастни клетки, каза д-р Ю-Хуа Ценг, старши изследовател в Joslin's Секция за интегративна физиология и метаболизъм.
Кафявите мастни клетки изгарят енергия, вместо да съхраняват енергия, както правят белите мастни клетки, отбелязва Ценг, старши автор на статията, „Проектираните от CRISPR човешки кафяви адипоцити предотвратяват затлъстяването, предизвикано от диетата, и подобряват метаболитния синдром при мишки“, публикувано наскоро в науката Транслационна медицина. В този процес кафявите мазнини могат да понижат прекомерните нива на глюкоза и липиди в кръвта, които са свързани с метаболитни заболявания като диабет.
Въпреки това хората с наднормено тегло или затлъстяване са склонни да имат по-малко от тази полезна кафява мазнина - бариера, която HUMBLE клетките са предназначени да преодолеят, според Tseng.
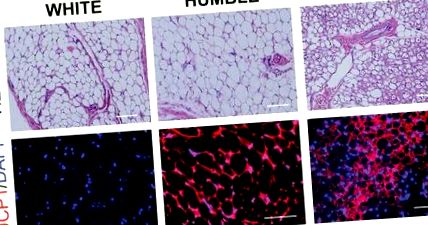
Тя и нейните колеги са създали клетките от човешки бели мастни клетки в стадия на предшественика. Изследователите са използвали вариант на системата за редактиране на генома CRISPR-Cas9, за да засилят експресията на ген, наречен UCP1, който задейства предшествениците на белите мастни клетки да се развият в клетки, подобни на кафяви мазнини.
Трансплантирани в мишки без имунна система, предшествениците HUMBLE се развиха в клетки, които функционираха много подобно на собствените кафяви мастни клетки на мишките, продължи Ценг, който е и професор по медицина в Харвардското медицинско училище.
Нейният екип сравнява трансплантациите на тези клетки с оригиналните бели мастни клетки при мишки, които са били на диета с високо съдържание на мазнини. Мишките, получили трансплантациите HUMBLE, показват много по-голяма чувствителност към инсулин и способност да изчистват глюкозата от кръвта (два ключови фактора, които са нарушени при диабет тип 2).
Освен това, мишките, получаващи HUMBLE трансплантации, са с по-малко тегло от мишки с трансплантирани бели мастни клетки, оставайки в същия диапазон като животните, които са получили кафяви мастни клетки.
Може би изненадващо, учените от Джослин демонстрират, че тези ползи се дължат най-вече на сигнали от трансплантираните клетки към ендогенни кафяви мастни клетки в мишките.
„Кафявите и подобни на кафяво бежово/преливащи адипоцити разсейват енергията и са предложени като терапевтични цели за борба с метаболитните нарушения. Терапевтичните ефекти на клетъчната терапия при хора обаче остават неясни. Тук създадохме човешки кафяви (HUMBLE) клетки чрез инжектиране на човешки бели преадипоцити, използвайки CRISPR-Cas9 – SAM – gRNA, за да активираме ендогенна експресия на разединяващ протеин 1. Затлъстелите мишки, които са получили HUMBLE клетъчни трансплантации, показват трайно подобрение на глюкозния толеранс и чувствителността към инсулин, както и увеличен разход на енергия “, пишат изследователите.
„Механично, повишеният метаболизъм на аргинин/азотен оксид (NO) в HUMBLE адипоцитите насърчава производството на NO, който се пренася от S-нитрозотиоли и нитрити в червените кръвни клетки, за да активира ендогенната кафява мазнина и подобрява хомеостазата на глюкозата при животни реципиенти. Заедно тези данни демонстрират ползата от използването на технологията CRISPR-Cas9 за проектиране на човешки бели адипоцити за показване на кафяви мастноподобни фенотипове и могат да разкрият клетъчно базирани терапевтични възможности за борба със затлъстяването и диабета. "
„Клетките в различни тъкани комуникират помежду си“, обясни Ценг. „В този случай открихме, че нашите трансплантирани HUMBLE клетки секретират молекула, наречена азотен оксид, която се пренася от червените кръвни клетки до ендогенните кафяви клетки и активира тези клетки.“
Ако техниката HUMBLE продължи да се доказва в предклиничните изследвания, евентуално може да бъде възможно да се генерира този тип клетки за отделни пациенти, предположи Tseng. Такава процедура би премахнала малко количество от белите мастни клетки на пациента, изолирала предшествените клетки, модифицирала тези клетки, за да подсили експресията на UCP1 и след това да върне получените HUMBLE клетки на пациента.
Този индивидуализиран подход обаче би бил сложен и скъп, така че лабораторията Tseng следва два алтернативни пътя, които могат да бъдат по-практични за клинична употреба.
Единият е да се използват клетки, които не са персонализирани, а вместо това са капсулирани чрез биоматериали, които предпазват клетките от отхвърляне от имунната система на пациента. (Изследователите на Joslin и техните сътрудници отдавна са изучавали такива материали за клетъчни трансплантации при диабет тип 1.) Другият вариант са генните терапии, които директно експресират гена UCP1 в белите мастни прогениторни клетки в тялото, така че тези клетки да придобият HUMBLE-подобни свойства.
Ценг подчерта, че това изследване върви напред въпреки пандемията Covid-19, която поставя хората с диабет в много по-висок риск от сериозни резултати, ако са заразени.
„Използването на клетъчни или генни терапии за лечение на затлъстяване или диабет тип 2 преди беше научна фантастика“, каза тя. „Сега научният напредък, като CRISPR технологиите за редактиране на гени, ще ни помогне да подобрим метаболизма, телесното тегло, качеството на живот и цялостното здраве на хората със затлъстяване и диабет.“
- Ролята на свободното ежедневно ходене при увеличаване на телесното тегло и затлъстяване при диабет
- Какво ни казват дебелите животни за човешкото затлъстяване
- Разкриване на генетиката на човешкото затлъстяване
- Насочването към един ензим може да лекува рак, диабет и затлъстяване
- Използване на конструкции за културна компетентност за разбиране на хранителните практики и осигуряване на грижи за диабета и
