Този сайт е предназначен за медицински специалисти в САЩ.
Този сайт е предназначен за медицински специалисти в САЩ.
- Преглед на заболяванията
- MDS
- Какво е MDS?
- Пръстен Sideroblasts
- IPSS-R
- Неефективна еритропоеза
- β-таласемия
- Епидемиология
- Неефективна еритропоеза
- MDS
- MOA
- Ефикасност
- MDS-RS
- МЕДАЛИСТ Пробен дизайн
- Базови характеристики
- Резултати за ефикасност
- β-таласемия
- ВЯРВАЙТЕ Пробен дизайн
- Базови характеристики
- Резултати за ефикасност
- MDS-RS
- Безопасност
- MDS-RS
- Предупреждения и предпазни мерки
- Нежелани реакции и профил на безопасност
- β-таласемия
- Предупреждения и предпазни мерки
- Нежелани реакции и профил на безопасност
- MDS-RS
- Дозиране и администриране
- MDS-RS
- Дозиране
- Прекратяване и модификация на дозата
- Администрация
- β-таласемия
- Дозиране
- Прекратяване и модификация на дозата
- Администрация
- Възстановяване
- Съхранение
- MDS-RS
- Достъп и поддръжка
- Celgene Patient Support ®
- Достъп и възстановяване
- Ресурси
- β-таласемия
- Ресурси
- Видеоклипове
- Ресурси за пациенти и болногледачи
- MDS-RS
- Ресурси
- Видеоклипове
- Ресурси за пациенти и болногледачи
- β-таласемия
- Преглед на заболяванията
- MDS
- Какво е MDS?
- Пръстен Sideroblasts
- IPSS-R
- Неефективна еритропоеза
- β-таласемия
- Епидемиология
- Неефективна еритропоеза
- MDS
- MOA
- Ефикасност
- MDS-RS
- МЕДАЛИСТ Пробен дизайн
- Базови характеристики
- Резултати за ефикасност
- β-таласемия
- ВЯРВАЙТЕ Пробен дизайн
- Базови характеристики
- Резултати за ефикасност
- MDS-RS
- Безопасност
- MDS-RS
- Предупреждения и предпазни мерки
- Нежелани реакции и профил на безопасност
- β-таласемия
- Предупреждения и предпазни мерки
- Нежелани реакции и профил на безопасност
- MDS-RS
- Дозиране и администриране
- MDS-RS
- Дозиране
- Прекратяване и модифициране на дозата
- Администрация
- β-таласемия
- Дозиране
- Прекратяване и модификация на дозата
- Администрация
- Възстановяване
- Съхранение
- MDS-RS
- Достъп и поддръжка
- Celgene Patient Support ®
- Достъп и възстановяване
- Ресурси
- β-таласемия
- Ресурси
- Видеоклипове
- Ресурси за пациенти и болногледачи
- MDS-RS
- Ресурси
- Видеоклипове
- Ресурси за пациенти и болногледачи
- β-таласемия
Миелодиспластичните синдроми (MDS) са хетерогенна група от миелоидни злокачествени заболявания, характеризиращи се с многоредови цитопении, включително анемия 1
Световната здравна организация (СЗО) класифицира MDS като неопластичен и следователно рак 2
- MDS се характеризират с:
- Дисфункция на костния мозък 2,3
- Дисплазия 2,3
- Геномна нестабилност 2
- Цитопении в периферната кръв 2,3
- Неефективна хемопоеза 3
Анемията е налице при повечето пациенти с MDS 1
- При диагностицирането анемията е най-честата цитопения, налична при пациенти с MDS 1 *
- 94% от пациентите с MDS са получили трансфузия на червените кръвни клетки в регистъра SEER-Sound на 783 пациенти от 2001 до 2007 г. 4
- 13% от всички пациенти с MDS, изискващи трансфузия на червените кръвни клетки, са имали пръстенни сидеробласти 4
* Определено в анализ на база данни на 7012 пациенти с нелекуван MDS от 11 държави за проекта на Международната работна група за прогноза на MDS (IWG-PM). 1
Въз основа на Насоките за клинична практика на NCCN в онкологията (NCCN Guidelines ®), подходите за управление на MDS се различават в зависимост от подвида на MDS и тежестта на заболяването 5
IPSS-R, Ревизирана международна прогностична система за точкуване.
* Разпределението на рисковите оценки по IPSS-R по време на диагнозата е оценено в наскоро диагностицираната кохорта от пациенти; (N = 7012) за популацията пациенти, включена в анализа на IPSS-R.
Наличието на пръстенни сидеробласти при пациенти с MDS е свързано с MDS с по-нисък риск
Световната здравна организация (СЗО) разпознава два подтипа MDS с пръстеновидни сидроблати (MDS-RS)
- MDS-RS и еднопосочна дисплазия
- MDS-RS и многоредова дисплазия
- Пръстенните сидеробласти могат да бъдат идентифицирани чрез аспират на костния мозък с желязо, оценено от патолог
- Сидеробластите присъстват при до 45% от пациентите с MDS
- Известна е вариабилност при докладването на костния мозък
Насоките на NCCN за MDS препоръчват luspatercept-aamt (REBLOZYL) за лечение на симптоматична анемия при много нисък до среден риск от MDS с пръстенни сидеробласти (Категория 2А):
- След 3 месеца без отговор на ESA при пациенти със серумен EPO
- Като първоначално лечение за пациенти със серумен EPO> 500 U/L
Пациентите с MDS могат също да имат пръстенни сидеробласти 6
Пръстенните сидеробласти са част от класификацията на СЗО 2016
- СЗО 2016 разпознава 2 подтипа MDS, специфични за пръстеновидните сидеробласти 7:
- MDS-RS с дисплазия с една линия (MDS-RS-SLD)
- MDS-RS с многолинейна дисплазия (MDS-RS-MLD)
- Подтипът MDS-RS се идентифицира със 7:
- ≥15% пръстенни сидеробласти в костния мозък
- ≥5% пръстенни сидеробласти в костния мозък и наличие на мутация SF3B1 (идентифицирана чрез молекулярно тестване)
- MDS-RS е разпознат като част от системата за кодиране ICD-10-CM 8
- Пръстеновидните сидеробласти могат също да присъстват на всяко ниво в други подтипове на MDS 9
- MDS/MPN-RS-T е рядък подтип, признат от СЗО 2016. Той има прилики с MDS-RS, но се характеризира със специфични клинични характеристики 7,10
- Те включват анемия, дисплазия на костния мозък с пръстенни сидеробласти и персистираща тромбоцитоза ≥450 x 10 9/L с пролиферация на големи и морфологично нетипични мегакариоцити 7
ICD-10-CM, Международна класификация на болестите, Десета ревизия, Клинична модификация.
Пръстеновидните сидеробласти са еритробласти с натоварени с желязо митохондрии, свързани с анемия 9
Само с илюстративна цел.
- Пръстеновидните сидеробласти се идентифицират чрез оцветяване с желязо и резултатите могат да бъдат намерени в докладите за патологията 9
- Налице е променливост в начина, по който патолозите описват присъствието на пръстенни сидеробласти в докладите за патологията 11
Консултирайте се с вашия патолог за това как се отчитат пръстенни сидеробласти при вашите пациенти с MDS
Категоризацията IPSS-R е предпочитаната * прогностична система на NCCN Guidelines ® 5
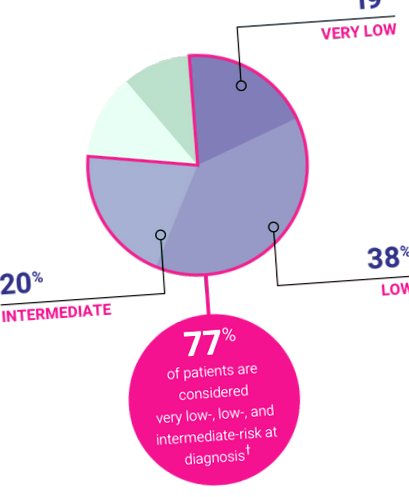
По-голямата част от пациентите с MDS имат IPSS-R с много нисък до среден риск при диагностициране 1
Разпределение на пациентите с MDS по IPSS-R рисков статус (N = 7012) †
* Насоките на NCCN за MDS също така отбелязват, че другите системи за стратификация страдат добре. 5
† Разпределение на оценките на риска IPSS-R по време на диагностицирането, оценено в наскоро диагностицираната кохорта от пациенти; (N = 7012) за популацията пациенти, включена в анализа на IPSS-R. 1
IPSS-R, Ревизирана международна прогностична система за точкуване.
IPSS-R се основава на цитогенетика на костния мозък, процент на взрив на мозъка и наличие и дълбочина на цитопениите 1
| Прогностични стойности на оценките 1 | ||||||||
| Прогностична променлива | BM взривове,% | Цитогенетика | Hgb, g/dL | Тромбоцити, х 10 9 клетки/л | ANC, x 10 9 клетки/L | |||
| 0 | ≤2 | Много добре | ≥10 | ≥100 | ≥0,8 | |||
| 0,5 | - | - | - | 50 до 2 до 10 | Бедно | - | - | - |
| 4 | - | Много беден | - | - | - | |||
ANC, абсолютен брой неутрофили; BM, костен мозък; Hgb, хемоглобин.
Резултатът от IPSS-R се изчислява чрез добавяне на стойностите за прогностичните фактори заедно
Пример за IPSS-R нискорисков резултат:
- 2% брой взривове = 0
- Добра цитогенетика = 1
- 8 g/dL Hgb = 1
- Тромбоцити 75 х 10 9 клетки/L = 0,5
- ANC 0,9 x 109 клетки/L = 0
Общо добавени стойности = 2,5
При диагностициране> 90% от пациентите с MDS имат анемия (
Анемията е свързана с лоша прогноза при МДС
- Пациентите, които получават по-малко от 2 единици кръв на месец, показват значително намалена преживяемост в сравнение с тези, които не се нуждаят от трансфузия
- По-ниските нива на хемоглобин (Hgb) при пациенти с MDS са свързани с намалена преживяемост и по-лоши сърдечно-съдови резултати
Необходимо е да се помогне за справяне с анемията поради неефективна еритропоеза при пациенти с MDS, изискващи трансфузия на червените кръвни клетки
Неефективната еритропоеза е основната причина за анемия при MDS 12
Анемията при MDS е свързана с дисфункция на костния мозък, характеризираща се като неефективна еритропоеза 13
- При MDS стволовите клетки нямат способността за диференциация и съзряване, което води до дисфункция на костния мозък и лошо производство на кръвни клетки, по-специално червените кръвни клетки
Неефективната еритропоеза при MDS може да доведе до анемия, изискваща трансфузия на червените кръвни клетки и се характеризира с 12,14:
Повишена пролиферация на еритроидни предшественици
Повишена смърт на еритроидни предшественици
Нарушено съзряване на еритроидите
Наличието на анемия въпреки увеличената пролиферация на прогениторни клетки е показателно за неефективна еритропоеза при MDS
Необходимо е да се помогне за справяне с анемията поради неефективна еритропоеза при пациенти с MDS, изискващи трансфузия на червените кръвни клетки
Индикация
REBLOZYL е показан за лечение на анемия при възрастни пациенти с бета таласемия, които се нуждаят от редовно преливане на червени кръвни клетки (RBC).
REBLOZYL е показан за лечение на анемия, която не успява да стимулира еритропоезата и изисква 2 или повече единици червени кръвни клетки за 8 седмици при възрастни пациенти с миелодиспластични синдроми с много нисък до среден риск с пръстенни сидеробласти (MDS-RS) или с миелодиспластика/миелопролиферативна неоплазма с пръстенни сидеробласти и тромбоцитоза (MDS/MPN-RS-T).
REBLOZYL не е показан за употреба като заместител на трансфузиите на червените кръвни клетки при пациенти, които се нуждаят от незабавна корекция на анемията.
ВАЖНА ИНФОРМАЦИЯ ЗА БЕЗОПАСНОСТ
ПРЕДУПРЕЖДЕНИЯ И ПРЕДПАЗНИ МЕРКИ
Тромбоза/тромбоемболия
При възрастни пациенти с бета таласемия се съобщава за тромбоемболични събития (TEE) при 8/223 (3,6%) пациенти, лекувани с REBLOZYL. TEEs включват дълбока венозна тромбоза, белодробна емболия, тромбоза на порталната вена и исхемичен инсулт. Пациентите с известни рискови фактори за тромбоемболия (спленектомия или едновременна употреба на хормонозаместителна терапия) могат да бъдат изложени на допълнителен повишен риск от тромбоемболични състояния. Помислете за тромбопрофилактика при пациенти с повишен риск от ТЕЕ. Наблюдавайте пациентите за признаци и симптоми на тромбоемболични събития и незабавно въвеждайте лечение.
Хипертония
Хипертония се съобщава при 10,7% (61/571) от пациентите, лекувани с REBLOZYL. По време на клиничните проучвания честотата на хипертония от 3 до 4 варира от 1,8% до 8,6%. При пациенти с бета таласемия с нормално изходно кръвно налягане, 13 (6,2%) пациенти развиват систолично кръвно налягане (SBP) ≥130 mm Hg и 33 (16,6%) пациенти развиват диастолично кръвно налягане (DBP) ≥ 80 mm Hg. При възрастни пациенти с MDS с нормално изходно кръвно налягане, 26 (29,9%) пациенти развиват SBP ≥130 mm Hg и 23 (16,4%) пациенти развиват DBP ≥ 80 mm Hg. Следете кръвното налягане преди всяко приложение. Управлявайте нови или обостряния на съществуваща хипертония, използвайки антихипертензивни средства.
Ембрио-фетална токсичност
REBLOZYL може да причини увреждане на плода, когато се прилага на бременна жена. REBLOZYL причинява повишена загуба след имплантацията, намален размер на постелята и повишена честота на скелетни вариации при проучвания при бременни плъхове и зайци. Посъветвайте бременните жени за потенциалния риск за плода. Посъветвайте жените с репродуктивен потенциал да използват ефективна контрацепция по време на лечението и поне 3 месеца след крайната доза.
НЕЖЕЛАНИ РЕАКЦИИ
Бета-таласемия
- Сериозни нежелани реакции са настъпили при 3,6% от пациентите на REBLOZYL. Сериозните нежелани реакции, възникващи при 1% от пациентите, включват мозъчно-съдов инцидент и дълбока венозна тромбоза. Смъртоносна нежелана реакция е настъпила при 1 пациент, лекуван с REBLOZYL, който е починал поради непотвърден случай на остра миелоидна левкемия (AML)
- Най-честите нежелани реакции (поне 10% за REBLOZYL и 1% повече от плацебо) са главоболие (26% срещу 24%), болки в костите (20% срещу 8%), артралгия (19% срещу 12%), умора (14 % срещу 13%), кашлица (14% срещу 11%), коремна болка (14% срещу 12%), диария (12% срещу 10%) и замаяност (11% срещу 5%)
Миелодиспластични синдроми
- Нежеланите реакции от степен ≥3 (≥2%) включват умора, хипертония, синкоп и мускулно-скелетна болка. Смъртоносна нежелана реакция е настъпила при 5 (2,1%) пациенти
- Най-честите (≥10%) нежелани реакции включват умора, мускулно-скелетна болка, замаяност, диария, гадене, реакции на свръхчувствителност, хипертония, главоболие, инфекция на горните дихателни пътища, бронхит и инфекция на пикочните пътища
ЛАКТАЦИЯ
Не е известно дали REBLOZYL се екскретира в кърмата или се абсорбира системно след поглъщане от кърмаче. REBLOZYL е открит в млякото на кърмещи плъхове. Когато лекарството присъства в животинското мляко, вероятно е лекарството да присъства в кърмата. Тъй като много лекарства се екскретират в кърмата и поради неизвестните ефекти на REBLOZYL при кърмачета, трябва да се вземе решение дали да се преустанови кърменето или да се прекрати лечението. Поради възможността за сериозни нежелани реакции при кърменото дете, кърменето не се препоръчва по време на лечението и в продължение на 3 месеца след последната доза.