Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Институт на науките де ла Вие, Университет Католик дьо Лувен, Лувен Ла Ла Ньов, Белгия
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Centre de Recherche du Center Hospitalier de l & Universite de Montreal (CRCHUM), University of Montreal, Montreal, QC, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Кореспонденция: Университет на Британска Колумбия, Ванкувър, BC V6T 1Z3, Канада. Имейл: [email protected] Потърсете още статии от този автор
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Институт на науките де ла Вие, Университет Католик дьо Лувен, Лувен Ла Ла Ньов, Белгия
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Centre de Recherche du Center Hospitalier de l & Universite de Montreal (CRCHUM), University of Montreal, Montreal, QC, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Фармацевтични науки, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Департамент по клетъчни и физиологични науки, Група за изследване на диабета, Институт по науките за живота, Университет на Британска Колумбия, Ванкувър, Британска Колумбия, Канада
Кореспонденция: Университет на Британска Колумбия, Ванкувър, BC V6T 1Z3, Канада. Имейл: [email protected] Потърсете още статии от този автор
Резюме
СЪКРАЩЕНИЯ:
МАТЕРИАЛИ И МЕТОДИ
Животни и in vivo физиология
Флуоресцентна микроскопия
Панкреатите от PBS-перфузирани мишки бяха събрани и фиксирани в 4% параформалдехид за 24 h, измити и съхранявани в 70% етанол, преди вграждането на парафин. Секции (5 μm) бяха взети от поне 3 различни области на панкреаса, на разстояние 100 μm. Секциите бяха депарафинизирани, хидратирани с намаляващи концентрации на етанол и изплакнати в PBS, след това изложени на 15 минути индуцирано от топлина извличане на епитоп при 95 ° C с 10 mM цитратен буфер (рН 6.0). Секциите бяха блокирани и инкубирани с първичен анти-инсулин (ab7842; Abcam, Cambridge, MA, USA) и анти-зелен флуоресцентен протеин (GFP) (A11122; Thermo Fisher Scientific, Waltham, MA, USA) за една нощ във влажна камера в 4 ° С. Първичните антитела се визуализират след инкубация с вторични антитела, конюгирани с AlexaFluor 488, 555, 594 или 647, както се изисква (1: 1000; Thermo Fisher Scientific). Гонадната и периреналната мастна тъкан се събират от мишки, оставени без храна в продължение на 4 часа, и тъканите се фиксират в 4% параформалдехид. Размерът на адипоцитите беше измерен чрез оцветяване за перилипин в участъци с дебелина 5 μm (Cell Signaling Technology, Danvers, MA, USA). Всички изображения са направени на ImageXpress micro с обектив с височина × 10 (NA 0,3).
Имуноблот анализи и откриване на протеини
В Western blot анализи са използвани 30-40 μg протеин за сондиране на полимераза I и фактор на освобождаване на транскрипт (PTRF; ab48824; Abcam); съотношението на фосфо-кавеолин-1 (3251) към общия кавеолин-1 (3267, клатрин (4796), инсулинов рецептор (3020), съотношение на фосфохормон-чувствителната липаза (Hsl; 4139) към общия Hsl (4107), съотношение на фосфо-Akt (4060) към общия Akt (9272) и съотношението на фосфо-p44/42 MAPK (4370) към общия p44/42 MAPK (4695; всички от Cell Signaling Technology); и липопротеинова липаза (Lpl; sc ‑ 32885; Санта Круз биотехнология, Далас, Тексас, САЩ) в гонадна тъкан от мишки, които са останали без храна за една нощ и по време на 15-минутна инсулинова стимулация (2 U/kg телесно тегло). Актин (NB600-501; Novusbio, Littleton, CO, САЩ) и винкулин (13901; Технология за клетъчна сигнализация) са използвани като справочници за зареждане.
Изолация на островчета, култура и перифузия
Панкреатичните островчета са изолирани с помощта на колагеназа, филтрация и ръчно бране (18). Островчетата се култивират през нощта (37 ° C, 5% CO2) в среда RPMI 1640 (Thermo Fisher Scientific) с 11 mM глюкоза (Millipore-Sigma), 100 U/ml пеницилин, 100 μg/ml стрептомицин (Thermo Fisher Scientific) и 10% фетален говежди серум (Thermo Fisher Scientific). Инвитро секрецията на инсулин се измерва чрез перифузия и радиоимуноанализ (19).
Изолация на РНК, количествена PCR в реално време и анализ на транскриптома
Микрокомпютърна томография и рентгенова абсорбциометрия с двойна енергия
Сканирането се извършва със скенер TriFoil Micro-Computed Tomography (CT) (Northridge Tri-Modality Imaging, Inc., Chatsworth, CA, USA) със следните настройки: разделителна способност, 50 μm; време за сканиране,
4 минути. Всяка мишка беше сканирана 1 седмица преди и отново 5 седмици след инжектиране на тамоксифен. Мишките бяха разположени по гръб в скенера с прав гръбначен стълб и ъгъл от минимум 90 ° между гръбначния стълб и бедрената кост, което беше потвърдено от скаутско сканиране. Животните са сканирани, докато са анестезирани (O2 при 1.0 L/min; 5% изофлуран). Анализът на сканираните изображения беше извършен със софтуер Amira 6.0.1 (FEI, Hillsboro, OR, USA). Първото трансекционно сканиране, показващо таза, беше зададено като референтно сканиране за всяка мишка. Вътрешните слоеве на коремната стена бяха приложени, за да се разграничат висцералните обеми от подкожни мазнини (μm 3). Беше определена чиста маса in vivo чрез двуенергийна рентгенова абсорбциометрия (Lunar Piximus; вече не се произвежда) денситометър при мишки 5-7 седмици след тамоксифен (от 15 контролни и 12 експериментални мишки).
Статистически анализ
Данните са изразени като средни стойности ± sem, освен ако не е посочено друго. Резултатите се считат за статистически значими при P
РЕЗУЛТАТИ И ДИСКУСИЯ
Индуцируема, частична Ins2 делеция на ген като експериментален модел за намаляване на производството на инсулин
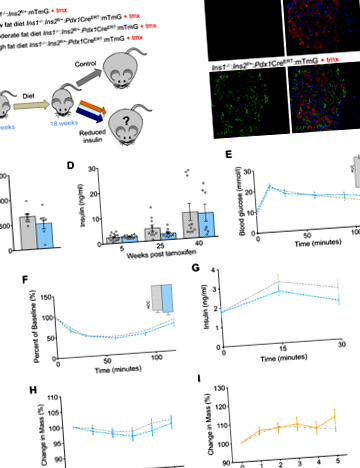
За директна оценка на трайните ефекти на хиперинсулинемията върху затлъстяването и загубата на тегло, генерирахме модел на мишка, при който дозата на инсулиновия ген може да бъде намалена чрез използване на индуцируема система Cre-loxP (Фиг. 1A). На 6 седмична възраст мишките се хранеха с 1 от 3 диети; ниско съдържание на мазнини (10%), умерено съдържание на мазнини (25%) или високо съдържание на мазнини (58%). След 12 седмици консумация на тези диети, контрол на отпадъци (Ins1 -/-: Ins2 f /+: mTmG) и експериментален (Ins1 -/-: Ins2 f/+: Pdx1Cre ERT: mTmG) мъжки мишки се инжектират интраперитонеално с тамоксифен, което води до почти пълна рекомбинация на този генетичен фон (фиг. 1)Б.) (20).
Индуцируема частична загуба на Ins2 не влияе върху теглото на мишките, хранени с диета с умерено или ниско съдържание на мазнини
Манипулация на Ins2 генната доза при експериментални мишки, хранени с диета с умерено съдържание на мазнини, не е повлияла значително нивата на инсулиновите острови (Фиг° С), нито тази манипулация е довела до статистически значима промяна в циркулиращия инсулин при експериментални мишки през цялото проучване (Фиг. 1д). В съответствие с тези констатации, глюкозният толеранс, инсулиновата чувствителност и стимулираната от глюкоза секреция на инсулин не са нарушени при експериментални мишки в сравнение с контролните кученца в контекста на тази диета (Фиг. 1E – G). Понижаване на Ins2 генната доза при мъжки мишки не повлиява телесната маса при мишки, хранени с диета с умерено съдържание на мазнини (фигЗ.). По подобен начин телесната маса е непроменена след намаляване на Ins2 генна доза при експериментални мишки, хранени с диета с ниско съдържание на мазнини (Фиг. 1Аз). Тези резултати са в съответствие с предишни доказателства от други генетични манипулации, които не засягат телесната маса при мишки, хранени с диети с ниско или умерено съдържание на мазнини (21).
Индуцируемото намаляване на гена Ins2 умерено намалява островната секреция на инсулин при мишки, хранени с HFD
Индуцируемото намаляване на инсулина причинява загуба на тегло при мишки, хранени с HFD
За да проверим нашата хипотеза, че затлъстяването може да бъде обърнато чрез остро потискане на инсулина, ние изследвахме телесното тегло на HFD хранени контролни кученца и експериментални мишки 5 седмици след инжектиране на тамоксифен. В пилотно проучване открихме, че инжектирането на тамоксифен води до леко намаляване на телесната маса в сравнение с това при мишки, третирани с носител (допълнителна фигура S1). За да бъдем консервативни, сметнахме, че е най-подходящо да сравним групи мишки, които и двете са били инжектирани с тамоксифен. Използвайки този консервативен подход, установихме, че острото намаляване на Ins2 генна доза доведе до
Маркерите за липидна мобилизация се променят след индуцирано намаляване на инсулина
Индуцируемото намаляване на инсулина е свързано с променен имунен профил в мастната тъкан
| Кръвни микрочастици | 4.24Е - 09 |
| Активност на липиден транспортер | 1.73E - 02 |
| Транспорт на липиди | 2.62E - 02 |
| Свързване на стероиди | 2.62E - 02 |
| Богати на триглицериди липопротеинови частици | 4.78E - 02 |
| Частица липопротеини с много ниска плътност | 4.78E - 02 |
| Неутрален липиден метаболитен процес | 6.20E - 02 |
| Отговор на вируса | 6.20E - 02 |
| Извънклетъчен матрикс | 6.20E - 02 |
| Зависим от циклин протеин киназа холоензимен комплекс | 6.20E - 02 |
| Метаболитен процес на ацилглицерол | 6.20E - 02 |
| Локализация на липидите | 6.20E - 02 |
| Плазмена липопротеинова частица | 6.51E - 02 |
| Свързване с фосфолипиди | 6.97Е - 02 |
| Протеин-липиден комплекс | 7.08E - 02 |
| Чревна абсорбция | 7.74Е - 02 |
| Аденилилтраснферазна активност | 7.74Е - 02 |
| Свързване с рецептора на липопротеинови частици | 8.96E - 02 |
Нашите данни предоставят първите молекулярно генетични доказателства, че затлъстяването може да бъде обърнато чрез рязко и умерено намаляване на производството само на инсулин. Резултатите от това проучване на лечението, комбинирано с предишните ни проучвания за превенция (11, 12), ясно показват причинно-следствения контрол на затлъстяването чрез хиперинсулинемия в генетично проследима система на бозайници. Степента на намаляване на дозата на инсулиновия ген, постигната в настоящото ни проучване (
30%) не причинява промени в хомеостазата на глюкозата и е постижимо при човешки популации като превантивна мярка или стратегия за отслабване. Например, периодично и непрекъснато ограничаване на енергията за период от 6 месеца води до подобни намаления в циркулиращия инсулин при пациенти със затлъстяване, съчетани с 5-10% загуба на телесно тегло (48). Въпреки че такива интервенции за ограничаване на храненето често са свързани с висок процент на отпадане (49), изокалоричното ограничение на дневния прием на фруктоза от 28 до 10% е алтернативен подход, който може да смекчи високите нива на отпадане и е доказано успешно, че постига подобни намаления в циркулиращия инсулин и загуба на тегло при затлъстели юноши (50). Степента на загуба на тегло в нашето проучване, когато е преведена на хора, е свързана с подобрения на рисковите фактори, свързани със сърдечно-съдови заболявания, както и намаляване на риска от развитие на диабет тип 2 с повече от 50% (51).
ЗАКЛЮЧЕНИЯ
Нашите резултати имат дълбоки последици за хранителните насоки и терапевтичните усилия за борба със затлъстяването и съпътстващите заболявания. Нашите открития подкрепят концепцията, че състоянието на хиперинсулинемия на индивида трябва да бъде цел за модификации на начина на живот, диетичен състав на макронутриенти и разработване на лекарства за целите на отслабването. Проучванията, при които се оценяват индивидуализирани диетични отговори (52) и се определят механично, ще бъдат полезни при проектирането на персонализирани нутригеномни стратегии. Подходите, които физиологично модулират нивата на инсулина, могат също да имат терапевтична полза отвъд загубата на тегло, включително при подобряване на чувствителността към инсулин и може би дори дълголетие (53).
ПРИЗНАВАНИЯ
Авторите благодарят на Farnaz Taghizadeh и Xiaoke (Betty) Hu [и двамата с Университета на Британска Колумбия (UBC)] за съдействие при изолации на островчета, перифузии и работа с животни; консорциумът за последователност и биоинформатика на UBC за секвениране на РНК; Центърът за високопроизводителна феногеномика на UBC за микро-КТ изображения; и Джон Шипилоу и д-р Нанси Форд (UBC) за техническа поддръжка и помощ. Центърът се подкрепя от Канадската фондация за иновации, Фондацията за развитие на знанията на Британска Колумбия и Стоматологичния факултет на UBC. Финансовата подкрепа беше предоставена чрез оперативна субсидия от Канадските институти за здравни изследвания; Награди за стипендии на Канадската асоциация за диабет (на M.M.P. и MS); награда за изследователска работа на канадска асоциация за диабет (на A.P.C.); стипендия на Фондация Бензон (за S.S.); и Фондация за изследване на младежкия диабет и Фондация за здравни изследвания на Майкъл Смит за докторантски стипендии (на G.E.L.) Авторите не декларират конфликт на интереси.
ВНОСКИ НА АВТОРА
М. М. Пейдж проектира и извършва експерименти, анализира резултатите и пише ръкописа; S. Skovsø извърши микро-CT сканиране и анализ; H. Cen, A. P. Chiu и G. E. Lim извършват Western blot анализи; D. A. Dionne и D. F. Hutchinson извършиха експерименти; М. Сабат извърши образни експерименти и анализи; S. Flibotte извърши анализ на РНК секвениране; S. Sinha извърши РНК секвениране; и Дж. Д. Джонсън проектира експерименти, анализира резултатите, редактира ръкописа и е гарант за тази работа; и всички други автори прегледаха и редактираха ръкописа.
| fsb2fj201700518r-sup-0001.docxapplication/docx, 71 KB | Допълнителен материал |
Моля, обърнете внимание: Издателят не носи отговорност за съдържанието или функционалността на която и да е поддържаща информация, предоставена от авторите. Всички заявки (различни от липсващо съдържание) трябва да бъдат насочени към съответния автор на статията.
- Учените идентифицират ген, свързан с тънкостта, който може да помогне да се противопоставят на наддаването на тегло - ScienceDaily
- Замяна на калорични напитки с вода или диетични напитки за отслабване при възрастни основни резултати от
- Отпуснете се, спечеленото наддаване на тегло през уикенда; да убиете вашата диета; Диаграмата
- Причини за наддаване на тегло, които не са; t, свързани с вашата диета - Insider
- Обратимост на предизвиканото от психотропно лечение наддаване на тегло сред деца и юноши с