Фани Ланглет
1 Център за диабет Наоми Бери и Медицински отдели, Колумбийски университет, Ню Йорк, 10032, САЩ
Марсел Тарбие
2 Лаборатория „Наука за живота“, Департамент по молекулярни биологии, Институт Уенър-Грен, Стокхолмски университет, 17121, Стокхолм, Швеция
Ребека А. Хейслер
3 Център за диабет Наоми Бери и отдели по патология и клетъчна биология, Колумбийски университет, Ню Йорк, 10032, САЩ
Стефания Камастра
4 Катедра по клинична и експериментална медицина, Медицински факултет на Университета в Пиза, Пиза, Италия
Елеутерио Феранини
4 Катедра по клинична и експериментална медицина, Медицински факултет на Университета в Пиза, Пиза, Италия
5 CNR Институт по клинична физиология, Пиза, Италия
Марк Р. Фридлендер
2 Лаборатория „Наука за живота“, Департамент по молекулярни биологии, Институт Уенър-Грен, Стокхолмски университет, 17121, Стокхолм, Швеция
Доменико Ачили
1 Център за диабет Наоми Бери и Медицински отдели, Колумбийски университет, Ню Йорк, 10032, САЩ
Свързани данни
Резюме
Цели
Чернодробната инсулинова резистентност е отличителен белег на диабет тип 2 и затлъстяване. Сигнализирането на инсулиновия рецептор чрез AKT и FOXO има важни метаболитни ефекти, които традиционно се приписват на регулирането на генната експресия. Не е известно обаче дали всички метаболитни ефекти на FOXO произтичат от неговата регулация на кодиращите протеини иРНК.
Методи
За да отговорим на този въпрос, ние получихме профили на експресия на FOXO-регулирани миши чернодробни микроРНК (miRNAs) по време на гладуване и повторно хранене, използвайки мишки, които нямат Foxo1, 3a и 4 в черния дроб (L-Foxo1,3a, 4).
Резултати
От 439 анализирани miRNA, 175 са диференцирано изразени в нокаути на Foxo. Техните функции са свързани с инсулин, Wnt, Mapk сигнализиране и стареене. Сред тях отчитаме поразително увеличение на експресията на miR-205-5p при L-Foxo1,3a, 4 нокаута, както и при затлъстели мишки. Ние показваме, че miR-205-5p усилването на функцията увеличава фосфорилирането на AKT и намалява SHIP2 в първичните хепатоцити, което води до инхибиране на FOXO. Това води до намалено производство на хепатоцитна глюкоза. В съответствие с тези наблюдения, miR-205-5p повишаване на функцията при мишки понижава нивата на глюкоза и подобрява толерантността към пируват.
Заключения
Тези открития разкриват хомеостатичен miRNA контур, регулиращ инсулиновата сигнализация, с потенциални последици за in vivo метаболизма на глюкозата.
1. Въведение
Инсулиновата резистентност предразполага към диабет и затлъстяване [1]. Плейотропните ефекти на инсулина са частично медиирани от пътя PI3K/AKT/FOXO1 [1], [2], [3]. В черния дроб инсулинът намалява производството на глюкоза и увеличава използването на глюкоза чрез инхибиране на FOXO, докато инсулиновата резистентност активира FOXO, допринасяйки за хипергликемия и хипертриглицеридемия [4], [5]. Кодиращите протеини гени на FOXO са проучени подробно [6], [7], [8]. Въпреки това, малко е известно за FOXO регулирането на генната експресия чрез микро-РНК (miRNA)-медиирано генно заглушаване.
miRNAs регулират генната експресия във физиологични и болестни състояния, включително инсулиноустойчив диабет [9], [10]. Интересното е, че проучванията за асоцииране на генома за локусите на чувствителност към диабет тип 2 показват, че повечето от свързаните с диабета варианти се локализират в некодиращи региони [11], [12], повишавайки възможността миРНК, транскрибирани от тези региони, да допринесат за развитието на заболяването. Няколко чернодробни miRNAs, включително miR-33 [13], miR-122 [14], miR103/107 [15] и miR-802 [16], са показали, че след транскрипция контролират експресията на гени, участващи в метаболизма и инсулиновата сигнализация.
Като се има предвид ролята на FOXO в инсулиновото действие, ние предприехме систематично търсене на FOXO регулирани чернодробни miRNAs и изследвахме тяхната метаболитна роля. Използвайки miRNA профилиране на FOXO-дефицитни мишки, ние каталогизирахме FOXO-модулирани miRNAs и идентифицирахме miR-205-5p като ендогенен регулатор на инсулиновата чувствителност, който координирано насочва компонентите на инсулиновата сигнална каскада.
2. Материал и методи
2.1. Експериментален модел и подробности за предмета
2.1.1. Мишки
Мъжки мишки (на възраст 9-24 седмици) се поддържат в чау (PicoLab диета за гризачи 20, 5053; Purina Mills). Всички експерименти са одобрени от институционалния комитет за грижа и употреба на животните в университета Колумбия.
L-Foxo1, L-Foxo1,3a, 4, db/db, ob/ob и Sin3a lox/lox: Sin3b lox/lox [3], [4], [6], [17] и iL-Sin3a/Описани са 3b мишки [6]. C57Bl6, ob/ob, db/db и 10-седмични DIO мишки бяха от The Jackson Laboratories. За да свръхекспресираме miR-205-5p, инжектирахме 1 × 10 11 частици (AAV8.TBG.miRNA (Scramble) -CMV-GFP или AAV8.TBG.miR-205-5p-CMV-GFP) в C57Bl6J и убихме животните след 25 дни. За нокдаун на miR-205-5p, мишките C57Bl6J бяха хранени с високо съдържание на мазнини в продължение на 10 седмици (DIO) (OpenSource Diets, Cat #: D12492) и инжектирани с потребителски miRCURY LNA (Exiqon, hsa-miR-205-5p) (Партида nb: 681392) или контрол (Партида nb: 681393) (15 mg/kg) за 3 дни и убит след 25 дни.
За miRNA секвениране и miR-205 печалба на функция, L-Foxo1,3a, 4 и C57Bl6J мишки бяха на гладно през нощта и се пречистват (или не) в продължение на 4 часа. За miR-205 загуба на функция, DIO мишките бяха на гладно в продължение на 5 часа. За qPCR, L-Foxo1, L-Foxo1,3a, 4 и iL-Sin3a/3b мишки бяха на гладно през нощта; ob/ob, db/db и DIO мишки за 5 часа.
2.1.2. Първична хепатоцитна култура
Първичните хепатоцити бяха изолирани и трансфектирани с плазмиди (500 ng/5 × 105 клетки, 48 часа), използвайки Lipofectamine2000, както е описано [18]. miR-205-5p беше свръхекспресиран с miRCURY LNA miRNA Mimics (15-50nM/5 × 105 клетки, 48 часа) срещу миши miR-205-5p; cel-39-3p беше използван като контрол. Клетките се инкубират със 100 uM 8-CPT-cAMP, 1 uM dex, 100 nM инсулин или носител за 7 часа.
2.1.3. Човешки изследвания
Чернодробни биопсии са получени по време на бариатрична хирургия при 10 диабетици тип 2 и 10 недиабетици [19], [20]. Екстрахирахме РНК с РНК-по-късно (Ambion Inc., Applied Biosystems, Austin, TX, USA) и получихме плазмени проби след бързо нощуване. Пациентите с диабет са прекратили лечението 48–72 часа преди проучването. Протоколът е одобрен от университета в Пиза IRB. Естеството и целта на изследването бяха внимателно обяснени на всички участници, преди да дадат писмено съгласие за участие.
2.2. Подробности за метода
2.2.1. Химикали и антитела
Реагентите са от следните производители: кетамин (KetaSet ®), ксилазин (AnaSed ®), Medium 199, HBSS, EGTA, HEPES, PenStrep и гентамицин (Life Technology), колаген 4 (Worthington), Humulin ® R U-100 (Lilly) ), 8- (4-хлорофенилтио) (CPT) -cAMP, дексаметазон, циклохексимид, говежди серумен албумин, d -глюкоза и натриев пируват (Sigma – Aldrich), Lipofectamine2000 (Thermo Fisher), miRCURY LNA (Qiagen) (биотинилиран miamu) 205-5p и cel-39-3p), anti-FOXO1 (C29H4, # 2880S), anti-Phospho-FoxO1 (Thr24)/FoxO3a (Thr32) (# 2599S), anti-Akt, anti-Phospho-Akt (Ser473 ) (D9E, # 4060), анти-SHIP2 (# 3397S) и анти-PTEN (# 9188S) (клетъчна сигнализация), анти-актин (ab8227) (Abcam).
2.2.2. Плазмиди/вируси
RFP (CTL) и FOXO1 плазмидите са описани [21]. Плазмидите, кодиращи miTarget ™ 3′UTR miRNA Target Clones бяха от GeneCopoeia (CTRL: CmiT000001-MT05 и FOXO1: Mmi7055419-MT05); AAV8.TBG.eGFP и AAV8.TBG.Cre от Penn Vector Core; AAV8.TBG.miRNA (Scramble) -CMV-GFP и AAV8.TBG.miR-205-5p-CMV-GFP от SignaGene.
2.2.3. Изследвания на РНК и miRNA
За qPCR използвахме RNeasy kit (Qiagen), GoScript (Promega) и GoTaq ® qPCR Master Mix (Promega). Нивата на генна експресия са нормализирани до TATA-свързващ протеин (TBP), използвайки метода 2 -ΔΔCt и са представени като относителни нива на транскрипт. За изследвания с miRNA изолирахме РНК с Mirvana (Thermo Fisher, AM1560) или Trizol (Life Technologies). За miRNA секвениране, общата РНК беше количествено определена с Ribogreen и библиотеките бяха подготвени с TruSeq (Illumina, Сан Диего, Калифорния), количествено определена с Agilent 2100 Bioanalyzer (Agilent Technologies, Santa Clara, CA) HighSensitivity kit и секвенирана на единичен Illumina HiSeq 2500 Rapid край 50 цикъл поток клетка. Етикетите с ниско качество бяха променени с FASTX-Toolkit (http://hannon-lab.cshl.edu/fastx_toolkit/). Четенията бяха обработени с тръбопровода miraligner и картографирани в miRBase v.20. За miRNA qPCR използвахме miScript II RT Kit (Qiagen) и miScript SYBR Green PCR Kit (Qiagen). Грундовите анализи са от Qiagen. SNORD61 беше използван за нормализиране на нивата на miRNA, използвайки метода 2 -ΔΔCt.
2.2.4. Анализ на протеини
Екстрахирахме протеини в лизисен буфер (20 mM Tris-HCl (рН = 7,4), 150 mM NaCl, 10% глицерол, 2% NP-40, 1 mM EDTA, 20 mM NaF, 30 mM Na4P2O7, 0,2% SDS, 0,5% натриев дезоксихолат) с протеазен/фосфатазен инхибиторен коктейл (1Х, клетъчно сигнализиране) и използвани 0,15 mg в буфер за SDS за вестерн-блот. Използвахме ImageJ (Национален здравен институт) за денситометрия.
2.2.5. Анализи на луцифераза
Ние трансфектирахме хепатоцити с плазмиди, кодиращи миТаргет ™ 3′UTR миРНК целеви клонинги (1ug/5 × 10 5 клетки), или миРНК имитира (50 nM), използвайки Lipofectamine 2000 (Invitrogen). 48 часа след трансфекцията, ние изследвахме луцифераза с комплект за анализ на двойна луминесценция Secrete-Pair ™ (GeneCopoeia) в луминометър с микроплаки Orion L (Berthold).
2.2.6. Метаболитни изследвания
Описано е производството на глюкоза и липогенезата в първичните хепатоцитни култури [18]. Проведохме тестове за толерантност към глюкоза и пируват при 9-15-седмични мъжки мишки след 16-часово гладуване, използвайки 2 g глюкоза или пируват/кг, и тестове за толерантност към инсулин след 5-часов пост, използвайки 0,6 U инсулин/кг. Чернодробните триглицериди, холестерол [22] и гликоген бяха измерени, както е описано [5]. Измерихме глюкоза с OneTouch (One Touch Ultra, Bayer), триглицериди (Infinity, # TR22421, ThermoFisher), холестерол (Cholesterol E, # 439–17501, Wako Pure химикали) и NEFA (HR Series NEFA-HR (2), # 999–34691, # 995–34791, # 991–34891, # 993–35191, чисти химикали Wako) чрез колориметрични анализи.
2.2.7. Статистика
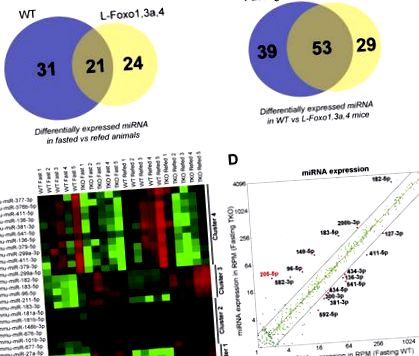
FOXO модулират чернодробната miRNA. A-B, Диаграми на Venn, обобщаващи диференциално експресирани miRNAs (A) между пости и повторни условия и (Б.) между WT и L-Foxo1,3a, 4 мишки (n = 5 на група). ° С, Топлинна карта на експресията на miRNA от WT и L-Foxo1,3a, 4 мишки. д, Разпръскване на експресия на miRNA в четения на милион (RPM) в гладно WT срещу L- Foxo1,3a, 4 мишки.
3.2. Регламентираните от FOXOs miRNAs са насочени към MAPK, Wnt и инсулинова сигнализация
След това изградихме топлинна карта, сравняваща диференциално експресираните miRNAs в WT срещу L-Foxo1,3a, 4 мишки на гладно и в условия на глад, използвайки 5% степен на фалшиво откриване, и извършихме йерархично групиране (Фигура 1 С). Открихме четири клъстера: клъстери 1 и 2 включваха miRNA, чиято експресия не се регулираше на гладно или повторно хранене, но се увеличи в L-Foxo1,3a, 4 мишки в по-голяма (клъстер 1) или по-малка степен (клъстер 2); клъстерите 3 и 4 включват miRNA, регулирана в състояние на гладно спрямо хранене, чиито нива се увеличават (клъстер 3) или намаляват (клъстер 4) в L-Foxo1,3a, 4 мишки. Заключението от тези данни е, че FOXO са способни както да индуцират, така и да инхибират експресията на miRNA, както правят при генната експресия [6]. Нещо повече, наблюдението, че регулирането от FOXO на пръв поглед превъзхожда регулирането от състоянието на хранене за клъстери 1-2, предполага, че ефектите на FOXO върху експресията на miRNA могат да бъдат преки и косвени.
След това генерирахме разпръснати графики на отделни miRNAs като функция от техните нива в WT на гладно срещу L-Foxo1,3a, 4 мишки (Фигура 1 D). От този анализ избрахме miRNAs, изразени на нива> 5 четения на милион, които показаха значително (p Фигура 2 A) по време на гладуване и ∼80% намаление при повторно хранене (Фигура S1A), което показва, че FOXO потискат чернодробните miR-205- 5р по време на гладуване. Интересното е, че видяхме само 2-кратно увеличение на единични нокаутиращи мишки L-Foxo1 (Фигура 2 B), което предполага, че голямото увеличение на L-Foxo1,3a, 4 мишки вероятно се дължи на FOXO3 (нивата на FOXO4 са много ниски), или че трите изоформи могат да се компенсират една друга. В първичните хепатоцити от мишки L-Foxo1, mmu-miR-205-5p се увеличи 2 пъти (Фигура 2 С) и увеличението беше частично обърнато чрез трансфекция на FOXO1 (Фигура S1B). Освен това mmu-miR-205-5p не се регулира от сАМР/дексаметазон или инсулин в първични хепатоцити от мишки L-Foxo1 (Фигура 2 С), като не успява да имитира ефекта от гладуването и повторното хранене. Това предполага, че регулацията се губи по време на култивиране на хепатоцити, или че косвените механизми опосредстват инхибирането на miR-205 от FOXOs in vivo.
Чернодробна експресия на miRNA-205 при мишки и хора. A-B, експресия на miR-205-5p в черния дроб на WT срещу L-Foxo1,3a, 4 (n = 5 на група) и L-Foxo1 (n = 7 и 9, съответно), измерена чрез qPCR. ° С, експресия на miR-205-5p в първични хепатоцити от контролни WT или L-Foxo1 мишки след 7-часово третиране с носител, cAMP/dex, cAMP/dex/инсулин (n = 4 на група). D-G, експресия на miR-205-5p в черния дроб на WT срещу iL-Sin3a/b (д) (n = 6 и 7, съответно), чау срещу диети, индуцирани затлъстели мишки (DIO) мишки (Д), n = 5 на група), WT срещу ob/ob мишки (F) (n = 5 на група), WT срещу хиперинсулинемични db/db (ins high) (G, n = 7/4, съответно). Данните са средни ± SEM. * P lox/lox: Sin3b мишки lox/lox (iL-Sin3a/b мишки) [6]. Не открихме промени в miR-205-5p при постигнати през нощта iL-Sin3a/b в сравнение с WT мишки (Фигура 2 D). Неуспехът на FOXO да свърже кандидат-регулаторни региони на гена miR-205 и липсата на вариации на miR-205-5p при iL-Sin3a/b мишки или на регулация чрез гладуване срещу повторно хранене (in vivo) или чрез cAMP/dex срещу инсулин (in vitro) предполагат, че miR-205-5p се регулира от FOXO косвено, вероятно чрез инхибиране на потенциален miR-205 активатор.
Предвид потенциалната му роля в инсулиновата сигнализация, ние анализирахме регулирането на miR-205-5p при затлъстяване, инсулинова резистентност и диабет тип 2. При индуцирано от диета затлъстяване (DIO), ob/ob C57J/B6 и хиперинсулинемични db/db мишки с начална хипергликемия (~ 200 mg/dl) (Фигура 2 E, F и G, съответно), miR-205-5p се увеличава след 5-часов бърз в сравнение с контролите. Това е в съответствие с предишни доклади, показващи, че чернодробният miR-205-5p се увеличава при резистентни на диабет, но не и при мишки, податливи на диабет [36].
3.4. Mmu-miR-205-5p инхибира експресията на FOXO1 и засилва инсулиновата сигнализация
Предвид потенциалната му роля в сигнализирането на PI3k/Akt [37], [38], [39], ние анализирахме въздействието на свръхекспресията на miR-205-5p върху инсулиновата сигнализация чрез трансфекция на първични миши хепатоцити с имитация на miR-205-5p. Свръхекспресията върху miR-205-5p в хепатоцитите повишава базалното AKT фосфорилиране, без да променя нивата на протеини. Този ефект е притъпен от cAMP/dex (Фигура 3 А-С). Увеличението на AKT фосфорилирането е свързано с повишено фосфорилиране на FOXO1 на T24 (Фигура 3 A, D). miR-205-5p активира PI3K/AKT чрез насочване на PIP3 фосфатази Pten [37] и Ship2 [40]. В първичните хепатоцити свръхекспресията на miR-205-5p намалява Ship2 и увеличава Phlpp2 (Фигура 3 Д), но няма ефект върху Pten. Анализът на нивата на протеин чрез Western blot потвърждава тези данни (Фигура 3 F-H). Тези резултати показват, че miR-205-5p подобрява инсулиновата сигнализация in vitro.
- Пептидът подобрява чувствителността към глюкоза и инсулин, намалява теглото при мишките. Констатациите предполагат потенциал
- Чувствителност към глутен без целиакия и репродуктивни нарушения
- Метаболитното здраве е по-тясно свързано с намаляване на белодробната функция, отколкото затлъстяването
- Novo Nordisk открива завод за инсулин в руския Pharmafile
- Сестрински интервенции Захарен диабет тип 2 Инсулинова резистентност към кофеин - Opther Diabetes Health