Резюме
ВЪВЕДЕНИЕ
Примковите диуретици, като фуроземид, се използват широко за намаляване на претоварването с течности при пациентите и са добре известни със своите ефекти на загуба на бъбреците, които често предизвикват хипокалиемия (11, 12, 22). Индуцираното от фуроземид K загуба е резултат от инхибиране на реабсорбцията на Na в дебелия възходящ крайник на Henle (TAL), с повишено доставяне на Na до чувствителния към алдостерон дистален нефрон, което стимулира секрецията на K в замяна на Na-медииран Na епителен канал (ENaC) реабсорбция (25). Повечето пациенти, които се лекуват с фуроземид, са на „западна” диета, характеризираща се с относително високо съдържание на Na и ниско съдържание на К и тенденция към киселинно натоварване. Пропиляването на K при тези пациенти може да бъде предотвратено чрез прилагане на амилорид (2), инхибитор на ENaC, за да се предотврати реабсорбцията на Na, която задвижва секрецията на K през бъбречния външен медуларен K (ROMK) канал. Въпреки това, по-често пациентите са избрали диети с ниско съдържание на Na, високо K (LNaHK), които са известни със своите антихипертензивни ефекти, както се разкрива от проучването на диетичните подходи за спиране на хипертонията (DASH) (1, 23) и проучвания на субекти на диети в средиземноморски стил (14, 33). Не е ясно как се поддържа K хомеостазата, когато диуретиците с цикли се приемат от пациенти, които се придържат към такива диети.
В допълнение към високото съдържание на К, много „древни“ вегетариански диети са и алкални, което е фактор, допринасящ за здравината на костите (21). Степента, до която диетата DASH е алкална, е несигурна. Въпреки това, при членове на изолираното южноамериканско племе Яномами, които са показали ниско кръвно налягане, докато са били на вегетарианска диета с почти нулево съдържание на Na и високо К, високото алкално съдържание е било високо, както се разкрива от много ниска концентрация на Cl в урината (19 ). Нашите високи (5%) - K диети са проектирани да бъдат по същия начин алкални благодарение на равни порции K-хлорид, K-карбонат и K-цитрат (28, 29). Тази комбинация води до средно рН на урината от 8,4, за разлика от 6,3, при мишки, хранени с нормална К-диета или високо-К диета само с Cl като противоположно значение.
Неотдавнашното ни проучване установи, че фуроземидът е диуретик, изразходващ K, при мишки, хранени с нормална диета (0,3% Na и 0,6% K) и K-щадящ агент при животни, хранени с диета с нормален Na, високо K (HK) (0,3 % Na, 5% K) (28) или диета LNaHK (0,01% Na, 5% K) (29). При мишки, хранени с HK диета, фуроземидът щади K чрез инхибиране на K секрецията чрез Ca-активиран K (BK) канал с голяма проводимост във връзка с BK β4-субединицата (BK-α/β4) в свързващия канал и кортикалния събирателен канал (28). При мишки, хранени с диета LNaHK, фуроземидът има допълнителен ефект: той повишава плазмената К концентрация ([K]) чрез инхибиране на секрецията на К от TAL (29).
ЕФЕКТИ НА ФУРОСЕМИДЪТ НА СЕКРЕТИЯТА К В СВЪРЗВАЩАТА ТРЪБА НА МИШКИТЕ, ХРАНЕНИ ОТ ХАК ДИЕТА
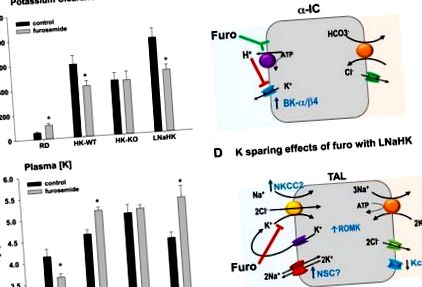
При мишки, хранени с нормална диета, TAL реабсорбира 20% от филтрирания К чрез процес, включващ поглъщане чрез Na-K-2 Cl транспортер (NKCC2) в апикалната мембрана и реабсорбция през изправящ навътре К канал през базолатералната мембрана ( 10). Както е показано на фиг. 1, А и В, лечението с фуроземид причинява значително загуба на К при мишки, хранени с редовна диета. Фуроземидът има значителен К-съхраняващ ефект при HK диети, хранени с див тип (WT) мишки, но не и при мишки с нокаут на BK-β4. Тези резултати предполагат, че K-щадящият ефект е локализиран в чувствителния към алдостерон дистален нефрон, където BK-α/β4 секретира K при мишки, хранени с високо-K, алкална диета (32). Тъй като фуроземидът подкислява урината (35), BK-α/β4-медиираната K секреция е отменена. Няма K-щадящ ефект на фуроземид при HK диетични мишки, лекувани с ацетазоламид за алкализиране на урината (28).
A и B: K клирънс и плазмена K концентрация ([K]) 7 дни след като необработена (контролна) или обработена с фуроземид питейна вода е предоставена на мишки от див тип (WT), хранени с редовна диета (RD; 0,3% Na, 0,6 % K), диета с ниско съдържание на Na, високо K (LNaHK) (0,01% Na, 5% K) или диета с високо съдържание на K (HK-WT) (0,3% Na, 5% K) и Ca- с голяма проводимост активирани K канал β4-субединица (BK-β4) -нокаут мишки, хранени с HK диета (HK-KO). Всички диети са дадени за 7–10 дни преди започване на пречистването на водата. Стойностите са средни стойности ± SE; n = 4-6 за RD; n = 12-14 за HK-WT; п = 7–8 за HK-KO; и n = 4 за LNaHK. * P Фиг. 1C). Western blot анализът на бъбречната кора разкрива, че експресията на BK-β4 е намалена, когато фуроземид е добавен към питейната вода. Нещо повече, имунохистохимичното оцветяване показва, че фуроземидът води до намаляване на апикалната до цитоплазмената експресия на BK-α. Този ефект е обърнат, когато ацетазоламид се прилага заедно с фуроземид за алкализиране на урината. Механизмът, при който алкална урина (в резултат на ацетазоламид или алкално хранене) увеличава експресията на BK-β4, не е разбран. Въпреки това, BK-β4 предотвратява разграждането на BK-α през лизозомния път (32), като по този начин поддържа повече BK-α в апикалната мембрана.
Механизмът на индуцираното от фуроземид подкисляване на урината е изследван от няколко групи. Едно проучване показа, че фуроземидът инхибира Na/H обменника в TAL (7), а друго показва, че фуроземид стимулира вакуоларна АТФаза (V-ATPase), медиирана H + секреция (13). Много изследвания предполагат, че H + се стимулира, тъй като фуроземидът увеличава дисталното доставяне на Na, което засилва деполяризацията на луминалната мембрана и електрическата движеща сила за секрецията на H + (3, 31). Нашето проучване не определи in situ дейностите на Na/H обменника в TAL или V-ATPase в интеркалирани клетки (29). Фуроземидът обаче повишава експресията на V-ATPase в свързващата тубула с> 100% (28). Това е в съгласие с констатацията, че фуроземидът не подкислява урината на мишките със селективен нокаут на V-ATPase B1 субединицата на свързващия канал (13).
ЕФЕКТИ НА ФУРОСЕМИД ВЪВ ВРЪЗКА С МИШКИТЕ, ХРАНЕНИ С ДИЕТА LNaHK
По-дълбоко намаляване на клирънса на K и увеличаване на [K] се наблюдава при мишки, хранени с диета LNaHK и лекувани с фуроземид, в сравнение с мишки, хранени с HK диета (Фиг. 1, A и B) (29). Микропунктурата на ранния дистален канал на мишки, хранени с LNaHK, но не и с HK, разкрива нетна секреция на К от TAL, която е премахната, когато мишките са били лекувани с фуроземид или когато е използвана ROMK-нокаут (ROMK-KO) мишка [ Реф. 29; вижте също коментар, свързан с това изследване (4)]. Това проучване in vivo подкрепя предишно проучване ex vivo, при което изолираният перфузиран TAL на хамстер показва нетна секреция на К (27). Корковият TAL показа нетна секреция на К с ниска базолатерална К проводимост. За разлика от това, медуларният TAL, който имаше висока базолатерална К проводимост, не показва нетна K секреция (34). Не установихме дали TAL на мишката показва подобна хетерогенност по отношение на секрецията на K в кората в сравнение с медуларния TAL.
По отношение на влиянието на високо диетично К, ние предполагаме, че повишената плазма [К], независимо от алдостерона, може да инициира сигнализиране за насочване на клетъчния К към апикалната мембрана за секреция, а не към базолатералната мембрана за рециклиране/реабсорбция. Предишни проучвания със скоби разкриха 30-pS (17) и 70-pS (16) ROMK канал, който се използва за рециклиране на луминал К. При липса на ROMK канал (ROMK-KO), мишките проявяват синдром на Бартър тип 2, характеризиращ се със загуба на Na и концентрационна способност на TAL (15). Нашите експерименти със скоби разкриха повишена вероятност за отваряне на 70-pS ROMK канала в TAL на мишки, хранени с диета LNaHK (29). 70-pS канал и нетна K секреция при мишки, хранени с диетата LNaHK, липсват при ROMK-KO мишки, което показва ролята на 70-pS ROMK канала в нетна K секреция.
Високата плазма [K] може също да инициира сигнализиране, за да инхибира базолатералния К канал на TAL. Като прецедент на това схващане, високата плазма [K] сигнализира за намаляване на реабсорбцията на NaCl в дисталната извита тубула (26), отчасти чрез инхибиране на базолатералния К канал, съдържащ хетеромер на K напрежените канали KCNJ10 и KCNJ16 ( Kir4.1/5.1) (30). Доказателствата сочат, че базолатералният K канал на TAL също включва KCNJ10 (36). Експериментите със скоби обаче разкриват други K канали в базолатералния TAL на мишки KCNJ10 -/- (8).
В допълнение към ROMK канала, ние открихме и 33-pS неселективен катионен канал (NSC-33) в апикалната мембрана на изолирания разделен отворен TAL. NSC-33 показва значително увеличение на вероятността за отваряне на канала при мишки, хранени с диета LNaHK [1,26 ± 0,18 (n = 13) за диета LNaHK срещу 0,68 ± 0,10 (n = 13) за редовна диета; непубликувани наблюдения]. NSC-33 може да осигури както входен път на Na, с деполяризираща движеща сила, така и изходен път K за секреция на K. Аргинин вазопресин активира 28-pS NSC чрез cAMP в клетки A6, дистална клетъчна линия (18). Не е изследвано дали активността на NSC-33 се увеличава при нисък прием на Na или аргинин вазопресин.
В заключение, въпреки че фуроземидът има добре установени K-разхищаващи ефекти, той трябва да се използва с повишено внимание, когато пациентите консумират древни алкални диети с високо съдържание на К. Ефектите на подкисляване на урината на фуроземид биха могли да предотвратят елиминирането на K от BK-α/β4 канала, който отделя K в дисталния нефрон при лица, консумиращи алкална диета с високо K Ако съдържанието на Na в диетата също е ниско, фуроземид може да попречи на елиминирането на K от TAL.
ПРЕДОСТАВЯ
Изследванията на този преглед са финансирани от Националния институт по диабет и храносмилателни и бъбречни болести R01 DK-071014 и R01 DK-92474 (S. C. Sansom) и F30 DK-108456 (B. Wang).
ОПОВЕСТЯВАНИЯ
Не се декларират конфликти на интереси, финансови или други, от авторите.
- Проблеми с храненето и здравни ефекти от вегетарианските диети - Крейг - 2010 - Хранене в клинична
- Отрицателни ефекти от дългосрочното хранене с високозърнести диети на лактиращи кози върху производството на млечна мазнина
- PLOS ONE Ефекти на специфични, обогатени с много хранителни вещества диети върху мозъчния метаболизъм, познание и
- Бременността и кърменето имат анти-затлъстяване и антидиабетни ефекти при мишки Aya - Макарова - 2010
- Систематичен преглед и метаанализ на клиничните изпитвания на ефектите от диетите с ниско съдържание на въглехидрати върху