Jeon-Kyung Kim
1 Изследователски център Neurobiota, Факултет по фармация, Университет Kyung Hee, Сеул, Южна Корея
2 Катедра по живот и нанофармацевтични науки, Университет Кюнг Хи, Сеул, Южна Корея
Кюнг-Еон Лий
1 Изследователски център Neurobiota, Факултет по фармация, Университет Kyung Hee, Сеул, Южна Корея
2 Катедра по живот и нанофармацевтични науки, Университет Кюнг Хи, Сеул, Южна Корея
Sang-Ah Lee
1 Изследователски център Neurobiota, Факултет по фармация, Университет Kyung Hee, Сеул, Южна Корея
2 Катедра по живот и нанофармацевтични науки, Университет Кюнг Хи, Сеул, Южна Корея
Хьо-Мин Джанг
1 Изследователски център Neurobiota, Факултет по фармация, Университет Kyung Hee, Сеул, Южна Корея
2 Катедра по живот и нанофармацевтични науки, Университет Кюнг Хи, Сеул, Южна Корея
Донг-Хюн Ким
1 Изследователски център Neurobiota, Факултет по фармация, Университет Kyung Hee, Сеул, Южна Корея
2 Катедра по живот и нанофармацевтични науки, Университет Кюнг Хи, Сеул, Южна Корея
Свързани данни
Данните, генерирани за това изследване, са достъпни при поискване до съответния автор.
Резюме
Въведение
Следователно изолирахме възпалителна Е. coli K1 и противовъзпалителна Lactobacillus mucosae (бивша Lactobacillus reuteri) NK41 от здрава човешка чревна микробиота и изследвахме дали K1 може да причини променена микробиота, колит, когнитивен депресия и мишки и дали NK41 намалява K1- индуцирана променена микробиота, когнитивен спад и депресия при мишки.
Резултати
Ефекти на Escherichia coli K1 и Lactobacillus mucosae NK41 върху активирането на NF-κB в макрофаги
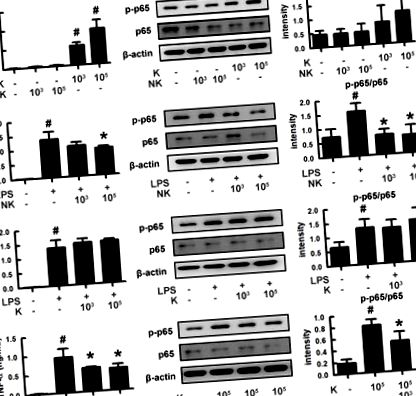
За да разберем как чревните бактерии да регулират появата на психиатрични разстройства, изолирахме чревни бактерии и измерихме възпалителни и противовъзпалителни бактерии от човешки изпражнения (Фигура 1). От тези бактерии K1 мощно индуцирана експресия на фактор на туморна некроза (TNF) -α и активиране на NF-κB в макрофаги, като LPS, докато NK41 не ги засяга. NK41 мощно потиска LPS- или K1-индуцирана експресия на TNF-α и NF-κB активиране в активиран макрофаг. Освен това, NK41 силно затруднява LPS-индуцираната експресия на TNF-α в BV-2 клетки (Фигура S1). K1 и NK41 са идентифицирани като E. coli и L. mucosae въз основа на резултатите от оцветяване по Gram, API 50 CHL Kit (bioMerieux, Сеул, Южна Корея) и 16S rDNA секвениране (ABI 3730XL DNA анализ), съответно.
Ефекти на чревните бактерии K1 и NK41 върху експресията на TNF-α и активирането на NF-κB в макрофаги. (А) Ефекти на NK41 и K1 върху експресията на TNF-α и активирането на NF-kB в макрофаги. (Б) Ефекти на NK41 върху експресията на TNF-α и активирането на NF-κB в LPS-стимулирани макрофаги. (° С) Ефект на K1 върху експресията на TNF-α и активирането на NF-kB в LPS-стимулирани макрофаги. (Д) Ефект на NK41 върху NF-κB активиране в K1-стимулирани макрофаги. Макрофаговите клетки (1 × 106/ml) се инкубират с K1 или NK41 (1 × 10 3 или 1 × 105 CFU/ml) в отсъствие или присъствие на LPS в продължение на 2 часа (за NF-кВ) или 20 часа ( за TNF-a). р-р65 и р65 (NF-кВ) бяха измерени чрез имуноблотинг. TNF-a се измерва чрез ELISA комплект. Стойностите на данните са посочени като средна стойност ± SD (n = 4). # p Фигура 2). K1 при дози 1 × 10 8 и 1 × 10 9 образуваща колония единица (CFU)/мишка/ден показва значително депресивно поведение при EPM и FS задачи (Фигури 2B, C). Поведение, подобно на увреждане на паметта, се наблюдава след лечение с K1 в доза 1 × 109 CFU/мишка/ден в задачата Y-лабиринт (Фигура 2D) K1 в доза 1 × 10 9 CFU/мишка/ден също увеличава инфилтрацията на Iba1 + клетки в хипокампуса. Освен това, K1 причинява NF-κB активиране в хипокампуса, докато експресията на BDNF и CREB фосфорилирането са потиснати (Фигури 2E, F и Фигури S2A, B, S3). Лечението с NK41 обаче не повлиява когнитивния спад в задачите на лабиринта Y-лабиринт и Banes и депресивното поведение в задачата FS, дори при доза 1 × 10 9 CFU/мишка/ден (Фигури 2G – I). NK41 в доза 1 × 10 9 CFU/мишка/ден не повлиява Iba1 + клетъчна популация, активиране на NF-κB и експресия на BDNF в хипокампуса (Фигури 2J, K и Фигури S2C, D, S3).
За да разберем дали NK41 и K1 могат да повлияят на биосинтеза на муцини като MUC1 и MUC2 в червата, ние изследвахме техните ефекти върху експресията на муцин в дебелото черво (Фигура 3Н). Лечението с K1 значително индуцира експресията на MUC2, а не MUC1, докато лечението с NK41 не повлиява експресията на MUC1 и MUC2. Освен това, лечението с NK41 значително потиска експресията на MUC1 и MUC2. Когато дебелото черво на мишките беше оцветено с алцианско синьо, дебелото черво на третирани с K1 мишки беше силно оцветено, проявяващо се с нарушен и съкратен епител (Фигура 3I).
Lactobacillus mucosae NK41 Облекчен Escherichia coli K1-индуциран колит при мишки
Устната сонда на лечение с K1 причинява колит при мишки (Фигура 4). По този начин, лечението с K1 причинява съкращаване на дебелото черво и индуцира активност на миелопероксидазата, експресия на IL-6 и TNF-α и активиране на NF-κB в дебелото черво (Фигури 4A-E). Освен това, лечението с K1 увеличава инфилтрацията на NF-κB +/CD11b + и CD11b +/CD11c + клетки (активирани дендритни клетки [DCs] и макрофаги) в дебелото черво (Фигури 4F, G). Лечението с NK41 значително намалява K1-индуцирано съкращаване на дебелото черво, макроскопски резултат, активност на миелопероксидазата, експресия на IL-6, TNF-α и MUC2, активиране на NF-κB и инфилтрация на CD11b + и/или CD11c + клетки, докато MUC1 е засегнат. Лечението с NK41 също повишава експресията на клаудин-1 и оклудин, потиснат K1 (Фигура 4Е). Освен това, NK41 облекчава индуцираното от K1 увреждане на муциновия слой в дебелото черво.
Дискусия
IL-6, TNF-α и кортикостерон са силно изразени при пациенти с тревожност и депресия (28, 29). Прекомерната експресия на IL-6 и кортикострон се увеличава от стресови фактори като обездвижване и патогенна инфекция чрез активиране на оста HPA. Лечението с терапевтични лекарства за психични разстройства намалява нивата на IL-6 и кортикостерона в кръвта, повишава експресията на BDNF и облекчава невропсихиатричните разстройства (10, 11, 30). Лечението с кортикостерон потиска експресията на BDNF в SH-SY5Y клетки in vitro и при мишки. BDNF индуцира de novo синтез на протеини като синаптофизин и дребрин, които участват в нервната и синаптичната пластичност (31, 32). Освен това системното излагане на LPS активира микроглията и повишената експресия на провъзпалителни цитокини в мозъка на мишки (10, 11). Установихме също така, че орално изследване на Е. coli при мишки причинява ендотоксемия и възпаление на хипокампала. Следователно, индуцираната от Е. coli ендотоксемия може да причини възпаление в мозъка, включително хипокампуса. LPS причинява системно невровъзпаление, което води до увреждане на паметта чрез модулация на NF-κB-медииран BDNF/CREB израз (15, 33). Следователно, регулирането на ендотоксемия-медиирана кортикостерон и експресия на BDNF може да бъде полезно за лечение на психични разстройства.
В заключение, чревната микробиота, която се състои от възпалителни и противовъзпалителни бактерии при хора и животни, е двупосочно свързана с мозъка: свръхрастежът на възпалителни бактерии като Е. coli в стомашно-чревния тракт може да причини психични разстройства с чревни възпаления и превъзходството на противовъзпалителните бактерии като L. mucosae може да облекчи психиатричните разстройства с отслабването на променената микробиота (Фигура 6).
- Интерференция на Bifidobacterium choerinum или Escherichia coli Nissle 1917 със Salmonella
- Програма за медицинско управление на теглото UCLA Център за човешко хранене - Лос Анджелис, Калифорния
- Инвазивни бактерии Салмонелни инфекции - Отслабване
- Метаболитни ефекти на диетите с много ниско съдържание на въглехидрати Неразбраните злодеи на човешкия метаболизъм
- Lactobacillus fermentum и Lactobacillus amylovorus като пробиотици променят телесното затлъстяване и червата