Джон Уинклер
Департамент по биология, IKBSAS, Университет на Британска Колумбия-Окананаган, Канада
Санджой Гош
Департамент по биология, IKBSAS, Университет на Британска Колумбия-Окананаган, Канада
Резюме
Хроничните възпалителни заболявания като диабет нарастват в западния свят. Въз основа на цунамито на нови случаи всяка година трябва да се обмислят нови терапевтични мерки. Обещаващ начин може да включва отслабване на основното възпаление чрез естествени здравни продукти (NHP). Това е така, защото повечето NHPs имат богата история в традиционната медицина и може да се считат за по-безопасни при подходящи дози и условия. Най-голямата пречка в изследванията на NHP обаче е, че тези продукти рядко идват с проверени ползи за здравето или графици за дозиране, установени чрез съвременни научни изследвания. Фулвиновата киселина (FvA), един такъв NHP, идва от хуминови вещества, произведени от микроорганизми в почвата. Традиционната медицина и съвременните изследвания твърдят, че FvA може да модулира имунната система, да повлияе на окислителното състояние на клетките и да подобри стомашно-чревната функция; всички те са отличителни белези на диабета. Този миниревю очертава наличните рецензирани изследвания на FvA и разглежда неговите анекдотични здравни претенции. Ние показваме, че въпреки че наличните изследвания са минимални, има сериозни доказателства за продължаване на изследванията на FvA за предотвратяване на хронични възпалителни заболявания, включително диабет.
1. Въведение
Заболяванията, свързани с хронично възпаление като диабет, сърдечно-съдови заболявания и колит, се увеличават. Например броят на хората, живеещи с диабет в Канада през 2015 г., е 3,4 милиона и се очаква да достигне 5 милиона до 2025 г. [1]. Милиони долари са вложени в разработването на лекарства за лечение на тези заболявания с малък успех [2]. По този начин е време да се проучат нови пътища за лечение и профилактика на хронични възпалителни заболявания. Естествените здравни продукти (NHP) могат да осигурят обещаващ път в това търсене на алтернативи. Първо, те изискват малко или никакво развитие, и второ, те често са придружени от история, богата на традиционната медицина [3]. Фулвиевата киселина (FvA) е публично достъпна NHP, която съчетава тези два факта и може да осигури обещаващи резултати за хронични възпалителни заболявания.
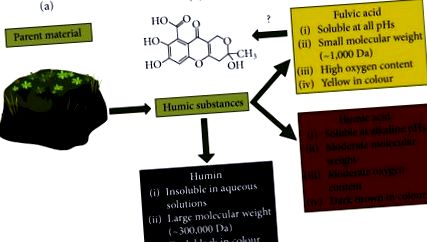
FvA е подклас от различни съединения, известни като хуминови вещества, които са странични продукти от органично разграждане от микроорганизми [4]. Това, което разделя FvA от други хуминови вещества (HS), е набор от физични и химични свойства, показани на фигура 1 (а), посочени от Стивънсън [5] и последвани от Международното общество за хуминови вещества (IHSS; Сейнт Пол, Минесота, САЩ ) [4, 6]. По дефиниция FvAs се състоят от хидрофилни, съдържащи карбоксилни молекули с малко молекулно тегло. Другите HS имат по-високо молекулно тегло и различна разтворимост и съдържание на кислород. Структурата на FvA е предложена от много автори като смес от ковалентно свързани фенолни, хиноидни и бензен карбоксилни съединения [6]. Важно е да се отбележи, че FvA може да се променя в зависимост от географското местоположение. Изходният материал, от който произхожда FvA, влияе върху съдържанието на кислород, азот, ароматен пръстен и въглерод [7]. Например в Израел съдържа FvA, изолиран от глина
2,0% (m/m) азот и FvA, изолиран от пясък, съдържа
4,4% (m/m) азот [7]. Освен това FvA, изолиран от Израел, има
49% (m/m) въглерод, докато FvA от Италия има
39% съдържание на въглерод [7]. Health Canada показва, че FvA е в съответствие със структурата, показана на Фигура 1 (b) [8].
Характеризиране и класификация на хуминовите вещества. Адаптиран от [5]. а) Хуминовите вещества се изолират от различни изходни материали като торф, въглища, вода и почва чрез серия от валежи/разтваряне; техните общи характеристики са подчертани във всяко поле [9, 10]. (б) Предложен състав на фулвокиселина от Health Canada.
FvA се използва непряко в традиционната индийска медицина („Аюрведа“) от около 3000 години [3]. Веществото, наречено Shilajit, катраноподобен ексудат от Хималаите, съдържа около 15–20% FvA и се използва за медицински цели. Според древните текстове Shilajit може да има имуномодулационни, антиоксидантни, диуретични, антихипертензивни и хипогликемични ефекти [3]. Освен това, когато се прилага външно, се твърди, че е антисептик и аналгетик [11]. Отзивите за Shilajit показват, че приемът е безопасен; фармакологичното дозиране на такива молекули обаче остава неизвестно [3]. Въпреки такава липса на информация, Shilajit/FvA в момента е на разположение като хранителен нутрицевтик за обществеността [12]. Целта на този преглед е да изследва и подчертае настоящата база от знания относно FvA и неговите ефекти върху животни и животински клетки.
2. Имуномодулация от FvA
Най-адекватно изследваното твърдение за FvA е способността му да модулира имунната система. Резултатите от подобни проучвания обаче остават противоречиви. FvA може да бъде както възпалително, така и противовъзпалително в животинските системи. Наличната литература относно ефектите на FvA върху имунната система е обобщена на Фигура 2 .
Известна литература за ефектите на фулвовата киселина върху имунната система. Показано е, че фулвиновата киселина предизвиква, както и намалява възпалението.
2.1. Противовъзпалителни ефекти на FvA
Астмата, алергиите и екземата, заедно с много други нарушения, могат да бъдат свързани със свръхактивни имунни клетки [13]. В тези случаи противовъзпалителните лекарства са от решаващо значение за намаляване на симптомите. Няколко проучвания показват, че FvA може да действа като противовъзпалително чрез намаляване на освобождаването на провъзпалителни медиатори от клетките. Първо, Junek et al. показват, че FvA при 200 μg/ml може да намали експресията на тумор некрозис фактор алфа (TNF-α) след излагане на ендотоксин липополизахарид (LPS) в диференцирани човешки моноцити (U937) [14]. Също така е показано, че FvA намалява секрецията на циклооксигеназа 2 (COX2) и простагландин Е2 (PGE2) след хомоцистеинова стимулация в първични човешки моноцити [15]. Показано е, че FvA от разтворена утайка (SS-FA) намалява B-хексозаминидазата и освобождаването на хистамин в имуноглобулин-Е-чувствителни мастоцити и базофилни клетки [16]. Тази информация предполага, че FvA може да има противовъзпалителни и антиалергични ефекти. Yamada et al. също показват, че SS-FA намалява TNF-α, интерлевкин-4 (IL-4) и IL-13 от мастоцитите.
За съжаление проучванията in vivo за ефектите от FvA са твърде малко и са спорадични. Пилотно клинично проучване показва, че FvA (оксифулвинова киселина), получен от въглища, при 4,5% (тегл./Тегл.) Намалява размера на пшеницата и изгарянето след предизвикване на алерген при хората [17]. Намаляването с FvA показва сходни резултати с 1% хидрокортизон. Противовъзпалителните свойства на оксифулвиковата киселина са показани и при мишки [18]. В проучването мишките, сенсибилизирани с динитрофлуоробензол в ухото и след това отново предизвикани 6 дни по-късно, виждат намаляване на отока при лечение с FvA, сравнимо със стероидното лекарство. Патентована процедура за изолиране, при която се получава фулвокиселина, получена от въглехидрати (CHD-FvA), имитира почти изцяло горната информация. В рандомизирано клинично проучване е показано, че локалното приложение на CHD-FvA значително намалява екзема при хора [19]. В това проучване обаче се съобщава и за усещане за парене. В допълнение, пероралното поглъщане на CHD-FvA, изолиран от Южна Африка при 100 mg/kg, може да намали отока на лапите при плъхове на нива, подобни на нестероидните противовъзпалителни лекарства [20]. Като цяло, горните проучвания обещават потенциала на FvA за лечение на свръхактивни имунни нарушения, по-специално екзема.
2.2. Провъзпалителни ефекти на FvA
2.3. Вредни имунни ефекти на FvA
Няколко проучвания показват, че FvA може да бъде и вреден. FvA, получен от унгарски лигнит, може да активира хуморален имунитет и да намали функцията на щитовидната жлеза при плъхове [26]. В това проучване FvA увеличава титъра на антителата срещу овалбумин 14 дни и 26 дни след предизвикване. Те също така показват, че диаметърът на лимфоцитите се увеличава при плъхове, знак за клетъчно активиране [26]. Тези резултати не са изолирани; Kunavue и Lien показват повишаване на IgG антителата при отбиване на свине след лечение с FvA [27]. Не се установява значително увеличение на броя на лимфоцитите, моноцитите или гранулоцитите в кръвта. За съжаление Kunavue и Lien не споменават местоположението и процедурата за изолиране на използвания FvA.
Такива противоречиви ефекти изглежда са резултат от различията в терапевтичните дози и/или произхода на FvA в проучването. По този начин е абсолютно необходимо да се установи безопасно дозиране на FvA в зависимост от неговия източник, за да се лекуват/предотвратяват имуномодулаторни нарушения.
3. Оксидативен стрес
Оксидативният стрес е тясно свързан с хронични възпалителни заболявания [28]. Оксидативният стрес се описва като дисбаланс на силно реактивни кислородни видове (ROS) в сравнение с антиоксидантите [29]. Когато клетъчното равновесие се измести към по-висока ROS, ендогенните антиоксиданти като глутатион (GSH) и супероксиддисмутаза (SOD) са надминати. Това води до клетъчна дисфункция, липидна пероксидация и възможна клетъчна смърт [30]. Ефектите на FvA върху окислителното състояние в клетките и животните са обобщени на Фигура 3 .
Известна литература за ефектите на фулвовата киселина върху редокс състоянието на клетките. Показано е, че фулвиновата киселина има различни ефекти, които включват увеличаване на оксидативния стрес, но също така и намаляването му.
3.1. Антиоксидантни способности на FvA
Доказано е, че FvA изолира супероксидните радикали и други ROS извън клетката [31]. Вътре в клетката обаче FvA може да раздели електронно-транспортната верига в чернодробните митохондрии, което е свързано с намаляване на производството на ROS [32]. В допълнение, най-обещаващото in vivo проучване относно антиоксидантната способност на FvA е намаляването на маркерите на оксидативен стрес след индуциране на изопротеренол (ISO) на миокардно увреждане при плъхове. Shikalgar и Naikwade показват, че FvA при 300 mg/kg/ден в продължение на 4 седмици намалява липидната пероксидация и маркерите за увреждане на миокарда след ISO и значително повишава нивата на GSH, SOD и каталаза (CAT) [33]. Друго проучване потвърждава тази информация при рибите. След хранене с FvA в продължение на 60 дни се наблюдава намаляване на липидната пероксидация и увеличаване на експресията на SOD, CAT и глутатион пероксидаза (GPx) [34].
3.2. Оксидантни способности на FvA
Точно както при възпаление, FvA също може да причини окислително увреждане, вместо да го предотврати. FvA увеличава оксидативния стрес, когато е изложен на изолирани хрущялни клетки от 12-дневни ембрионални пилета [35]. Това проучване контрастира с тези, показващи намаляване на липидната пероксидация и допълнително предполага FvA като причинителен фактор за болестта на Kashin-Beck. Основен фактор за повишен оксидативен стрес е, че FvA може да увеличи честотите на клетъчно дишане при продължителна експозиция в митохондриите на плъхове, което може да доведе до производството на повече кислородни радикали [30]. Доказано е, че FvA увеличава окислителните маркери като водороден прекис и азотен оксид и индуцира апоптоза в клетъчните линии на рак на черния дроб [36]. По същия начин FvA може да увеличи контракциите на гладката мускулатура, което може да бъде свързано с окислително увреждане [37].
4. Здраве на червата
Червата образуват интерфазата на външния свят, микробиома и гостоприемника. Достатъчно доказателства показват, че лошото здраве на червата може да доведе до възпаление и заболявания [38]. В селското стопанство е доказано, че FvA влияе върху състава на почвените микроби и може да се конюгира с различни минерали, подпомагайки усвояването в растенията [39, 40]. В резултат на това се препоръчва FvA да подобри чревната флора, усвояването на хранителни вещества и да излекува неблагоприятни нарушения, свързани с червата. По-долу е наличното съдържание относно ефектите на FvA върху здравето на червата и обобщено на Фигура 4 .
Известна литература за ефектите на фулвовата киселина върху здравето на червата. Доказано е, че фулвиновата киселина влияе върху микробиома, абсорбцията на хранителни вещества и чревните разстройства.
4.1. Преместване на микробиотата
По отношение на микробиотата има много малко информация при животните. Изследване на Gao et al. показват, че FvA при 1,5% (тегл./тегл.) може да модулира чревната микрофлора при риби от мох (Paramisgurnus dabryanus) [34]. След 60 дни хранене, изобилието от Proteobacteria phyla намалява и нивата на Firmicute се увеличават в червата. В допълнение, 10 бактериални рода са повлияни от лечението с FvA. Забележителните бактерии включват увеличаване на Variovorax, Lactococcus и Lactobacillus и намаляване на Serratia и Acinetobacter. Това е единственото проучване, изследващо ефекта на FvA върху микробиома.
4.2. Подобряване на абсорбцията на хранителни вещества
Gao et al. [34] показват също, че FvA повишава активността на храносмилателните ензими като лизозим, протеази и киселинни/алкални фосфатази в рибите. Това се засилва отчасти чрез интензивно проучване, изследващо смилаемостта на хранителните вещества при свинете [27]. FvA, добавен при 200 ppm в храната, подобрява храносмилането на фосфор и пепел, но интересно е, че не оказва влияние върху смилаемостта на мазнините и протеините, контрастни данни, открити в хляба.
Показано е, че FvA влияе върху бионаличността на тежки метали и при животински модели. FvA може да увеличи абсорбцията на мед в свинските яйцевидни епителни клетки и едновременно с това намалява нейната токсичност [41]. В допълнение към хранителните вещества е доказано, че FvA посредничи при доставката на лекарства и при плъхове [42]. Карбамазепин (CBZ), често срещан антиконвулсант, има ниска бионаличност, но когато се конюгира с FvA, абсорбцията през извечна чревна торбичка на плъх се увеличава заедно с концентрациите на CBZ в кръвната плазма. Доказано е, че FvA увеличава усвояването на хранителни вещества и лекарства; по този начин, загриженост представлява абсорбцията на замърсители и токсини в кръвта. Въпреки това, в проучване на Qiang et al., FvA не увеличава абсорбцията на перфлуороктансулфонат (PFOS) в шараните, заключение, основано на количеството PFOS в изпражненията на рибата в сравнение с контролите [43].
4.3. Подобрете чревните разстройства
Съществува предварително клинично проучване, което изследва ефикасността на пробиотиците в комбинация с FvA при стомашно-чревни (GI) нарушения [44]. За съжаление обаче всички групи, включително тези с FvA, не виждат подобрение в индекса за качество на стомашно-чревния живот (GIQLI) и визуалната аналогова скала (VAS) за симптоми на GI. Това проучване показва безопасността на приема на FvA за период от 12 седмици. Въпреки че FvA не е показал ефект в предишното проучване, FvA, изолиран от Shilajit, показва обещание да бъде антиулцерогенен по време на няколко теста на батерията при плъхове албиноси [45].
5. Потенциал на FvA при диабет
Захарният диабет тип 2 (T2DM) се характеризира с неправилно сигнализиране за инсулин и отслабено поемане на глюкоза в клетките [46]. Това може да доведе до продължителна хипергликемия след хранене и неблагоприятни симптоми [46]. Причината за диабета остава загадка, но изследванията свързват възпалението, оксидативния стрес и промените в чревния микробиом сред многото причиняващи фактори [47]. Показано е, че Shilajit, който съдържа FvA, намалява хипергликемията при плъхове с диабет и увеличава активността на SOD в бета-клетките на панкреаса [48, 49]. За съжаление обаче няма преки доказателства на английски език, показващи само FvA за предотвратяване на симптомите на T2DM. Въпреки това, натрупващите ефекти, подчертани в този преглед и последните две проучвания, предполагат терапевтичния му потенциал.
Тези с T2DM показват признаци на хронично възпаление и повишени проинфламаторни цитокини в серума като TNF-α, IL-1 и IL-6 [47]. Показано е, че FvA намалява тези видове цитокини и провъзпалителни маркери в животински модели [14, 16]. В допълнение, предложен режим на лечение на T2DM включва нестероидни противовъзпалителни лекарства (НСПВС) за облекчаване на симптомите [50]. FvA може да се побере като допълнително лечение за намаляване на маркерите на оксидативен стрес и възпаление, тъй като FvA може да действа по подобен начин на НСПВС [20]. FvA може също да намали окислителните щети и да увеличи антиоксидантните ензими като SOD, CAT и GPx [33]. Бета клетките, които са отговорни за производството на инсулин, претърпяват окислително увреждане по време на T2DM [51]. Защитата на редокс състоянието на бета клетките може да се окаже полезна за предотвратяване на T2DM. И накрая, пациентите с T2DM се откриват с промяна в чревния микробен състав и FvA може да повлияе на бактериалната общност [34].
6. Заключения
Информацията, събрана в този преглед, показва, че FvA може да действа като имунен модулатор, да повлияе на редокс състоянието и потенциално да повлияе на здравето на червата. Показано е, че FvA намалява проинфламаторните маркери, но също така активира имунната система, за да убива бактериите. Доказано е, че намалява оксидативния стрес и дори индуцира апоптоза в чернодробните линии на рак. Показано е, че FvA също влияе върху микробиома и евентуално подобрява функцията на червата. FvA изглежда има ин-ян ефект, когато става въпрос за тези физиологични състояния. Тази тенденция може да се забележи при повечето лекарства и НХП; токсичността обаче може да се прояви при висок прием и лошо приложение [52, 53].
Въпреки че подкрепящата литература е минимална, ако се разглежда в комбинация, възниква потенциалът FvA да бъде кандидат за предотвратяване на възпалителни заболявания като диабет. Това е обещаващо, тъй като сегашният ни подход към тези видове заболявания липсва. Важно е да се отбележи, че изследванията на FvA в някои случаи са противоречиви, което се смята за резултат от отклонение в дозировката, изходния материал и процедурата на изолиране. Освен това няма консенсус относно структурата на FvA, стандартна изолация или изходен материал. По този начин е от първостепенно значение да се съчетаят тези фактори и да се установи дозиране за възрастови групи и различен FvA. Това ще помогне да се направят убедителни изявления относно функцията на FvA и нейното влияние върху имунните заболявания.
Благодарности
Авторите биха искали да признаят на членовете на лабораторията Ghosh и на лабораторията Gibson от Университета на Британска Колумбия за техните съвети и постоянна подкрепа.
Конфликт на интереси
Авторите заявяват, че няма конфликт на интереси по отношение на публикуването на тази статия.
- Урзоловата киселина показва обещаващ терапевтичен потенциал, но са необходими повече доказателства за корейски преглед
- Урсодезоксихолова киселина, хелатиращи агенти и цинк при лечението на метаболитни чернодробни заболявания
- Топ 10 ползи за здравето на фулвовата киселина за жени; s Wellbeing MAHALO Грижа за кожата
- Терапевтичен потенциал за насочване на метаболизма на водородния прекис при лечението на мозъчна исхемия
- Най-добрият хляб за хора с диабет