Резюме
ЗАДЕН ПЛАН:
Алкохолното чернодробно заболяване (ALD) е свързано с висок риск от заболеваемост и смъртност. Недохранването придружава това състояние и може да бъде едновременно последица и допринася за патологията. Много проучвания са изследвали ползите от осигуряването на допълнително хранене при лечението на пациенти с ALD. Настоящото проучване представлява мета-анализ на наличните доказателства.
МЕТОД:
Мета-анализ на рандомизирани контролирани проучвания, сравняващи хранителни добавки плюс нормална болнична диета спрямо диета самостоятелно.
РЕЗУЛТАТИ:
Идентифицирани са седем рандомизирани контролирани проучвания, включващи 262 пациенти с ALD. Сборен анализ не разкрива статистическа разлика в смъртността между групите, на които е приложена специална хранителна терапия, спрямо нормална балансирана диета (OR 0,80 [95% CI 0,42 до 1,52]). В допълнение, храненето не подобрява значително асцит (OR 1.29 [95% CI 0.52 до 3.20]) или каквито и да е биохимични параметри. Енцефалопатията обаче показва значително подобрение или разделителна способност (OR 0,24 [95% CI 0,06 до 0,93]).
ЗАКЛЮЧЕНИЕ:
Хранителните добавки не осигуряват полза за смъртността при пациенти с ALD и нито асцитът, нито биохимичните параметри се подобряват значително. Въпреки това енцефалопатията е значително подобрена и следователно хранителните добавки трябва да бъдат насърчавани в тази обстановка.
Продължи
ИСТОРИКА:
L’hépatopathie alcoolique (HPA) s’associe à un risque élevé de morbidité et de mortalité. Elle s’accompagne de недохранване, laquelle peut être à la fois une conséquence et un élément вноска на патология. De nombreux essais ont porté sur les avantages des suppléments dietnels pour la prendre en charge. La présente étude est une méta-analysis des données probantes accessibles.
МЕТОДОЛОГИЯ:
Méta-анализ на d’essais aléatoires et contrôlés comparant un régime seul aux suppléments nutritionnels associés à un régime normal chez les bolniki hospisés.
РЕЗУЛТАТИ:
Les chercheurs ont repéré sept essais aléatoires et contrôlés portant sur 262 пациенти, различни от HPA. L'analyse groupée n'a révélé aucune différence statistique du taux de mortalité entre les groups ayant reçu une thérapie dietnelle spéciale et ceux ayant reçu un régime équilibré normal (RRR 0,80 [95% IC 0,42 à 1,52]) . En outre, les suppléments n’amélioraient pas les ascites (RRR 1,29 [95% IC 0,52 à 3,20]) или les paramètres biochimiques de manière significative. Независим, les cas d’encéphalopathie so sontriebementment atténués ou se sont resolus (RRR 0,24 [95% IC 0,06 à 0,93]).
ЗАКЛЮЧЕНИЕ:
Les suppléments nutritionnels n’avaient aucun avantage sur le taux de mortalité dans les d’HPA, et les les ascites ni les paramètres biochimiques ne se sont améliorés de manière significative. Cependant, les cas d’encéphalopathie se sont sigérablement atténués. Par conéquent, il faut стимулиращ l’administration de suppléments dietnels dans ce context.
Алкохолното чернодробно заболяване (ALD) обхваща спектър от чернодробни заболявания, които започват с мастен черен дроб и могат да прогресират до хепатит и фиброза и в крайна сметка до цироза. Докато повечето случаи на затлъстяване на черния дроб са обратими при спиране на алкохола, алкохолният хепатит може да се обърне, а смъртността, свързана с тежка ALD, е висока (1–3). Следователно, необходимостта от специфично лечение е оправдана и към днешна дата не е установено, че конкретно лечение има значително въздействие върху заболяването (1,3). Повечето проучвания са фокусирани върху стероиди и пентоксифилин, които могат да осигурят умерена полза при тежки случаи (4–6); обаче опасенията относно токсичността и ограничената ефикасност ограничават общото им приложение в клиничната практика (6,7). Като цяло, хранителната подкрепа получи широко признание при лечението на пациенти с алкохолен хепатит (7), но цялостният му ефект върху резултата остава несигурен.
Пациентите с алкохолен хепатит обикновено са анорексични и недохранени, тъй като заместват калориите от храната с калориите от алкохола. Тези пациенти също развиват малабсорбция от намалено производство на жлъчка от засегнатия черен дроб, оток на червата от ниско ниво на албумин, механично нарушаване на чревната стена и хроничен панкреатит, който е често срещан при тази популация (8,9). Предполага се, че недохранването, придружаващо алкохолизма, също може да допринесе за увреждане на черния дроб (10). Това може да се обясни с увреждане на свободните радикали и повишен риск от инфекция, които се появяват поради липсата на антиоксиданти, главно витамини и аминокиселини (9,10). Следователно, изглежда логично, че освен спирането на алкохола, хранителната подкрепа трябва да бъде от полза при лечението на ALD. Хранителната подкрепа е проучена в няколко контролирани и неконтролирани клинични проучвания, за да се оцени нейният благоприятен ефект (9-11). Тези проучвания дадоха различни резултати и силата на контролираните проучвания е ниска. Целта на настоящия систематичен преглед беше да се оценят ефектите от хранителната подкрепа при пациенти с алкохолен хепатит, със или без цироза, по отношение на смъртността и други параметри.
МЕТОДИ
Статистически анализ
МАСА 1
Характеристики и съпоставимост на включените рандомизирани контролирани проучвания
| Насрала и Галамбос (18), 1980 | 35 (18 контрол, 17 проучвания) | 28 | Аминокиселини, MVI | Интравенозно | Болнична диета |
| Naveau et al (19), 1985 | 37 (19 контрол, 18 проучвания) | 28 | 40 kcal/BW, MVI, глюкоза, мазнини, аминокиселини | Интравенозно | Болнична диета |
| Calvey et al (17), 1985 | 64 (22 контролни, 21 конвенционални протеини, 21 BCAA формула) | 21. | 2000 kcal, въглехидрати, MVI, 65 g протеин срещу 25 g BCAA + 40 g протеин | Перорално или интравенозно (ако не е възможно орално) | Болнична диета |
| Achord (22), 1987 г. | 28 (14 контрол, 14 проучвания) | 21. | 860 kcal, аминокиселини | Интравенозно | Болнична диета |
| Саймън и Галамбос (20), 1988 | 31 (17 контролни, 14 проучвания) | 28 | Декстроза, аминокиселини, липиди, MVI | Интравенозно | Болнична диета |
| Bunout et al (23), 1989 | 36 (19 контрол, 17 проучвания) | 28 | 50 kcal/BW, декстроза, казеин (протеин), липиди | Устно | Болнична диета |
| Kearns et al (21), 1992 | 31 (15 контрол, 16 проучвания) | 28 | 167 kJ/kg, 1,5 g протеин/kg | Устно | Болнична диета |
BCAA аминокиселини с разклонена верига; BW телесно тегло; MVI Мултивитамини
Качество на включените изследвания
Качеството на изследванията е хетерогенно. С изключение на едно проучване, всички проучвания бяха заслепени, вероятно защото за наблюдателите беше очевидно, че участниците се различават в управлението на хранителните си качества. Във всички проучвания се съобщава за рандомизация; обаче само три проучвания описват техния метод на рандомизация, който изглежда адекватен. Сравненията между изходните характеристики на изследваните групи бяха описани във всички опити и бяха сходни. Отпадане на участниците е настъпило във всички проучвания с изключение на едно, с описани причини: най-вече поради неспазване на диетата и усложнения на терапията или на централната венозна линия. Отпадналите пациенти не са включени в нито един анализ на проучването.
Смъртност
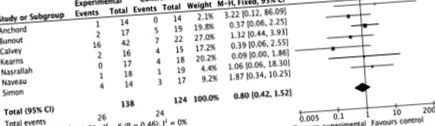
Сборен анализ на седемте проучвания не разкрива статистическа разлика в смъртността между двете групи (OR 0,80 [95% CI 0,42 до 1,52]) (Фигура 1). Повторните анализи с изключените опити показват подобен резултат. Причини за смъртност са докладвани във всички проучвания, с изключение на едно, и изглежда са сходни между изследваните групи. Основните причини са влошаване на чернодробната недостатъчност, стомашно-чревно кървене, хепатореналния синдром и инфекция/сепсис, включително спонтанен бактериален перитонит. Графиката на фунията за регистрите на ИЛ от включените опити не демонстрира асиметрия (Фигура 2).
Смъртност на пациенти с алкохолно чернодробно заболяване от седем рандомизирани клинични проучвания за оценка на допълнителното хранене по време на хоспитализация
Фуния на включени опити
Заболеваемост
В трите проучвания, които сравняват клинични прояви, допълнителното орално или интравенозно хранене не подобрява значително асцита (OR 1,29 [95% CI 0,52 до 3,20]). От друга страна, трите проучвания, които оценяват степента на енцефалопатия, показват значително подобрение или разрешаване с хранителни добавки (OR 0.24 [95% CI 0.06 до 0.93]). Тези проучвания оценяват клинично степента на енцефалопатия и не прилагат лактулоза или антибиотици като лечение. Пациентите в тези проучвания, за които е установено, че имат енцефалопатия при рандомизиране, са преоценени в края на проучването и е документирана промяна на статуса. Някои проучвания сравняват общия брой пациенти с енцефалопатия преди и след рандомизацията. Решено е да не се включват тези проучвания, тъй като не са оценени индивидуални промени в енцефалопатията. За отбелязване е, че в две от шестте проучвания, при които допълнителното хранене се дава интравенозно, се съобщава свързана с катетър бактериемия. Naveau et al (19) откриват положителни кръвни култури при четири от 18 интравенозно лекувани пациенти.
Биохимични резултати
С изключение на едно проучване, тестовете за чернодробна функция и други биохимични маркери бяха измерени и сравнени между групите през периода на изследването. Въпреки че имаше тенденция към подобрение с хранителни добавки, тези резултати не бяха значителни. Шест от седемте проучвания сравняват промените в нивата на билирубин (P = 0,38), пет проучвания сравняват нивата на албумин (P = 0,52), четири проучвания сравняват нивата на алкална фосфатаза (P = 0,18) и три проучвания сравняват нивата на аланин трансаминаза и аспартат трансаминаза ( P = 1,0 и P = 0,40, съответно) (Фигура 3).
Скатерни графики, сравняващи промяната в няколко биохимични маркера преди и в края на изследването, между контролната група (•) и експерименталната група (▪). Линиите в разпръснатия график представляват средната стойност и SEM. Предоставена е стойността P. ALT Аланин аминотрансфераза; AST Аспартат аминотрансфераза
ДИСКУСИЯ
Трябва да се отбележи, че други проучвания демонстрират явните ползи от храненето за пациенти с цироза и други форми на чернодробно заболяване върху оцеляването, престоя в болница и заболеваемостта (24,25). В голямо рандомизирано многоцентрово проучване 622 пациенти с цироза с различни причини са били произволно назначени да получават аминокиселини с разклонена верига (BCAA) само с диета спрямо диета (25). Резултатите от това проучване, което беше най-голямото от този вид, показаха значително намаляване както на смъртността (P = 0,015), така и на чернодробните усложнения, включително асцит, оток и енцефалопатия, посочени от значително увеличение на албумина (P = 0,018) и по-ниски средни нива на амоняк в кръвта. Дали тази намеса е полезна при ALD не е видно от нашия мета-анализ, но нито популацията, нито размерът на извадката са подобни. По същия начин, от включените ни проучвания, Calvey et al (17) изследва употребата на BCAA, но също така не успява да покаже каквато и да е полза от смъртността спрямо конвенционалната терапия с протеини или диета. Това проучване обаче показа, че BCAA подобрява/решава чернодробната енцефалопатия и нормализира азотния баланс повече от конвенционалната протеинова или диетична терапия.
Ограничение на нашето проучване е фактът, че проучванията включват или ентерална, или парентерална хранителна подкрепа в сравнение с нормална болнична диета. Съставът на експерименталната диета обаче е сходен за различните групи, тъй като включва смес от аминокиселини или протеини и въглехидрати. Четири RCT добавиха мултивитамини към режима, но е малко вероятно това да обърка общите резултати. Важно е, че на всички контроли и субектите беше предложена нормална, изходна болнична диета и периодът на проследяване беше разумен за краткосрочна смъртност. Липсват обаче данни за дългосрочна смъртност.
Нашите резултати показаха, че допълнителната хранителна терапия подобрява чернодробната енцефалопатия (OR 0.24 [95% CI 0.06 до 0.93]). В миналото основата на лечението на енцефалопатия беше да се ограничи количеството протеин в диетата - теоретично, да се ограничи количеството на дезаминиране на протеина до ароматни аминокиселини и натрупване на амоняк (26). Въпреки това, по-скорошни проучвания демонстрират благоприятния ефект от осигуряването на адекватни количества протеин по време на енцефалопатия (27) и евентуално доставяне на увеличени количества протеин, за да се поддържа положителен азотен баланс, ако е недохранван (28). Това доведе до 1997 г. Европейското общество за парентерално и ентерално хранене публикува консенсусни насоки, препоръчващи дневният прием на протеин при пациенти с чернодробно заболяване, ако е възможно, да бъде приблизително 1,0 g/kg до 1,5 g/kg в зависимост от степента на чернодробна декомпенсация ( 29). Рандомизирано проучване на пациенти с цироза с енцефалопатия през 2003 г. (30) не съобщава за разлика между даването на диета с ниско спрямо високо протеини по отношение на разрешаването на енцефалопатията или смъртността, но групата с ниско съдържание на протеини показва по-високо разграждане на протеините.
Не е добре разбрано защо диетата с високо съдържание на протеини може да бъде полезна при енцефалопатия, особено защото патофизиологията на енцефалопатията остава неясна; амонякът и свръхпроизводството на други невротоксини обаче е добре приета теория (31,32). В резултат на нарушена чернодробна функция са необходими други пътища за изчистване на амоняк. Един от начините е превръщането на амоняк в глутамин чрез мускули (9). Неотдавнашно проучване, включващо плъхове с остра чернодробна недостатъчност и произтичащите от това повишения на нивата на амоняк, демонстрира повишено производство на глутамин от скелетните мускули. Това предполага, че запазването на мускулната маса чрез по-добро хранене може да бъде от полза за предотвратяване или подобряване на чернодробната енцефалопатия и произтичащите от това усложнения при пациенти с ALD (33). Нашите резултати и други данни показват, че не само диетата с високо съдържание на протеини може безопасно да се прилага при пациенти с цироза с енцефалопатия, но също така може да бъде полезна за подобряване или разрешаване на чернодробната енцефалопатия.
ЗАКЛЮЧЕНИЕ
Недохранването може да бъде фактор, допринасящ за заболеваемостта и смъртността на пациентите с ALD. Нашият мета-анализ на седем проучвания, изследващи допълнителни хранителни добавки в продължение на три до четири седмици, разкрива незначително намаляване на смъртността. Нито асцитът, нито параметрите на чернодробната функция се подобриха с високо протеиновата и висококалоричната диета. Въпреки това, при пациенти с енцефалопатия се наблюдава значително намаляване на степента или разделителната способност. Тези доказателства допълнително защитават безопасността и важността на осигуряването на адекватно хранене, включително протеини, при ALD и чернодробна енцефалопатия и подкопават концепцията за ограничаване на протеина при тези пациенти.
Бележки под линия
ОПОВЕСТЯВАНИЯ: Авторите нямат финансови оповестявания или конфликти на интереси, които да декларират.
ПРИНОСИ: Рами Антар: Систематичен преглед и избор на статии, събиране и анализ на данни, изготвен ръкопис Фил Уонг: Дизайн на изследването, критична ревизия, надзор на изследването Питър Гали: Дизайн на изследването, систематичен преглед и избор на статии, надзор на проучването
- Biotype Diets System® Кръвни групи и хранителни алергии Journal of Nutritional & Environmental
- 6 Хранителни добавки и храни, които могат да подобрят вашата здравословна храна US News
- 6 малки хранения за по-добро управление на диабета
- Относно Nutrition Response Testing® Ulan Nutritional Systems
- Относно вирусен хепатит А инфекция; Блог за хранителни болести по хепатит