Резюме
Анатомичните доказателства при няколко вида показват силно хетерогенно разпределение на мазнините в предсърдния и камерния миокард. Предсърдните придатъци имат мастни натрупвания и още повече в задното ляво предсърдие. Въпреки че такова разпределение на мазнините се счита за нормално, мастната инфилтрация се счита за аритмогенна и различни сърдечни патофизиологични състояния показват излишни натрупвания на мастна тъкан в миокарда, особено в епикарда. Представени са хипотези за физиологичната и патофизиологичната роля на епикардната мазнина, но този проблем е слабо разбран. Следователно, този мини-преглед ще се фокусира върху разпределението на мазнините в епикарда и (пато) -физиологичните последици от това разпределение. Разглеждат се и потенциалните молекулярни механизми, които могат да задвижат структурно и електрическо ремоделиране на миокарда, съпътстващо мастната инфилтрация на сърцето.
Мастна тъкан на миокарда
Приблизително 80% от миокардната повърхност е покрита с мазнини и се смята, че
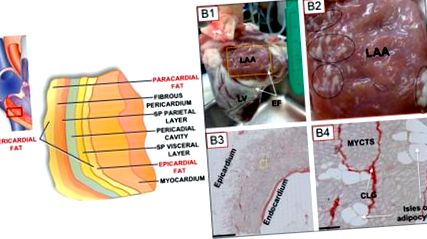
(А) Схема на депата на миокардната мастна тъкан в миокардната стена на дясната камера (Променено от Wong et al., 2016). (Б) Разпределение на епикардната мастна тъкан в сърцето на овцете. (Б) Нормално сърце за възрастни овце, показващо предсърдни и камерни епикардни мастни натрупвания. LAA, ляво предсърдно придатък; LV, лява камера; EF, епикардна мазнина, върху предсърдни и вентрикуларни повърхности. Жълта кутия в (B1) е 2 × 3 cm. (B2), [Вмъкване на кутия от (B1)] Овалът и кръговете представляват области с гъста предсърдна епикардна мазнина. (B3), LAA тъканна секция. Обърнете внимание на значителен епикарден мастен слой с обширна инфилтрация на адипоцити в предсърдния мускул (скала; 1 mm). (B4), Тъканна част на регион близо до жълта вложка в (B3), показва миоцити (MYCTS), острови на адипоцити и колаген (CLG; Picoserius оцветяване). Скала: 50 μm. (Променено от O'Connell et al., 2015).
Хистологичният анализ на секционирането на тъкани е предоставил важна информация за инфилтрацията на мазнини в миокарда. По този начин е известно, че на повърхността на предсърдията и вентрикулите има обширни мастни натрупвания (още повече за последните; Фигури 1В, В1). Както е показано на тази фигура, Фигура 1В, 1В, значителни мастни натрупвания присъстват в предсърдния миокард (Фигури 1В, В2), а адипоцитите са съседни на миоцитите, без данни за фасция, отделяща всеки тип тъкан, за разлика от това се наблюдава в скелетните мускули (Iacobellis et al., 2005; Hatem and Sanders, 2014). Адипоцитите експресират йонни канали, включително междинни съединителни канали (Burke et al., 2014), но има малко или нищо известно за електрическото свързване на адипоцити/миоцити. Съответно на дискусиите в този преглед, тази близост между адипоцити и миоцити, както и физическата близост между адипоцити/миоцити с други клетъчни типове, лесно позволява модулиращи ефекти на адипоцитните биофактори върху миоцитите. Очаква се такъв сценарий да има дълбоки последици за миокардната функция и патофизиологичното клетъчно ремоделиране.
Характеристики на депата на мастната тъкан при миокардни заболявания
Анализи на импулсната проводимост при нормално тегло и при затлъстели овце (Измервания по време на синусов ритъм и изохрони от лявата предна коса). (А) Представителни 5 ms изохронни карти. Обърнете внимание на струпването на изохрони (т.е. по-бавно време на разпространение) в затлъстелите овце в сравнение с контролата. (Б) Средни стойности на скоростта на проводимост, измерени в определените области на лявото предсърдие. Обърнете внимание, че скоростта на проводимост е намалена равномерно във всички области на предсърдния миокард. АНТ, преден; LA, ляво предсърдие; INF_LA, долно ляво предсърдие; LAT_LA, странично ляво предсърдие; POS_LA, задно ляво предсърдие; ROO_LA, ляв предсърден покрив; SEP_LA, преградно ляво предсърдие. Променено от Mahajan et al. (2015).
При затлъстели хора и животински модели има излишна мазнина в периатрията, както и мастна инфилтрация в миокарда. Освен това, при затлъстяване, миокардните клетки имат повишено съдържание на мазнини, което е отговорно за съпътстващата липотоксична кардиомиопатия. Предполага се, че комбинация от фактори, включително други съпътстващи заболявания, свързани със затлъстяването, са отговорни за генерирането на субстрати, които благоприятстват аритмогенността, и чрез механизми като посочените по-горе. Ролята на излишните миокардни мазнини, при липсата на други рискови фактори, стана интересна в редица лаборатории (Hatem et al., 2016; Pandit et al., 2016).
Свързани с болестта миокардни фибро-мастни инфилтрации (Мастни инфилтрации, черни звездички; фиброза, черни или бели кръстове). (А) Предсърдно мъждене (модифицирано от Haemers et al., 2015). (Б) Миотонична дистрофия (увеличение, 100X) (модифициран от Christensen et al., 2008). (° С) Миокарден инфаркт (модифициран от Pouliopoulos et al., 2013). (Д) Аритмогенна дяснокамерна кардиомиопатия (увеличение, 200Х). (Променено от Deshpande et al., 2016).
Общопризнато е, че аритмогенността включва взаимодействия на спусъка в комбинация със субстрат (Iacobellis et al., 2005; Sacks and Fain, 2007; Cherian et al., 2012; Hatem and Sanders, 2014; Heijman et al., 2014; Pandit и др., 2016). Текущите изследвания са насочени към разбиране на ролята на излишното затлъстяване, особено по отношение на основните сигнални механизми, при формирането на такива тригери и субстрати. Тези изследвания разглеждат няколко важни въпроса, които остават без отговор. Например, какви са относителните роли на различните сигнални пътища, като например автокринните, паракринните и вазокринните пътища? (Sacks and Fain, 2007). Съществува и въпросът за източника на адипоцитите/мастната тъкан, които инфилтрират миокарда при тези болестни състояния. Освен това, кои процеси инициират инфилтрация на миокарда и какви са молекулярните сигнални събития, свързани с процеса на иницииране? (Chilukoti et al., 2015; Pandit et al., 2016). Разбирането на такива процеси и определянето на ключови молекулярни участници е необходимо за предлагане на нови терапевтични подходи за лечение на тези заболявания.
Потенциални клетъчни и молекулярни механизми на индуцирано от мастната тъкан ремоделиране на миокарда
Както беше отбелязано по-рано в различни доклади (Iacobellis et al., 2005; Cherian et al., 2012; Hatem and Sanders, 2014; Pandit et al., 2016), адипоцитите и други различни клетъчни типове присъстват в миокарда, съставлявайки
70% от общото население на сърдечните клетки. От клетъчна гледна точка инфилтрацията на миокарда от необичайно пролифериращи клетки може да доведе до електрофизиологични предизвикателства, напомнящи на микрофиброза (Wong et al., 2016). Когато инфилтрират физически отделени работещи миокардни клетки, такива предизвикателства водят до отклонения в електрическото разпространение; включително забавяне и анизотропия в проводимостта на електрическия импулс. В действителност, в сравнително скорошно проучване с голяма популация (Friedman et al., 2014; Wong et al., 2016) е доказана връзка между перикардната мастна тъкан и предсърдната проводимост. Въпреки че не е експериментално установено, тази асоциация вероятно отразява миокардни събития, медиирани от горепосочените механизми.
Схема на механизмите, които са в основата на повишен аритмогенен риск с повишено излишно затлъстяване. АНС, вегетативна нервна система; IL, интерлевкин; ММР, матрична металопротеиназа; ROS, реактивни кислородни видове; TLR, тол-подобен рецептор; TNF, фактор на туморна некроза. (Променено от Pandit et al., 2016).
Като цяло, обектът на мастната инфилтрация еволюира от обикновените доклади за аутопсия и биопсия на миокарда до обширни изследвания на електрофизиологичните последици от такива инфилтрати. Всъщност напредъкът в техниките за изображения все повече се фокусира върху подобряването на способността ни за по-прецизно локализиране на епикардиалните мастни депа и свързаните с тях инфилтрации. Подобни изследователски начинания ще подобрят способността ни да определяме корелацията между такива места на инфилтрация и аритмогенни субстрати. Друг важен аспект на излишното затлъстяване и аритмогенност е произходът и локализацията на клетките, участващи в процеса на мастна инфилтрация. Нещо повече, типовете/подвидовете рецептори, включително свързаните с възпалението рецептори, подобни на таксите, които могат да участват в сигнализирането на различни биофактори, остават да бъдат изследвани. И накрая, предвид доказателствата за плюрипотентност на някои клетки, присъстващи в миокарда и особено в мастните тъкани на миокарда, разбирането на разнообразието от стимули или фактори, които могат да инициират адипогенеза в миокарда, също е важна посока за бъдещи изследвания.
Авторски приноси
JA: Разработи оригиналната идея за това мини ревю. Той също така е написал/редактирал мини рецензията. TH: Помощ при написването/редактирането на този отзив.
Изявление за конфликт на интереси
Авторите декларират, че изследването е проведено при липса на каквито и да било търговски или финансови отношения, които биха могли да се тълкуват като потенциален конфликт на интереси.
Бележки под линия
Финансиране. 1. Национални здравни институти (R01; JA). 2. Американска сърдечна асоциация (G-I-A; JA).
- Състав на диетичните макронутриенти при безалкохолна мастна чернодробна болест Преглед на свързаните с това
- Ефектите на мелатонин без пълни текстове върху безалкохолните мастни чернодробни заболявания са свързани с
- Клетките Безплатно разделяне на пълнотекстови протеинови фази по време на адаптация на стреса и HTML на клетъчната памет
- Изследователите на кортизол и мастни черни дробове откриват причина за тежки метаболитни нарушения - ScienceDaily
- Функция на клетъчната мембрана за клетъчно хранене