Резюме
Въведение
Обикновено се препоръчва оралната рехидратация да се използва като терапия от първа линия за предотвратяване или лечение на дехидратация при деца с остър гастроентерит (AGE) [5]. Въпреки доказаната ефикасност на оралната рехидратационна терапия, тя все още остава недостатъчно използвана [6, 14]. Основната причина е, че оралната рехидратационна терапия нито намалява честотата на изпражненията и загубата на течности, нито съкращава продължителността на заболяването, което намалява приемането му. Ефективните и евтини интервенции, които биха могли да допринесат за ефекта от оралната рехидратационна терапия, представляват интерес за болногледачите и здравните специалисти.
В страни, в които са налични както LGG, така и смекта, едновременното им приложение често се практикува с цел допълнително намаляване на продължителността и тежестта на заболяването. Съществува обаче несигурност относно ползите от едновременното приложение на LGG и смекта, докато очевидно това увеличава цената на лечението. Настоящото проучване е предназначено да определи дали LGG плюс смекта превъзхожда LGG само за лечение на деца с AGE.
Методи
Указанията от изявлението CONSORT са спазени за това проучване [9].
Дизайн на проучването и участници
Това беше двойно-сляпо, рандомизирано, плацебо-контролирано проучване. Деца на възраст от 4 до 60 месеца с AGE, дефинирани като преминаване на три или повече разхлабени или воднисти изпражнения на ден за> 1 ден, но 5 дни, скорошна анамнеза за диария, посочена или от бележки на родители/настойник или болница, в основата на хронични стомашно-чревни заболяване, недохранване (съотношение тегло/височина под 5-тия процентил), системна инфекция и имунни дефекти или имуносупресивно лечение.
Интервенция
При всички деца при влизането в проучването се вземат проби от изпражненията за микробиологични изследвания. За скрининг на бактерии са използвани стандартни култури на изпражненията (Салмонела, Шигела, Ешерихия коли). Наличието на ротавирус и ентеричен аденовирус тип 40/41 беше определено с помощта на имунохроматографска техника (VIKIA Rota-Adeno, bioMérieux, Marcy l’Etoile, Франция) съгласно инструкциите на производителя.
Резултати
The първичен изходна мярка е продължителността на диарията, дефинирана като времето от рандомизацията до последното диарийно изпражнение или като най-малко 12 часа без изпражнения. The втори изходните мерки включват честота на изпражненията, консистенция на изпражненията, определени с помощта на седемточковата скала за форма на изпражненията на Бристол [7] (1 за твърди бучки до 7 за воднисти изпражнения - за подробности вижте Таблица 1), необходимост от антибиотична терапия (да/не), повръщане (да/не; колко пъти), рецидив на диария, поносимост на изследваните продукти, необходимост от хоспитализация (да/не, колко дълго), нужда от непланирана интравенозна рехидратационна терапия (да/не, колко време) и неблагоприятни събития.
Размер на пробата
Да се покаже разлика от 24 часа в продължителността на диария с α = 0,05 и 80% мощност (несдвоен студент т тест) и като се приеме 20% оттегляне, бяха необходими общо 88 участници. Изчисленията на размера на извадката бяха извършени с помощта на StatsDirect (версия 2.5.6; 2006-04-15 StatsDirect статистически софтуер. Http://www.statsdirect.com. Англия: StatsDirect Ltd. 2006).
Рандомизация и заслепяване
Рандомизацията на блокове с размер на блока 8 е направена с компютърно генериран списък с произволни числа, изготвен от изследовател (HS) без клинично участие в проучването. Списъкът е скрит от клиницистите, които записват пациенти и оценяват крайните точки (MPL, MU), както и от родителите до края на проучването. Изследваните продукти бяха приготвени централно в идентични опаковки от болничната аптека на Медицинския университет във Варшава от независим персонал, който не участва в провеждането на проучването.
Статистически методи
Студентът с две опашки т тестът е използван за сравнение на средните стойности на променливите, приближаващи нормалното разпределение. За ненормално разпределени променливи, Mann-Whitney U е използван тест. The χ 2 за сравнение на пропорциите е използван тест или точен тест на Фишер, според случая. Разликите между изследваните групи бяха счетени за значими, когато P стойност беше
Резултати
Поток на участниците
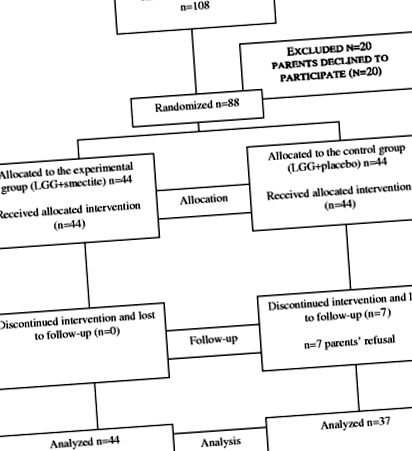
Фигура 1 е блок-схема, показваща напредъка на субектите през проучването. От 88 деца, които са били подложени на рандомизация, 44 са разпределени в експерименталната група (LGG/смектит), а 44 - в контролната група (LGG/плацебо). Седем деца от контролната група прекратиха проучването и в крайна сметка бяха загубени за проследяване. Общо 81 (92%) деца бяха включени в анализа.
Блок-схема на субекти, участващи в проучването
подбор на персонал
Участниците бяха наети измежду пациенти от педиатричната болница на Медицинския университет във Варшава, Полша, между август 2010 г. и юни 2012 г.
Изходни данни
Изходните демографски и клинични характеристики не се различават между двете групи и са представени в таблица 2.
Резултати
Резултатните мерки са обобщени в таблица 3 и на фиг. 2 и 3. Продължителността на диарията (първичният резултат) е сходна при групите LGG/смекта и LGG/плацебо (P = 0,43). Няма значителни разлики между изследваните групи за вторичните резултати, с три изключения. На 4-ия ден има намалена честота на изпражненията в групата на LGG/плацебо в сравнение с групата LGG/смекта (P = 0,03). Също така, консистенцията на изпражненията се различава между групите на ден 4. Консистенцията на изпражненията е по-трудна при LGG/плацебо в сравнение с групата LGG/смекта. Въпреки това изпражненията с оценки 3, 4 и 5 по скалата за форма на изпражненията в Бристол се наричат изпражнения с нормална консистенция. Не са наблюдавани значителни разлики в консистенцията на изпражненията между групите през всеки друг ден. Въпреки че няма значителна разлика в необходимостта от интравенозна рехидратация между групите, има разлика в нейната продължителност. В групата LGG/смекта в сравнение с групата LGG/плацебо е имало значително по-кратка продължителност на интравенозната терапия след рандомизиране (P = 0,02). Не са наблюдавани нежелани събития в изследваните групи.
Честота на изпражненията, брой на ден (медиана, диапазон)
Резултат за консистенция на изпражненията, използвайки скала за форма на изпражненията на Бристол (медиана, диапазон) —1 за твърди бучки до 7 за воднисти изпражнения
Дискусия
Основни констатации
Нашето двойно-сляпо, рандомизирано, плацебо контролирано проучване показа, че LGG плюс смекта изглежда е еднакво ефективен само за LGG за лечение на деца с AGE. Няма значителни разлики между изследваните групи за вторичните резултати, с три изключения. В групата на LGG/плацебо в сравнение с групата LGG/смекта има значително намалена честота на изпражненията, но само на 4 ден. Въпреки че имаше разлика между групите в консистенцията на изпражненията, тя нямаше клинично значение; това е така, защото изпражненията с оценки 3, 4 и 5 по скалата за форма на изпражненията в Бристол се наричат изпражнения с нормална консистенция. Ако е била необходима непланирана интравенозна рехидратация, е имало значително по-кратка продължителност на интравенозната терапия в групата на LGG/смекта в сравнение с групата само с LGG.
Сравнение с други проучвания
Доколкото ни е известно, това е първото проучване за оценка на едновременното приложение на LGG със смекта. Едно предварително публикувано рандомизирано контролирано проучване (RCT) сравнява приложението на смес от три пробиотични щама, т.е., Lactobacillus rhamnosus щамове E⁄N, Oxy и Pen (предлагани на пазара като Lakcid, Biomed, Полша), плюс смекта с приложението само на пробиотици [12]. Това проучване е проведено при 107 полски деца на възраст от 6 до 36 месеца с AGE. Авторите съобщават, че в пробиотичната/смектитовата група в сравнение с пробиотичната група има значително по-кратка продължителност на течните изпражнения, по-кратка продължителност на интравенозна рехидратация, по-кратка продължителност на хоспитализацията, по-кратка продължителност на треска> 38 ° C и по-голямо тегло печалба. Съществуват обаче някои методологични ограничения на изследването, включително неясно прикриване на разпределението, липса на заслепяване и анализ на намерение за лечение; това може да доведе до отклонения в подбора, представянето и/или износването и в крайна сметка да обезсили резултатите.
И обратно, ефикасността на LGG и смекта, прилагани поотделно, е проучена в редица RCT и техните мета-анализи. За LGG, един мета-анализ на осем RCT, включващ 988 участници, установи, че в сравнение с контролите, приложението на LGG няма ефект върху общия обем на изпражненията. Използването на LGG обаче е свързано със значително намаляване на продължителността на диарията, особено тази на ротавирусна етиология [15]. Положителен ефект от използването на LGG за лечение на остра диария беше потвърден и в по-скорошен преглед на Cochrane [1].
За смектит, един мета-анализ на данни от шест RCT показва, че смектитът значително намалява продължителността на диарията в сравнение с плацебо. Шансът за излекуване на интервенционен ден 3 е значително увеличен при смекта спрямо контролната група, като броят е необходим за лечение от 4 [13]. Две извършени впоследствие големи, двойно-слепи RCT, извършени в Перу и Малайзия, потвърдиха намаляване на продължителността на диарията и също така показаха намаляване на отделянето на изпражнения [4]. Последният открит RCT, извършен в Индия, също установява, че смекта намалява продължителността на диарията и предотвратява продължителен курс [11].
Силни страни и ограничения на изследването
Силните страни на това проучване включват адекватно рандомизиране и използването на анализ за намерение за лечение, като и двете минимизират риска от пристрастия. Въпреки че имаше цялостно (92%) проследяване, имаше не-значително повече пациенти, загубени от проследяване в групата LGG/плацебо в сравнение с групата LGG/смекта (7 срещу 0). Тъй като родителите не съобщиха причините за отказа да продължат, няма ясно обяснение за тази констатация.
Участници в това проучване са малки деца, които обикновено развиват AGE, така че резултатите са приложими за клиничната практика. От друга страна, нашите резултати се отнасят предимно за хоспитализирани деца. По принцип ефикасността на лечението може да е различна за различните подгрупи (напр. Стационарни пациенти в сравнение с амбулаторни пациенти). Приетите в болницата могат да бъдат по-сериозно засегнати, по-късно в хода на заболяването или да бъдат по-дехидратирани и по този начин да реагират по различен начин на лечението. Оценката в тези подгрупи е оправдана.
Потенциално ограничение на нашето проучване е липсата на перфектно ослепяване. Както беше посочено по-рано, пациентите са получавали смекта или плацебо в малки, еднакви опаковки от болничната аптека. И двете бяха бели прахове. След разтваряне във вода обаче те бяха с различни цветове, което потенциално би могло да бъде проблем, ако родителят/болногледачът е имал предишен опит със смекта.
За достъп до консистенцията на изпражненията използвахме скалата за форма на изпражненията в Бристол, която не е валидирана за най-малките деца. Докато това проучване беше в последния етап на планиране, бе публикувана скалата за изпражнения на бебето в Амстердам за оценка на консистенцията на изпражненията на недоносените и на недоносените деца (четири елемента), количеството (четири елемента) и цвета (шест елемента). Скалата е по-подробна и може да бъде полезна за разграничаване на нормалните и ненормалните модели на дефекация при кърмачета; той обаче не е валидиран за практически и изследователски цели [2]. Въпреки ограниченията на скалата за форма на изпражненията в Бристол, тя предлага по-обективен начин за оценка на консистенцията на изпражненията, отколкото просто разчитане на възприятията на болногледачите.
В нашето проучване продължителността на диарията се използва като основна мярка за резултат. За съжаление само тази мярка не се счита за оптимална. Количествените критерии за диария се препоръчват от Световната здравна организация за използване при оценката на терапевтични средства за лечение на остра диария [16]. Въпреки това, нежеланието на болногледачите и доставчиците на здравни грижи да извършват тромавото събиране на изпражнения, изпитано от нас при провеждането на някои предишни проучвания, беше основната причина да не се включат изхожданията от изпражненията в протокола на това проучване.
Заключение и последици за практиката
Въпреки че всички са единодушни, че при лечението на деца с AGE трябва да се избягват ненужни лекарства, въпреки това някои средства обикновено се използват. Констатациите от този RCT помагат за оптимизиране на управлението на AGE чрез обезсърчаване на използването на режими без доказана ефикасност, но допълнителни разходи. Резултатите от този двойно-сляп RCT показват, че добавянето на смекта към LGG като адювант към стандартната рехидратационна терапия при кърмачета и малки деца с AGE не предлага допълнителна полза. Ако има желание от страна на болногледачите или здравните специалисти за допълнително лечение, използването на LGG или смекта е по-рационален избор и може да се обмисли.
Препратки
Allen SJ, Martinez EG, Gregorio GV, Dans LF (2010) Пробиотици за лечение на остра инфекциозна диария. Cochrane база данни Syst Rev (11): CD003048
Bekkali N, Hamers SL, Reitsma JB, Van Toledo L, Benninga MA (2009) Мащаб на формата на бебешки изпражнения: развитие и резултати. J Pediatr 154: 521–526
Brouillard MY, Rateau JG (1989) Ефективност на адсорбция на 2 глини, смекта и каолин върху бактериални ентеротоксини. Проучване in vitro в клетъчна култура и в червата на новородени мишки. Gastroenterol Clin Biol 13: 18–24
Dupont C, Foo JL, Garnier P, Moore N, Mathiex-Fortunet H, Salazar-Lindo E (2009) Пероралният диосмектит намалява отделянето на изпражнения и продължителността на диарията при деца с остра водниста диария. Clin Gastroenterl Hepatol 7: 456–462
Guarino A, Albano F, Ashkenazi S, Gendrel D, Hoekstra JH, Shamir R, Szajewska H, Европейско дружество за детска гастроентерология, хепатология и хранене; Европейско общество за детски инфекциозни болести (2008) Насочени на доказателства насоки за лечение на остър гастроентерит при деца в Европа. J Pediatr Gastroenterol Nutr 46 (Suppl 2): S81 – S122
Guarino A, Albano F, Guandalini S, за работната група на ESPGHAN за остра диария (2001) Разтвор за орална рехидратация: към истинско решение. J Pediatr Gastroenterol Nutr 33 (Suppl 2): S2 – S12
Lewis SJ, Heaton KW (1997) Мащаб на формата на изпражненията като полезно ръководство за времето за преминаване на червата. Scand J Gastroenterol 32: 920–924
Mahraoui L, Heyman M, Plique O, Droy-Lefaix MT, Desjeux JF (1997) Апикален ефект на диосмектит върху увреждане на чревната бариера, индуцирано от базален туморен фактор некроза-a. Черва 40: 339–343
Moher D, Schulz KF, Altman DG (2001) Декларацията CONSORT: преразгледани препоръки за подобряване на качеството на докладите от рандомизирани проучвания с паралелни групи. Lancet 357: 1191–1194
Още J, Benazet F, Fioramonti J, Droy-Lefaix MT (1987) Ефекти от лечението със смекта върху стомашни и чревни гликопротеини при плъхове: хистохимично проучване. Histochem J 19: 665–670
Mujawr QM, Naganoor R, Ali MD, Malagi N, Thobbi AN (2012) Ефикасност на диоктаедричен смекта при остра водниста диария при индийски деца: рандомизирано клинично изпитване. J Trop Pediatr 58: 63–67
Pociecha W, Balcerska A (1998) Влияние на мукопротективните лекарства върху клиничния ход на детския ротавирусен гастроентерит. Gastroenterologia Polska 6: 533–542, полски
Szajewska H, Dziechciarz P, Mrukowicz J (2006) Мета-анализ: смекта при лечението на остра инфекциозна диария при деца. Aliment Pharmacol Ther 15 (23): 217–227
Szajewska H, Hoekstra JH, Sandhu B (2000) Управление на остър гастроентерит в Европа и въздействието на новите препоръки: многоцентрово проучване. J Pediatr Gastroenterol Nutr 30: 522–527
Szajewska H, Skórka A, Ruszczyński M, Gieruszczak-Białek D (2007) Мета-анализ: Лактобацилус GG за лечение на остра диария при деца. Aliment Pharmacol Ther 25: 871–881
Световна здравна организация (1990) Рационалното използване на лекарства при лечението на остра диария при деца. Световна здравна организация, Женева
Световна здравна организация (2005) Лечение на диария: наръчник за лекари и други старши здравни работници, 4-то изд. КОЙ, Женева
Благодарности
Тази работа е финансирана от Медицинския университет във Варшава.
Конфликт на интереси
Авторите не декларират конфликт на интереси.
Свободен достъп
Тази статия се разпространява при условията на лиценза за признание на Creative Commons, който позволява всяко използване, разпространение и възпроизвеждане на какъвто и да е носител, при условие че оригиналните автори и източникът са кредитирани.
Информация за автора
Принадлежности
Катедра по педиатрия, Медицински университет във Варшава, Dzialdowska 1, 01-183, Варшава, Полша
Małgorzata Pieścik-Lech, Magdalena Urbańska & Hania Szajewska
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
- Хипохлоремия и 30-дневна скорост на реадмисия при пациенти с остра декомпенсирана сърдечна недостатъчност -
- Екстракт от лист на бръшлян и остър бронхит - McIsaac Health Systems Inc.
- Скачащи крикове срещу скачащо въже Кой е по-добрият The Times of India
- Метаболитни ефекти на Lactobacillus reuteri DSM 17938 при хора с диабет тип 2 рандомизиран
- Метилпреднизолон за пациенти с тежък остър респираторен синдром на COVID-19 - изглед в пълен текст