Резюме
Хипоталамусното затлъстяване е потенциално последствие от краниофарингиома, произтичащо от увреждане на хипоталамуса, причинено или от тумора и/или от неговото лечение. Изглежда значителното наддаване на тегло, което характеризира това разстройство, е резултат от нарушена симпатоадренална активация, парасимпатикова дисрегулация и други хормонални и хипоталамусни нарушения, които нарушават баланса между енергийния прием и разходите. Като се има предвид хипопитуитаризмът, внимателното управление на хормоналния дефицит е важно за контрола на теглото при тези пациенти. В допълнение, диета, упражнения и фармакотерапия, насочени към увеличаване на симпатиковата продукция, контролиране на хиперинсулинизма и насърчаване на загуба на тегло са били използвани за лечение на това заболяване, но тези мерки рядко водят до трайна загуба на тегло. Въпреки че рутинните интервенции не са провеждани рутинно, новите данни показват, че хирургичните интервенции за отслабване, включително стомашен байпас на Roux-en-Y, могат безопасно и ефективно да се използват за лечение на хипоталамусно затлъстяване при пациенти с краниофарингиом.
Въведение
Докато разбирането ни за механизмите, лежащи в основата на развитието на затлъстяване при пациенти с ХП, е напреднало, терапевтичният напредък при лечението на HO остава ограничен. Няколко възможности за медицинско лечение са проучени при пациенти с HO, но контролът на теглото, постигнат с модификация на начина на живот и фармакотерапия, обикновено е скромен и често преходен. Като се имат предвид предимствата на бариатричната хирургия за лечение на конвенционално морбидно затлъстяване, напоследък има интерес към използването на хирургични техники за отслабване при пациенти с HO. В този преглед ще обсъдим медицинското и невроендокринното управление на HO и ще опишем случай на успешна загуба на тегло след операция на стомашен байпас при пациент с HO след лечение с CP. Ще използваме случая, за да илюстрираме ключови идеи, участващи в клиничното лечение на HO и да подчертаем нововъзникващата роля на хирургичните интервенции за отслабване при тази популация пациенти.
Клиничен случай
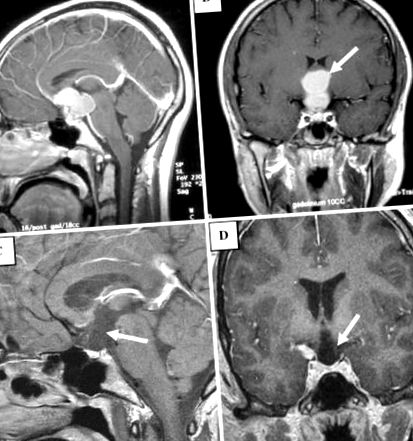
T1 претеглен постконтрастен сагитален (а) и коронален (б) изображението показва сложна двупосочна повишаваща маса (стрелка в б) на нивото на предната трета камера, запълваща супраселарното казанче; масата е отделна от нормално появяващата се хипофизна жлеза. T1 претеглена след контрастна сагитална (° С) и коронален (д) изображение, получено след операцията, показва резекция на супраселарната лезия, вече с деформиран разширен външен вид към предната долна трета камера и хипоталмичната област (стрелка в д), както и дефицит по пода на третата камера и отсъстващ стъбло на хипофизата (стрелка в ° С)
Промяна в ИТМ на пациента и клинични събития с течение на времето
За по-нататъшно изследване на въздействието на RYGB върху метаболитния профил на пациента, ние оценихме енергийните разходи в покой (REE) и секрецията на чревния хормон в отговор на смесено хранене, както преди, така и след 9 и 15 месеца след операцията. REE се измерва на гладно чрез непряка калориметрия, като се използва метаболитна количка ParvoMedics TrueOne 2400. Преди операцията, индиректната калориметрия разкрива разход на енергия в покой от 1877 kcal/24 h, с 9% по-нисък от прогнозирания REE, изчислен по установени формули (Таблица 1) [8, 9]. Девет месеца след операцията REE намалява до 1,142 kcal/24 h (31–34% по-малко от предвиденото), а 15 месеца след операцията REE намалява допълнително до 1 079 kcal/24 h (35–39% по-малко от предвиденото). Лептин, инсулин, грелин, ацил-грелин, пептид YY (PYY) и глюкагон-подобен пептид (GLP-1) бяха измерени на гладно (Таблица 1). Нивата на лептин и инсулин на гладно намаляват от изходното ниво. Обратно, имаше увеличение от 64% в нивата на циркулиращ грелин на 9 месеца и 107% увеличение от изходното ниво на 15 месеца. Нивата на ацил-грелин също се повишават след операцията. На гладно PYY и GLP-1 не се променят след RYGB.
маса 1
Разход на енергия в покой и хормонални нива на изходно ниво и 9 и 15 месеца след стомашен байпас
| Телесно тегло (кг) | 128 | 94 | 97 |
| REE (kcal/ден) a | |||
| Измерено | 1,877 | 1,142 | 1,079 |
| Харис-Бенедикт | 2,065 | 1,737 | 1,764 |
| Мифлин-Св. Jeor | 1 986 | 1,645 | 1,672 |
| РЗЕ (kcal/kg) a | |||
| Измерено | 14.7 | 12.2 | 11.2 |
| Харис-Бенедикт | 16.1 | 18.4 | 18.2 |
| Мифлин-Св. Jeor | 15.5 | 17.5 | 17.3 |
| Хормони | |||
| Лептин ng/ml b | 87.6 | 34,0 | 41.4 |
| Инсулин μIU/ml c | 22.5 | 2.18 | 3.62 |
| Грелин pg/ml d | 407 | 668 | 843 |
| Acyl-Ghrelin pg/ml e | 2.8 | 7.6 | 13.0 |
| PYY pg/ml f | 199 | 208 | 197 |
| GLP-1 pmol/1 | 13.5 | 10.8 | 10.4 |
Измерените енергийни разходи, получени чрез индиректна калориметрия, се отчитат, както се изчисляват енергийните разходи в покой, използвайки Harris-Benedict и Mifflin-St. Уравнения на Жор
Дискусия
Медицинско лечение на хипоталамусно затлъстяване
Управление на начина на живот
Управление на нарушена симпатоадренална активация - медикаментозно лечение със симпатомиметици
В допълнение към намалената REE, пациентите с HO показват нарушена симпатоадренална активация, илюстрирана от намалени катехоламини в урината [16, 17]. Впоследствие симпатомиметичната фармакотерапия се използва за отслабване на наддаването на тегло и насърчаване на загубата на тегло при пациенти с HO. Mason et al. лекува петима педиатрични пациенти, които развиват HO след резекция на CP с декстроамфетамин в продължение на 24 месеца. При дози, вариращи от 12,5 до 20 mg на ден, скоростта на увеличаване на теглото намалява от 2 ± 0,3 kg/месец на 0,4 ± 0,2 kg/месец и стабилизирането на теглото е постигнато след 1 месец и остава стабилно при проследяване 24 месеца. Докато калорийният прием не се различава преди и след лечението, дневниците за упражнения разкриват повишена физическа активност върху декстроамфетамин [18]. По същия начин, стабилизация на теглото или умерена загуба на тегло (-0,7 SDS при мъже, -0,44 SDS при жени) се наблюдава при десет от 12 пациенти с HO, лекувани с 10 mg дневно дексамфетамин [19].
Симпатомиметичният сибутрамин, който инхибира повторното поемане на норепинефрин и серотонин, също е оценен за лечението НО. При двойно сляпо плацебо контролирано 20 × 20 седмично кръстосано проучване с 10–15 mg сибутрамин води до значително намаляване на ИТМ в сравнение с плацебо, въпреки че по-специално загубата на тегло е по-изразена при тези с нехипоталамусно затлъстяване [20 ]. Този диференциран отговор може да отразява факта, че това лекарство вероятно е насочено към области на регулиране на телесното тегло, които са потенциално увредени при HO. Независимо от това, загубата на тегло на нашата пациентка със сибутрамин беше изразена, въпреки че трябва да се отбележи, че по това време тя беше силно ангажирана с интензивни упражнения. Докато сибутраминът ясно демонстрира предимства при пациенти с HO, той е изтеглен от пазара през октомври 2010 г. поради данни от проучването за сърдечно-съдови резултати на Sibutramine (SCOUT), което предполага повишен риск от инсулт и инфаркт на миокарда [21].
Фентерминът, който стимулира освобождаването на норепинефрин в хипоталамуса, е одобрен за краткосрочно лечение на затлъстяването. Доказано е, че води до умерена загуба на тегло като монотерапия и в комбинация с топирамат, но не е проучен при пациенти с HO [22, 23]. Използването на симпатикомиметиците кофеин и ефедрин в комбинация също може да се обмисли. Три случая на пациенти с ХП с НО, кофеин и ефедрин са свързани със средна загуба на тегло от 13,9% за 6 месеца, при поддържана загуба на тегло от 8,5 и 9,5% за 2/3 случая на 2 и 6 години съответно [24].
Управление на парасимпатиковата дисрегулация и хиперинсулинемия
Хамилтън и съавт. Изучават нов режим на перорално лечение, насочен към намаляване на секрецията на инсулин, използвайки диазоксид (2 mg/kg, максимална доза 200 mg/ден) и засилване на инсулиновото действие, използвайки метформин (1000 mg два пъти дневно) при пациенти с HO [27]. В това проспективно отворено 6-месечно изпитване за пилотно лечение средното наддаване на тегло е значително намалено. Наддаването на тегло след 6 месеца терапия е +1,2 ± 5,9 kg v. + 9,5 ± 2,7 kg през 6-те месеца преди проучването сред седемте субекта, завършили проучването. Двама от деветте участници бяха изтеглени - единият поради трансаминит и повръщане, а другият поради оток на педала. Въпреки че само метформин не е проучен при НО, той може да се разглежда като допълнителна терапия при пациенти с доказателства за инсулинова резистентност, непоносимост към глюкоза или диабет, предвид връзката му със загуба на тегло и намалено висцерално затлъстяване [28].
Управление на загуба на тегло с други агенти
Управление на хипопитуитаризма
Хирургично лечение на хипоталамусно затлъстяване
Предвид непреодолимите недостатъци на наличните медицински терапии за лечение на HO и ефективността на бариатричната хирургия за лечение на конвенционално затлъстяване, хирургичните техники за отслабване сега се разглеждат при пациенти с CP и HO, когато други интервенции се провалят. Въпреки че ентусиазмът за бариатрична хирургия при пациенти с HO е смекчен от опасения, че нарушаването на апетита може да попречи на спазването на следоперативни диетични ограничения, ползите от хирургичните интервенции изглеждат обещаващи [36, 37]. Доказано е, че операцията за стомашен байпас улеснява намаляването на теглото не само чрез ограничаване на обема на стомаха, но и чрез промяна на секрецията на апетитни чревни хормони като грелин, GLP-1 и PYY по начин, който благоприятства намаляването на апетита и загубата на тегло [38, 39]. При гризачите е доказано, че тези стомашно-чревни пептидни хормони упражняват своите метаболитни ефекти чрез взаимодействие с хипоталамусните неврони, които експресират анорексигенни и орексигенни фактори [40, 41]. Не е известно дали благоприятните централни ефекти от промените в секрецията на чревния хормон, наблюдавани при стомашен байпас, се запазват или отричат от хипоталамусно увреждане, налично в HO, въпреки това има данни, които предполагат, че при тази популация може да се постигне хирургично отслабване.
Въпреки че няма налични данни, сравняващи REE след RYGB при пациенти с HO с тези на съответстващите контроли, сравнително ниското изходно ниво и след операцията REE на нашия пациент може да показват, че някои пациенти с HO са с по-висок риск от възстановяване на теглото. Доказано е, че скелетната мускулна маса намалява след байпас, което вероятно допринася за намаляване след байпаса в REE [62]. Впоследствие трябва да се подчертае значението на постоперативното упражнение, тъй като то може да подобри динамичната мускулна сила, РЗЕ и функционалния капацитет и може да доведе до по-голяма загуба на тегло и подобрения в качеството на живот, свързано със здравето [63, 64].
Заключения
Благодарности
Авторите биха искали да признаят участието на нашия пациент в това проучване и експертната техническа помощ на Gerardo Febres и Irene M. Conwell. Този проект беше подкрепен от NIH/NIDDK RO1> DK072011 и NIH/NCRR UL1RR024156. JK има изследователска подкрепа от Covidien.
- Локално индуцирано покафеняване на мастна тъкан чрез пластир Microneedle за лечение на затлъстяване ACS Nano
- Честота на панкреатит, вторични причини и лечение на пациенти, посочени в специалност
- Стратегии за здраве и лечение при затлъстяване - издатели Karger
- Подобряване на диагностиката и лечението на хепатобилиарната патология при юноши със затлъстяване
- Как затлъстяването влияе на риска и лечението на псориазис