Проучване на промените в антикоагулантната практика при пациенти с неклапно предсърдно мъждене в Холандия
Налице е декларация за тази статия
Резюме
В Холандия има над 385 000 случая на предсърдно мъждене (AF), с над 45 000 нови случая всяка година. Освен всичко друго, пациентите с ФП са изложени на висок риск от инсулт. На пациентите често се предписва перорална антикоагулация, като антагонисти на витамин К (VKA), за да се намалят тези рискове. Наскоро представен клас перорални антикоагуланти, антагонисти без витамин К (NOAC), бързо набира валута в световната клинична практика. Това проучване дава представа за промените, които тези нови лекарства ще доведат до холандската клинична практика.
GARFIELD-AF е мащабен наблюдателен регистър на пациентите с АФ, стартиран през 2009 г., за да проследи развитието на глобалната антикоагулационна практика и да проучи въздействието на NOAC терапията по-специално при ФП. Регистърът включва широк спектър от изходни характеристики и има особен акцент върху: (1) кървене и тромбоемболични събития; (2) международни нормализирани колебания на съотношението; и (3) модели на спазване на терапията и устойчивост. Резултатите в този документ предоставят базовите характеристики на първите кохорти холандски участници в този регистър и обсъждат някои от последиците от промените в антикоагулационната практика.
Въпреки че терапията с VKA остава преобладаващо предпочитана от холандските практикуващи, NOACs очевидно печелят популярност. Между 2011 и 2014 г. NOACs представляват все по-голям дял от предписанията за перорални антикоагуланти.
Данните, предоставени от регистъра на GARFIELD-AF, могат да бъдат използвани от здравните системи за информиране на по-добри бюджетни стратегии, от практикуващите за по-добро приспособяване на пътищата на лечение към пациентите и накрая за насърчаване на осведомеността относно различните налични възможности за лечение и свързаните с тях рискове и ползи за пациентите.
Въведение
Предсърдното мъждене (AF) е най-често диагностицираната сърдечна аритмия, с над 385 000 прогнозни случая [1] в Холандия (5,5% от възрастовата група> 55 години). С приблизително 45 000 нови случая [1] всяка година, AF продължава да расте с тревожна скорост. Пациентите с ПМ имат петкратен риск да страдат от исхемичен инсулт [2, 3] и са изложени на значително повишен риск от други тромбоемболични събития [4, 5]. Освен това инсултите са два пъти по-склонни да бъдат летални при пациенти с ПМ, отколкото при тези без него [6]. Необходимостта от добра тромботична профилактика е очевидна.
Най-широко използваният метод за намаляване на инсулт и други тромбоемболични събития при пациенти с ПМ е антикоагулацията през устата. Пероралните антикоагуланти се подразделят предимно на антагонисти на витамин К (VKA, напр. Варфарин) и орални антикоагуланти без антагонисти на витамин К (NOAC), като последната подгрупа включва директен тромбин (дабигатран) и инхибитори на фактор Ха (ривароксабан, апиксабан, едоксабан). В Холандия NOACs бяха одобрени сравнително наскоро: дабигатран през 2008 г., ривароксабан през 2011 г., апиксабан през 2011 г. и едоксабан през 2015 г. Въпреки че клиничните проучвания показват, че NOACs не са по-ниски и в някои отношения по-добри (например по-малко вътречерепни кръвоизливи), до VKA [7], броят на пациентите, лекувани с VKA в Холандия, все още надхвърля броя на пациентите, лекувани с NOAC.
В Холандия система от антикоагулантни клиники съществува от 50-те години на миналия век. Тази мрежа от клиники обхваща страната и наблюдава по-голямата част от пациентите на VKAs. Мониторингът на международното нормализирано съотношение (INR), издаването на препоръки за коригиране на дозата и регистриране на нежелани реакции и усложнения от кървене са рутинна практика от десетилетия. Когато бяха въведени NOAC, здравният съвет на Нидерландия препоръча тези нови агенти да бъдат внимателно наблюдавани и тяхната ефикасност и усложнения да бъдат регистрирани [8]. Въпреки тези препоръки, регистрацията все още не е формализирана под формата на протоколи за проучване и понастоящем остава несигурно дали правилното наблюдение на усложненията на NOAC ще бъде институционализирано по същия начин, както при VKA. Този факт, съчетан с бавното усвояване на NOACs в Холандия досега, възпрепятства базираните в Холандия наблюдателни изследвания на техните относителни рискове и ефикасност.
Има редица причини, поради които е важно експерименталните данни да се допълват с данни от реалния живот или наблюдения. Първо, често се установява, че изследваните субекти и протоколи в експериментални (напр. Рандомизирани контролирани проучвания) неточно отразяват реалната популация пациенти, т.е. д., ключовите групи пациенти и типичните модели на грижи са недостатъчно представени [9]. На второ място, наблюдателните проучвания са в състояние да включат много по-широк спектър от потенциални рискови фактори, позволявайки анализ на по-сложни съпътстващи заболявания. На трето място, и по-подходящо за предотвратяване на тромбоза в AF, по-специално, както много други страни, Холандия може да бъде на ръба на промяна на парадигмата от VKAs към NOACs като преобладаващ тип профилактика на тромбоза. Следователно, сравняването на резултатите от нежелани събития между тези два вида антикоагулационни средства в реална обстановка ще става все по-важно за предоставянето на добро здравеопазване за пациенти с ПМ.
Методи
Регистърът GARFIELD-AF бе иницииран за преодоляване на недостига на информация около антикоагулационната терапия, чрез събиране и обобщаване на глобални данни за моделите на лечение и клиничните резултати на пациенти с неклапна ФП с ≥1 допълнителни рискови фактора за инсулт в един наблюдателен набор от данни [10] . Особената полезност на този регистър идва от неговата всеобхватност, тъй като: (1) включените базови характеристики покриват широк спектър от потенциални епидемиологични рискови фактори; (2) наборът от данни включва както перспективни, така и ретроспективни надлъжни кохорти; и (3) от юни 2014 г. включваше данни за пациентите (цел н = 55 000, текущи н = 41 677) от 35 различни страни.
Данните, събрани в регистъра GARFIELD-AF, ще бъдат особено забележими за тези изследователи и специалисти, които се интересуват от: (1) честотата на хеморагични и тромбоемболични събития при пациенти с ПМ, (2) колебания на INR за пациенти, лекувани с VKA, (3) модели на спазване на терапията и персистиране [10] Резултатите, свързани с горните променливи, ще бъдат обсъдени в бъдещи документи на GARFIELD-AF и не са обхванати от тази статия.
Критерии за включване на пациента
Всички пациенти на възраст ≥18 години с скорошна диагноза (≤6 седмици) на неклапна ФП, които имат поне един допълнителен рисков фактор за инсулт и са предоставили писмено информирано съгласие, отговарят на условията за включване в регистъра GARFIELD-AF. Пациентите, които трябва да бъдат включени в ретроспективната кохорта (вж. Записване на кохорти), трябва да бъдат диагностицирани в рамките на 6–24 месеца преди записването в регистъра.
Продължителност на проследяване д за всички пациенти е 2 години ≤ д ≤ 8 години. Пациентите, за които не се очаква по-нататъшно проследяване или удостоверително невъзможно, се изключват от регистъра, както и пациентите, чийто преходен ФП е вторичен за обратима причина.
Записване на кохорти
Има общо шест кохорти, първата от които е със задна дата, а останалите са перспективни и последователни. Всички кохорти се придържат към едни и същи критерии за включване на пациентите и са методологически различни само по отношение на периода, който обхващат. Пациенти, включени в потенциалните кохорти (н = 50 000) са записани
Резултати
Към юни 2014 г. холандската проба, включена в GARFIELD-AF, включва 929 пациенти в три кохорти. Таблица 1 изобразява селекция от описателни статистически данни за холандските кохорти от 1 до 3. GARFIELD-AF. Таблица 2 изобразява редица изходни фактори, които могат да допринесат за появата на нежелани събития при пациенти с ПМ, като състояние на пушене и CHA2DS2-VASc и ИМА-BLED резултати.
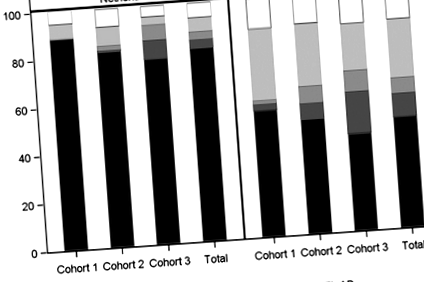
Данните показват, че пациентите, влизащи в последователни кохорти, са доста последователни по възраст (Таблица 1) и CHA2DS2-VASc резултат (Таблица 2), със средна възраст 71 години и оценка на риска 3 (SD 1.5). По-голямата част от потенциалните пациенти са диагностицирани с новопоявил се AF (73,6%) на изходно ниво, последван от пароксизмален AF (15,9%). Голяма част от потенциалните пациенти (81,4%) са били предписани VKA или VKA, комбинирани с аспирин, на изходно ниво (Таблица 1). Този дял обаче постепенно намалява с времето: от 88,8% в периода 2009–2011 г. на 77,9% в периода 2013–2014 г. Това намаление е настъпило в унисон с постепенното усвояване на NOACs (фиг. 1), което е преминало от 0% през 2009–2011 г. до 14,5% (NOACs или комбинация от NOAC и аспирин на изходно ниво) през 2013–2014 г. (Таблица 1). В същото време делът на пациентите, които не получават каквато и да е форма на антитромботично лекарство, почти не е засегнат, варирайки между 4,4 и 7,3% в тази страна (фиг. 1). В световен мащаб тази група пациенти без антитромботични медикаменти е средно около 12% и тази пропорция също почти не се променя във времето (фиг. 1).
Лечение при диагностициране, от кохорта
Дискусия
Въвеждането на нови лекарства в антикоагулационния пейзаж доведе до промени в моделите на лечение, което може да доведе до объркване по отношение на ефективното управление на антикоагулацията сред пациентите и практикуващите без подходящ достъп до информация. Сега, когато NOACs са показали, че са ефективни и безопасни за употреба в клинични изпитвания, е необходимо проучване на Фаза IV, за да се изследва действителното въздействие на тези нови лекарства. Наличието на голям, богат на променливи и неинтервенционен набор от данни, като GARFIELD-AF, може да се използва, за да разшири разбирането ни за това как различните видове антикоагулационни средства се сравняват помежду си при тяхното приемане и при ежедневното управление от пациентите и кои са следователно най-подходящ за сценарии от реалния живот.
Предварителните данни, съсредоточени върху Нидерландия в този ръкопис, показват забележителни промени във времето, със значителни различия в различните страни. В Холандия се наблюдава много постепенно усвояване на NOACs в сравнение с много други страни, включително съседката му Белгия, където само приблизително 20% от пациентите с ПМ все още са на терапия с VKA (данните не са показани). Този доста поразителен контраст между двете страни може да се обясни с наличието на мрежа от клиники за антикоагулация, обхващаща Холандия; тази ситуация е съвсем различна в Белгия, както и в много други страни по света.
Сред последователните кохорти трябва да се отбележи, че доста фиксирана част от пациентите остават нелекувани; делът на пациентите, приемащи аспирин, изглежда намалява във времето, което отчасти може да бъде причинено от относително по-голям дял от пациентите, които получават NOAC. Поради естеството на това проучване обаче не можем да дадем обяснения относно процесите на вземане на решения, които са в основата на тези очевидни промени в предписанията.
Може би най-голямата пречка за ефикасността на лечението е лошото спазване на терапията. Въпреки че моделите на несъответствие са разнообразни (напр. Редовни кратки пропуски в приемането на лекарства срещу редки по-дълги заклинания), въздействието върху ефикасността на лечението често се равнява на същия отрицателен резултат. Това важи особено за NOACs, които имат много по-кратък полуживот от VKAs [2]. Изследванията показват, че субоптималното придържане към дабигатран е свързано с повишен риск от смъртност от всички причини и инсулт [20]. Това подчертава належащата необходимост от предоставяне на добра информация на пациентите, но също така и от организиране на интегрирани антитромботични грижи за дългосрочни потребители на антикоагуланти. Интегрираните антитромботични грижи напоследък се препоръчват като стандартни грижи в национално утвърдения Национален стандарт за интегрирани антитромботични грижи 2.0 (LSKA 2.0) [21].
Регистърът GARFIELD-AF породи няколко изследователски статии, които свидетелстват за полезността на набора от данни за информиране на по-добри антикоагулационни практики. Анализ на характеристиките на първата кохорта (н = 10 614, обхващащи 19 държави, период на записване от декември 2009 г. до октомври 2011 г.) показва, че в края на ерата само с VKA антикоагулантната терапия е била недостатъчно използвана при пациенти с висок риск от инсулт и прекомерна при тези с нисък риск [22]. Друг, по-скорошен анализ потвърди тези констатации и също така показа, че повече жени, отколкото мъже, са изложени на умерен до висок риск от инсулт [23]. GARFIELD-AF е сред най-големите и най-дългогодишните от няколко скорошни мащабни наблюдателни регистри, които очертават използването и резултатите от антикоагулацията при AF.
Национални инициативи, като PINNACLE (Practice INNovation And Clinical Excellence), ORBIT-AF (Регистър на резултатите за по-добро лечение на предсърдно мъждене), Националният регистър за остри инсулти на Paul Coverdell, AFNET (Германската компетентна мрежа за предсърдно мъждене) и регионални инициативи, като PREFER в AF (Профилактика на тромбоемболични събития - Европейски регистър по предсърдно мъждене) допълват по-широкообхватни регистри с локализиран фокус, включително RealiseAF (Реално глобално проучване, оценяващо пациенти с предсърдно мъждене), RecordAF (РЕГИСТРАТИРАНЕ на сърдечния ритъм) нарушители, оценяващи контрола на предсърдно мъждене) и GLORIA-AF (Глобален регистър за дългосрочно орално антитромботично лечение при пациенти с предсърдно мъждене).
Големите регистри като описаните по-горе представляват редица реални ползи за различните групи в обществото, участващи в антитромботична терапия на пациенти с ПМ. Здравните системи ще могат да анализират по-добре бюджетните въздействия в непрекъснато развиващия се антикоагулационен пейзаж; клиницистите получават помощ при персонализиране на терапевтичните траектории, за да се възползват най-добре техните пациенти, въз основа на безбройните фактори, които допринасят за междуиндивидуалната вариабилност (напр. рискови фактори за несъответствие, профили на коморбидност, бъбречна функция); данните могат също да се използват за насърчаване на разбирането на пациентите за различните конкурентни възможности за лечение и свързаните с тях рискове и ползи. В Холандия, където подобна осведоменост все още не е оптимална, въздействието на регистъра GARFIELD-AF и други подобни може да бъде от полза.
Препратки
Heemstra HE, Nieuwlaat R, Meijboom M, Crijns HJ. Тежестта на предсърдното мъждене в Холандия. Neth Heart J. 2011; 19: 373–8.
Stambler BS. Нова ера за предотвратяване на инсулт при предсърдно мъждене: сравняване на ново поколение орални антикоагуланти с варфарин. Int Arch Med. 2013; 6: 46.
Go A, Hylek E, Phillips K. Разпространение на диагностицирано предсърдно мъждене при възрастни. J Am Med Assoc. 2001; 285: 2370–5.
Menke J, Lüthje L, Kastrup A, Larsen J. Тромбоемболия при предсърдно мъждене. Am J Cardiol. 2010; 105: 502–10.
Хюз M, Lip GYH. Инсулт и тромбоемболия при предсърдно мъждене: систематичен преглед на рисковите фактори за инсулт, схема на стратификация и данни за ефективността на разходите. Thromb Haemost. 2008; 99: 295–304.
Kakkar AK, Mueller I, Bassand JP, et al. Международен надлъжен регистър на пациенти с предсърдно мъждене с риск от инсулт: Глобален регистър за антикоагуланти в FIELD (GARFIELD). Am Heart J. 2012; 163: 13–19.e1.
Gómez-Outes A, Terleira-Fernández AI, Calvo-Rojas G, Suárez-Gea ML, Vargas-Castrillón E. Dabigatran, rivaroxaban или apixaban срещу варфарин при пациенти с неклапално предсърдно мъждене: систематичен преглед и мета-анализ на подгрупите. Thromb J. 2013; 2013: Идентификатор на статия 640723.
Холандски здравен съвет. Нови антикоагуланти: добре дозирано въведение 2012. http://www.gezondheidsraad.nl/sites/default/files/201707ENewAnticoagulants.pdf. Достъп до 26 октомври 2015 г.
Avorn J. В защита на фармакоепидемиологията - възприемане на Ин и Ян от изследванията на лекарствата. N Engl J Med. 2007; 357: 2219–21.
Apenteng PN, Murray ET, Holder R, Hobbs FDR, Fitzmaurice DA. Международен надлъжен регистър на пациенти с предсърдно мъждене с риск от инсулт (GARFIELD): британският протокол. BMC Cardiovasc Disord. 2013; 13: 31.
Bezemer ID, Roemer WH, Penning-van Beest FJA, van Eekelen E, Kramer MHH. INR изчисление на контрола: сравнение на холандски и международни методи. Neth J Med. 2013; 71: 194–8.
FNT. Резюме на годишните отчети за 2013 г. www.fnt.nl. Достъп до 26 октомври 2015 г.
Nerini E, Grip L, Camm AJ, Giugliano RP. Предсърдно мъждене и „другият проблем с наркотиците“: намаляване на несъответствието с технологиите. Eur Heart J. 2013; 34: 2031–3.
Heidbuchel H, Verhamme P, Alings M, et al. Практическо ръководство на EHRA за употребата на нови орални антикоагуланти при пациенти с неклапно предсърдно мъждене: резюме. Eur Heart J. 2013; 34: 2094–106.
Palareti G, Cosmi B. Кървене с антикоагулационна терапия - Кой е изложен на риск и как най-добре да се идентифицират такива пациенти. Thromb Haemost. 2009; 102: 268–78.
Saraf K, Morris P, Garg P, et al. Перорални антикоагуланти без антагонисти на витамин К (NOAC): клинични доказателства и терапевтични съображения. Postgrad Med J. 2014; 90: 520–8.
Liew A, Eikelboom JW, O’Donnell M, Hart RG. Оценка на интензивността на антикоагулацията и управление на кървенето със стари и нови орални антикоагуланти. Може ли J Cardiol. 2013; 29 (Suppl): 34–44.
Verheugt FW. Новите орални антикоагуланти при предсърдно мъждене: актуализация. Neth Heart J. 2013; 21: 480–4.
Fellner C. Актуализация на фармацевтичното одобрение. P T. 2015; 40: 807–8.
Shore S, Carey EP, MP Turakhia, et al. Придържане към терапията с дабигатран и надлъжните резултати на пациентите: прозрения от здравната администрация за ветераните. Am Heart J. 2014; 167: 810–7.
Kakkar AK, Mueller I, Bassand JP, et al. Профили на риска и антитромботично лечение на пациенти с новодиагностицирано предсърдно мъждене с риск от инсулт: перспективи от международния, наблюдателен, перспективен регистър на GARFIELD. PLOS ONE. 2013; 8: e63479.
Lip GY, Rushton-Smith SK, Goldhaber SZ, et al. Засяга ли сексът антикоагулантната употреба за профилактика на инсулт при неклапално предсърдно мъждене? Перспективният глобален регистър на антикоагулантите в FIELD-предсърдно мъждене. Circ Cardiovasc Качествени резултати. 2015; 8 (Suppl 1): 12–20.
Благодарности
Финансиране.
Глобалният регистър за антикоагуланти в FIELD - Предсърдно мъждене е спонсориран от Изследователския институт по тромбоза, Лондон, Великобритания. Финансирането на регистъра беше осигурено чрез безвъзмездна финансова помощ от Bayer Pharma AG, Берлин, Германия. Подготовката на тази статия беше финансово подпомогната чрез неограничен грант от Bayer, Холандия.
Информация за автора
Принадлежности
Лаборатория за клинична тромбоза и хемостаза, Институт за сърдечно-съдови изследвания Маастрихт, Маастрихт, Холандия
Катедра по вътрешни болести, Институт за сърдечно-съдови изследвания Маастрихт, Маастрихт, Холандия
НАСТОЛЕН КОМПЮТЪР. Hooftstraat 188, 1071 CH, Амстердам, Холандия
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar
Можете също да търсите този автор в PubMed Google Scholar