Въведение: кортизол, естественият глюкокортикоид
Синтетичните глюкокортикоиди имитират ефектите на кортизол, стероиден хормон, произведен от zona fasciculata, средната област на надбъбречната кора. При нормални физиологични условия кортизолът се освобождава денонощно, като най-високите нива се освобождават рано сутринта (с пик около 8 ч. Сутринта), като най-ниското му ниво е между полунощ и 4 ч. Сутринта (Chrousos, 2015). Освобождаването на кортизол се регулира от освобождаването на ACTH от хипоталамуса (оста HPA). Повишените нива на ACTH в кръвта от своя страна стимулират синтеза на кортизол от надбъбречната жлеза (Chrousos, 2015; Уикипедия: кортизол).
Освобождаването на кортизол също се увеличава значително по време на стрес (ето защо кортизолът често се нарича "хормон на стреса" ). Кортизолът има значителни метаболитни ефекти, които са полезни при стресови ситуации тип борба или бягство, като повишени кръвни нива на глюкоза и свободни аминокиселини (енергийни субстрати). Той засяга и много други функции на тялото, които биха били несъществени или вредни при стресова ситуация, една от които е потискането на възпалителните реакции. Мощният потискащ ефект на кортизол-подобни глюкокортикоиди върху имунната система често се използва при лечението на множество възпалителни разстройства, резултат от свръхактивност на имунната система, вариращи от астма до улцерозен колит (Chrousos, 2015).
Дефиниции
Механизъм на действие:
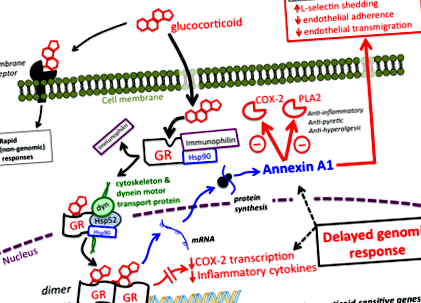
Глюкокортикоидите упражняват по-голямата част от своите ефекти чрез промяна на генната експресия (Фигура 1).
Предаване на сигнала:
Противовъзпалителни ефекти и механизми
Глюкокортикоидите намаляват възпалението чрез комбинация от инхибиране и регулиране на генната транскрипция, включително:
Миграцията на неутрофили през васкулатурата до местата на възпаление е значително намалена. Този ефект, съчетан с усилено освобождаване на клетките от костния мозък, и намалена неутрофилна апоптоза, причинява увеличаване на броя на левкоцитите (Чатъм, 2014).
ПРИЛОЖЕНИЕ А1 (Липокортин-1) - Глюкокортикоиден сигнализиращ пептид
160 структурно свързани протеини, които споделят общото свойство да се свързват към (или „анексират“) към фосфолипидните мембрани по зависим от калция начин. Като семейство те изпълняват различни биологични функции, вариращи от закрепване на цитоплазмени протеини до клетъчната мембрана, подпомагане на везикуларния трафик, до повлияване на събития, свързани с коагулацията, възпалението и апоптозата (Lim & Pervaiz, 2007; Уикипедия: Анексин).
Метаболитни ефекти и механизми
Въглехидрати и протеинов метаболизъм
Кортизолът се освобождава по време на стрес, за да доставя глюкоза като енергиен субстрат на органи, изправени пред стресови състояния. Стресовите реакции, които увеличават освобождаването на кортизол, включват енергични упражнения, психологически стрес или страх, остра травма, операция, болка, тежка инфекция и хипогликемия. Ефектите на кортизола за повишаване на кръвната глюкоза са важни за поддържането на енергийната хомеостаза по време на реакцията на стрес и гарантират, че критичните органи (като мозъка) продължават да получават хранителни вещества в момент, когато те са най-необходими за оцеляване.
Механизмите, участващи в повишаването на кръвната захар, включват:
Липиден метаболизъм
Хронично повишените глюкокортикоиди могат да предизвикат а драматично преразпределение на телесните мазнини . Смята се, че преразпределението на мазнините е резултат от различната чувствителност на периферните спрямо стволовите мастни клетки до:
Централна нервна система
Глюкокортикоидите могат да причинят разнообразни неврологични ефекти и поведенчески промени което може да отразява стероидните ефекти върху възбудимостта на невроните. Механизмите остават слабо разбрани.
Образувани елементи на кръвта
Прилагането на глюкокортикоиди води до разнообразни промени в различните видове бели кръвни клетки. Броят на циркулиращите еозинофили (които съставляват 2-4% от левкоцитите в кръвта) обикновено се намалява с глюкокортикоиди, поради повишена апоптоза и секвестиране на еозинофили в екстраваскуларни места (вероятно поради повишаване на регулацията на хемокиновия рецептор CXCR4). За разлика от тях, броят на циркулиращите неутрофили (които обикновено включват 60-70% от циркулиращите левкоцити) се увеличава от глюкокортикоидите поради комбинация от намалена миграция на неутрофилни тъкани, инхибиране на неутрофилната апоптоза и засилено освобождаване на клетките от костния мозък. Ефектът върху неутрофилите обикновено води до мрежа ( увеличен брой на левкоцитите ) (Chatham, 2014; Busti, 2015). Унищожават се и някои лимфоидни злокачествени заболявания, най-вероятно поради активиране на програмирана клетъчна смърт (Schimmer & Funder, 2011).
Терапевтични приложения
Синтетичните глюкокортикоиди са аналози на кортизола, които се използват за техните противовъзпалителни, имуносупресивни и антипролиферативни ефекти (Таблици 2 и 3). Примерите за често използвани синтетични съединения включват:
1/4 по сила на минералокортикоидите от кортизола. Бременност: По време на бременност плацентата експресира ензим (11β-хидроксистероид дехидрогеназа 2), който инактивира или кортизол, или преднизолон, като ги превръща в неактивни форми (кортизон или преднизон). Това предпазва плода от високи нива на тези глюкокортикоиди. За разлика от това, този ензим няма същия инактивиращ ефект върху някои други синтетични глюкокортикоиди като дексаметазон.
Таблица 1: Относителни възможности и продължителност на действие на терапевтичните глюкокортикоиди
Таблица 3: Общи клинични показания за системни глюкокортикоиди
| Алергия и пулмология | Астма (умерена/тежка), алергичен ринит, анафилаксия, уртикария, хранителни/лекарствени алергии |
| Дерматология | Остър тежък дерматит |
| Ендокринология | Надбъбречна недостатъчност |
| GI Болести | Болест на Crohn (IBD), улцерозен колит |
| Хематологични заболявания | Левкемия/лимфом |
| Офталмология | Увеит (възпаление на очите) |
| Ревматология/имунология | Ревматоиден артрит, системен лупус еритематозус, васкулит |
| Други | Множествена склероза, трансплантация на органи, нефротичен синдром, мозъчен оток |
(Адаптирано от Liu et al, 2013)
Фигура 3. Основните терапевтични ефекти (отгоре) и странични ефекти (отдолу), произведени от глюкокортикоиди. Много от нежеланите реакции са обратими при прекратяване на лечението с глюкокортикоиди. Асептичната некроза на бедрената кост и образуването на катаракта е постоянна и обикновено изисква хирургическа намеса. (Адаптиран от Buttgereit et al, 2005).
Странични ефекти
Може да доведе до дългосрочна терапия с високи дози глюкокортикоиди съзвездие от тежки токсичности (Saag & Fust, 2014), които са обобщени на фигури 3 и 4 и таблица 4.
Таблица 4: Кортикостероидни странични ефекти и механизми
| Хипергликемия/диабет | Повишена продукция на чернодробна глюкоза и намалено използване на периферна глюкоза (инсулиноустойчив захарен диабет) |
| Централно затлъстяване, Лунно лице, Бъфало гърбица | Повишава ефекта на липолитичните сигнали, което води до повишена FFA за подхранване на глюконеогенезата. Преразпределение на мазнините от крайниците към багажника, задната част на врата и надключичните ямки |
| Мускулна слабост и загуба | Разграждане на протеини и отклоняване на аминокиселини към производството на глюкоза |
| Качване на тегло | Повишеният апетит (ефект върху ЦНС) и повишената нужда от инсулин с течение на времето води до увеличаване на теглото |
| Остеопороза | Намалена реабсорбция на калций от бъбреците, водеща до вторичен хиперпаратиреоидизъм; забавяне на костния растеж чрез директно действие и намаляване на GH. Инхибиране на костното отлагане. |
| Аваскуларна некроза на главата на бедрената кост | Проучванията при животни показват, че GC-индуцираните повишени нива на серумни липиди водят както до повишено образуване на микроемболи в артериите, снабдяващи костите, така и до свързано с мазнини блокиране на венозния поток от костите. Резултатът от тези механизми е повишена исхемия в костите, който най-често засяга главата на бедрената кост, но може да се появи на всяко скелетно място като коляното, рамото, глезена или ръката (Wang et al, 1977; Jones, 1985; Nishimura et al, 1997; Chan & Mok, 2012; Jones & Mont, 2014). |
| Тънка кожа, която лесно се натъртва и заздравява слабо | Антипролиферативен GC ефект върху фибробласти и кератиноцити, водещ до дермална атрофия |
| Хирзутизъм и акне | поради ACTH-медиирано увеличение на надбъбречните андрогени |
| Хиперпигментация | директен ефект на ACTH върху рецепторите на меланокортин 1 |
| Повишени инфекции | Имуносупресия, свързана с атрофия на тимуса, намалено производство (брой) на неутрофили и моноцити, намалено производство на цитокини |
| Хипертония | Повишена сърдечна контрактилност, повишена съдова реактивност към вазоконстриктори (катехоламини, Ang II) |
| Хипомания, депресия, психоза | Нормалните нива на кортизол (еукортизолемия) поддържат емоционален баланс |
| Образуване на катаракта & Глаукома | Повишено вътреочно налягане и хипопаратиреоидизъм |
Страничните ефекти, подчертани в червено, са необратими (обикновено изисква хирургична подмяна). Съкращения: GC (глюкокортикоид).
Фигура 4. Симптоми на синдрома на Кушинг или хронични системни ефекти на повишени глюкокортикоиди. (Фигура на Mikael Häggström, възпроизведена от Wikimedia Commons)
Кушингоид мнемоничен
Мнемониката „Cushingoid“ е полезен начин да запомните признаците и симптомите на излишък от глюкокортикоиди:
Потискане на оста на HPA от глюкокортикоиди
Фигура 5. Вторична надбъбречна недостатъчност, причинена от хронична терапия с глюкокортикоиди (GC). Хроничното лечение с глюкокортикоиди ще намали освобождаването на ACTH от хипофизата, което в продължение на седмици до месеци може да доведе до прогресивна атрофия на клетките, продуциращи кортизол в надбъбречната жлеза (горе вдясно). Ако терапията с глюкокортикоиди внезапно бъде прекратена (което не се препоръчва), надбъбречната атрофия може значително да повлияе способността на надбъбречните жлези да отделят нормални нива на кортизол в отговор на освобождаването на ACTH, което води до признаци и симптоми на надбъбречна недостатъчност.
Вторична надбъбречна недостатъчност
Когато пациентът приема глюкокортикоид за лечение на заболяване, наличието на кортизол-подобно лекарство ще потисне освобождаването на ACTH от хипофизата (Фигура 5, горе вдясно). Тъй като произвеждащите кортизол клетки на надбъбречната жлеза (zona fasciculata) зависят от стимулацията на ACTH за нормална хомеостаза, намаляването на освобождаването на ACTH за всяко значително време (например няколко седмици или повече) ще доведе до прогресивна атрофия на тази зона. Надбъбречната атрофия намалява способността на надбъбречната жлеза да произвежда нормални нива на кортизол, когато терапията с глюкокортикоид (като преднизон) бъде прекратена.
Обикновено са необходими няколко седмици екзогенна глюкокортикоидна терапия за развитие на надбъбречна недостатъчност (Salvatori, 2005; Chrousos, 2015). По-продължително действащите глюкокортикоиди и по-високите дози системни глюкокортикоиди (срещу локални или инхалационни форми) са свързани с по-висок риск от развитие на надбъбречна супресия. Понастоящем няма настоящи насоки, основани на доказателства относно оптималния метод за прекратяване на терапията с глюкокортикоиди препоръчва се постепенно намаляване на дозите за период от седмици до месеци, преди пълното прекратяване, за да се осигури време за възстановяване на оста хипоталамус-хипофиза-надбъбречна жлеза (Liu et al, 2013).
Признаците и симптомите на вторична надбъбречна недостатъчност, които са резултат от внезапно оттегляне на глюкокортикоидите в присъствието на потискане на оста HPA, обикновено са подобни на тези, наблюдавани при болестта на Адисън, но не включват промени в пигментацията на кожата (тъй като секрецията на ACTH не се увеличава) или значителни електролитни нарушения (тъй като алдостеронът се регулира от системата ренин-ангиотензин, а не от ACTH) (Nieman 2013).
Хидрокортизон (дава се два или три пъти на ден) обикновено се предпочита за лечение на надбъбречна недостатъчност тъй като краткият му полуживот му позволява по-точно да имитира нормалния циркаден ритъм за кортизол.
- Електрическата мускулна стимулация действа ли E-Stim
- Допълнителна и алтернативна медицина - Penn State Hershey Medical Center - Панкреатит - Penn
- Намерете най-доброто) Отслабване с 5 килограма за седмица Как да отслабнете след раждането - лагер Комо
- Електрическите удари могат да ви помогнат да отслабнете
- Диета Годжи Бери Wolfberry Диета Годжи Бери Wolfberries