Дженифър Перроне
1 Катедра по неврология, Нюйоркски колеж по остеопатична медицина на Нюйоркския технологичен институт, Олд Уестбъри Ню Йорк, 11568 САЩ
Жанет М Чабла
1 Катедра по неврология, Нюйоркски колеж по остеопатична медицина на Нюйоркския технологичен институт, Олд Уестбъри Ню Йорк, 11568 САЩ
Брайън Х Халас
1 Катедра по неврология, Нюйоркски колеж по остеопатична медицина на Нюйоркския технологичен институт, Олд Уестбъри Ню Йорк, 11568 САЩ
Джудит М Хоровиц
2 Отдел по психология, колеж Medaille, Бъфало, Ню Йорк, 14214 САЩ
Герман Торес
1 Катедра по неврология, Нюйоркски колеж по остеопатична медицина на Нюйоркския технологичен институт, Олд Уестбъри Ню Йорк, 11568 САЩ
Това е статия с отворен достъп, разпространявана при условията на лиценза за приписване на Creative Commons (http://creativecommons.org/licenses/by/2.0), която позволява неограничено използване, разпространение и възпроизвеждане на какъвто и да е носител, при условие че оригиналното произведение е правилно цитиран.
Резюме
Заден план
Комбинираната терапия с флуоксетин и оланзапин бързо се превръща в ефективна стратегия за управление на симптомите на резистентна към лечение депресия. Определянето на лекарствени взаимодействия, лекарствен метаболизъм и фармакокинетика е от особен интерес за разкриване на потенциални задължения, свързани с увеличаване на лекарството при специални популации пациенти. В настоящите проучвания ние хронично прилагахме флуоксетин и оланзапин при нестресирани плъхове, за да разширим предишните си открития относно динамиката на телесното тегло.
Резултати
Хроничното лечение с флуоксетин (10 mg/kg) и оланзапин (5 mg/kg и 0,5 mg/kg) намалява наддаването на тегло, независимо от дозирането на оланзапин. При дози от 10 mg/kg и 5 mg/kg, съответно, флуоксетин и оланзапин също значително намаляват консумацията на храна и вода. Този фармакодинамичен ефект, свързан със събитието, обаче не е наблюдаван при дозировъчна парадигма от 10 mg/kg и 0,5 mg/kg, което предполага разлики в степента на поносимост като функция на дозата на оланзапин. Намаляването на наддаването на тегло не е свързано с очевидни промени в метаболизма на глюкозата, тъй като лекуваните с носител и лекарства плъхове показват неразличими нива на серумна глюкоза. Комбинацията от флуоксетин и оланзапин при плъхове дава плазмена концентрация на лекарството, която попада в рамките на очаквания терапевтичен диапазон за тези лекарства при психиатрични пациенти.
Заключения
Тези данни предполагат, че лечението с флуоксетин и оланзапин намалява наддаването на тегло при плъхове; фармакодинамичен ефект, свързан със събитието, който се различава значително от наблюдаваното в клиничното състояние. Трябва сериозно да се обмисли възможността за несъответстващи модели по отношение на промени в телесното тегло по време на терапия за увеличаване на лекарството.
Заден план
Резултати
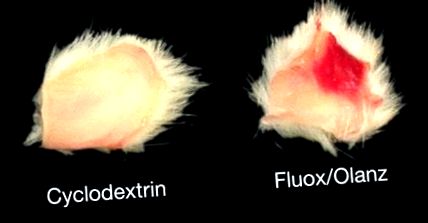
Всички плъхове понасяха добре режима на флуоксетин плюс оланзапин. Няма смъртност в резултат на 18-дневно приложение на лекарството в никоя от тестваните групи плъхове. Единственият очевиден неблагоприятен ефект е тъканната некроза в перитонеума на плъхове, инжектирани с флуоксетин плюс 5 или 0,5 mg/kg оланзапин (фиг. (Фиг. 1). 1). По този начин изглежда, че флуоксетинът произвежда фокален некротизиращ васкулит в мястото на инжектиране. По-рано са докладвани некротичните свойства на горния антидепресант [17]. Оланзапин, от друга страна, не предизвиква некроза на тъканите в перитонеалните кухини на плъхове, когато се прилага самостоятелно (данните не са показани).
Некроза на тъканите по време на хронично лечение с флуоксетин (флуокс) и оланзапин (оланц). Тази фигура изобразява еднакво изрязани перитонеални кухини на мъже, инжектирани IP с разтвор на носител (циклодекстрин) или горния модел на комбинация от лекарства в продължение на 18 последователни дни. Обърнете внимание на степента на увреждане на тъканите (
Ширина 1 см) на мястото на приложение на лекарството. Фокална некроза е очевидна при лекувани с наркотици плъхове, независимо от дозирането на оланзапин.
Промени в телесното тегло по време на хронично лечение с флуоксетин (флуокс, 10 mg/kg) и оланзапин (olanz, 5 mg/kg). Теглото на тялото на плъхове се записва преди и след терапия за увеличаване на лекарството. Данните представляват средно ± SEM. N = 5-7 животни на група. * P ≤ 0,05 в сравнение с лекувани с наркотици плъхове. NS = не е значително.
Промени в приема на храна и вода по време на хронично лечение с флуоксетин (флуокс, 10 mg/kg) и оланзапин (оланц, 5 mg/kg). Плъховете при този комбиниран лекарствен режим показват значително намаляване на консумацията на хранителни вещества и течности съответно на 10 и 12 ден от лекарствената терапия. Данните представляват средно ± SEM. N = 5-7 животни на група. * P ≤ 0,05 в сравнение с лекувани с наркотици плъхове.
Фактът, че лечението с флуоксетин плюс оланзапин в продължение на 18 дни забавя непрекъснатото увеличаване на теглото, наблюдавано при плъхове, изложени на циклодекстрин, предполага поне две проверими възможности. Първо, плъховете, изложени на терапия за увеличаване на наркотици, може да ядат по-малко от техните кохорти, лекувани с циклодекстрин. Второ, приложението на флуоксетин плюс оланзапин може да промени метаболизма на глюкозата при животни, лекувани с лекарства. За да тестваме първата възможност, измерихме средния прием на храна в продължение на 12 часа от тъмния цикъл при плъхове, лекувани с флуоксетин плюс 5 mg/kg оланзапин. На 10-ия ден от лечението с наркотици, плъховете, изложени на този режим за увеличаване на лекарствата, се хранят значително по-малко (t10 = 5,5, P ≤ 0,001) от третираните с носител животни (Фиг. (Фиг. 4). 4). Интересното е, че същата група плъхове също показа значително намаляване на приема на вода (t10 = 6,7, P ≤ 0,01) в сравнение с третирани с циклодекстрин животни (фиг. (Фиг. 4). 4). По този начин, плъховете, изложени на флуоксетин плюс 5 mg/kg оланзапин се хранят (
32%) и пиене (
38%) по-малко на 10 и 12 ден от лечението с наркотици, съответно.
Промени в телесното тегло по време на хронично лечение с флуоксетин (флуокс, 10 mg/kg) и оланзапин (olanz, 0,5 mg/kg). Теглото на тялото на плъхове се записва преди и след терапия за увеличаване на лекарството. Данните представляват средно ± SEM. N = 5-7 животни на група. * P ≤ 0,05 в сравнение с лекувани с наркотици плъхове. NS = не е значително.
Няма промени в консумацията на храна или приема на вода по време на хронично лечение с флуоксетин (флуокс, 10 mg/kg) и оланзапин (оланц, 0,5 mg/kg). Плъховете при този комбиниран лекарствен режим не показват видимо намаляване на консумацията на хранителни вещества и течности съответно на 10 и 12 ден от лекарствената терапия. Данните представляват средно ± SEM. N = 5-7 животни на група. NS = не е значително.
Няма промени в нивата на глюкозата на гладно след дозиране на хроничен флуоксетин (флуокс, 10 mg/kg) и оланзапин (оланц, 5 mg/g или 0,5 mg/kg). Плъховете под изобразените лекарствени схеми не показват явни разлики в метаболизма на глюкозата. Данните представляват средно ± SEM. N = 5-7 животни на група. NS = не е значително. Нивата на глюкоза на гладно при плъхове обикновено са в диапазона 155–242 mg/dL.
маса 1
Плазмени концентрации на флуоксетин, норфлуоксетин и оланзапин след 18 последователни дни терапия за увеличаване на лекарството.
| Измерване на наркотици | Доза на флуоксетин (10 mg/kg) | Доза на оланзапин (5 mg/kg) |
| Флуоксетин | 344,1 ± 54,2 (нг/мл) | |
| Норфлуоксетин | 695,4 ± 118,4 (ng/mL) | |
| Оланзапин | 178,5 ± 34 (нг/мл) * | |
| Измерване на наркотици | Доза на флуоксетин (10 mg/kg) | Доза на оланзапин (0,5 mg/kg) |
| Флуоксетин | 410,0 ± 36,6 (ng/ml) | |
| Норфлуоксетин | 501,5 ± 114,7 (ng/ml) | |
| Оланзапин | 46,7 ± 4,4 (ng/ml) |
Фактът, че независимо от дозирането на оланзапин и двете групи плъхове са загубили равни количества телесно тегло, е показателно, че тези две явления (т.е. относителни нива на лекарства и динамика на телесното тегло) може да не са причинно свързани. Не са открити забележими промени в мозъчната структура или целостта, както е оценено чрез оцветяване по Нисл и стереологично броене на клетки, проведени в хипоталамуса на плъховете (данните не са показани). Стойностите са средни стойности ± SEM. N = 7 за дозираща група. * P ≤ 0,01 в сравнение с подходящата доза оланзапин.
Дискусия
В настоящото проучване са направени измервания на плазмени концентрации на флуоксетин, норфлуоксетин и оланзапин, за да се оцени тяхната фармакология след 18-дневна комбинирана експозиция на лекарството. Като цяло, плазмените нива на лекарството спадат в рамките на очаквания терапевтичен диапазон, който обикновено се наблюдава при психиатрични пациенти. Например, след 30-дневен прием на 40 mg/ден, плазмените нива на флуоксетин са в диапазона от 90-300 ng/ml при различни популации пациенти [15]. В нашите проучвания върху животни, при доза от 10 mg/kg (IP), постигнатите средни плазмени концентрации са в диапазона 300–400 ng/ml след 18 дни комбинирано медикаментозно лечение. Пероралните дози оланзапин при 20 mg/ден често дават плазмени нива от 20–100 ng/ml при здрави доброволци и при пациенти с шизофрения [30]. Концентрациите ≥80 ng/ml се считат за праг за възникване на неблагоприятни ефекти. В настоящото ни проучване при доза от 5 mg/kg оланзапин средните плазмени нива, постигнати на антипсихотичното лекарство, са били
178 ng/mL. Относително високите нива на оланзапин могат да помогнат да обяснят отчасти хипофагичните и адипсични явления, наблюдавани при плъхове при това конкретно дозиране. Тълкувани по този начин, концентрациите на оланзапин ≥80 ng/mL (както в нашите проучвания) достигат праг за поява на неразположение или неприязъчни ефекти. За разлика от това, животните, изложени на доза от 0,5 mg/kg оланзапин, показват оптимален терапевтичен диапазон на плазмените нива на оланзапин (
47 ng/mL) и нормално поведение при хранене и пиене. Трябва да се отбележи, че дозиращата парадигма, приложена в настоящите ни проучвания, дава флуоксетин, норфлуоксетин и оланзапин в плазмени концентрации, подобни на тези, докладвани от Zhang et al [4] при остър експериментален дизайн. Следователно е възможно при плъхове да се наблюдават малко или никакви значими метаболитни взаимодействия между комбинираното лечение с флуоксетин и оланзапин като функция от хронична експозиция на лекарства. Тази възможност е достойна, тъй като по време на комбинирана терапия с флуоксетин и оланзапин също не се съобщава за клинично значими метаболитни взаимодействия [29]. Поставяйки настоящите данни в рамките на нарастващия набор от експериментални и клинични доказателства, е малко вероятно лекарствените взаимодействия да променят фармакологичния профил на флуоксетин и оланзапин, когато двата психоактивни агента се прилагат едновременно на експериментални животински модели.
Заключения
Методи
Прилагане на животни и лекарства
Експериментални процедури
Измервания на глюкозата
За да се определят относителните нива на глюкоза, всички животни са гладували в продължение на 12 часа в последния ден на инжектиране (т.е. ден 18). Глюкозните серумни нива бяха определени с помощта на Life-Scan Basic Touch Meter (Johnson & Johnson, New Brunswick, NJ). Накратко, 10 μl серум се пипетира като свободно течаща капка върху всяка лента за тест с едно докосване и се отчита в глюкомера за 45 секунди. Нивата на глюкозата на гладно са представени като средни стойности ± SEM в mg/dL.
Анализ за флуоксетин, норфлуоксетин и оланзапин чрез GC-MS
Всички разтворители, използвани за анализи на лекарства, са HPLC клас. Хлороформ и 1-хлорбутан са получени от Burdick & Jackson (Muskegon, MI). Етил ацетат и ацетонитрил са получени от EMD (Gibbstown, NJ). Амониев хидроксид, сертифициран за ACS, е получен от Fisher (Fairlawn, NJ). Аскорбинова киселина е получена от Sigma (Сейнт Луис, Мисури), докато трифлуорооцетният анхидрид е получен от Pierce (Rockford, IL).
Работни разтвори, съдържащи съответно оланзапин, флуоксетин и норфлуоксетин при 10 ng/μL, 1,0 ng/μL и 0,1 ng/μL, бяха приготвени в метанол. Работните разтвори, използвани за изготвяне на стандарти за калибриране и контрол, са получени от различни източници на референтен материал (напр. Флуоксетин) или различно претегляне на един и същ референтен материал (напр. Оланзапин). Стандартите и контролите за калибриране бяха приготвени чрез добавяне на подходящи количества работни разтвори за почистване, отделни силанизирани епруветки с култура 16 × 100 mm, които съдържаха 1 ml празна говежда кръв и 0,2 ml 2,5% аскорбинова киселина. Стандартите за калибриране варират от 1 ng/mL до 1000 ng/mL. Контролите се приготвят при 35 ng/mL, 100 ng/mL и 650 ng/mL.
Обем от 0,25 ml от всяка кръвна проба се прехвърля в чисти силанизирани епруветки с култура 16 × 100 mm. За да се приведе подготовката на пробата до обем от 1 ml, към всяка епруветка се добавя 0,75 ml обем Milli Q H2O. Следователно пробите бяха 4-кратно разреждане в сравнение със стандартите и контролите. 0,2 ml обем 2,5% аскорбинова киселина се добавя към всяка проба в подготвителна епруветка. Пробата, стандартите и контролите бяха извлечени чрез процедура течност/течност. Осемдесет ng флуоксетин-d6 (80 μL от 1 ng/μL флуоксетин-d6 в Milli Q H2O) и 80 ng клозапин (80 μL от 1 ng/μL клозапин в метанол) бяха добавени към всяка епруветка и епруветките след това бяха за кратко завихрен. След това към всяка епруветка се добавят 0,1 ml обем от концентриран амониев хидроксид и 4 ml обем 1-хлорбутан: ацетонитрил (4: 1). На всяка тръба беше поставена чиста винтова капачка, облицована с тефлон. Епруветките се смесват 20 минути с помощта на бутален шейкър и се центрофугират при 2000 rpm в продължение на 10 минути, като се използва IEC центрофуга (Needham, MA). Използвайки чисти, отделни стъклени пастьорски пипети, горният органичен слой от всяка епруветка се прехвърля в чисти, отделни 13 × 100 mm епруветки за култивиране. Органичният слой се изпарява до сухо под струя въздух при 40 ° C с помощта на изпарител Turbo Vap (Zymark Corporation, Hopkinton, MA).
За дериватизация към всяка епруветка се добавят 0,1 ml обем хлороформ и 0,1 ml обем трифлуорооцетен анхидрид. След това върху всяка тръба бяха поставени чисти винтови капачки, облицовани с тефлон. Епруветките се нагряват в продължение на 20 минути при 70 ° С, като се използва сух блоков нагревател. След нагряване тръбите се отстраняват от нагревателя и се оставят да се охладят при стайна температура. След това капачките се отстраняват и епруветките се изпаряват при същите условия, както е описано по-горе. Дериватизираните екстракти се разтварят със 100 μL етилацетат и след това се прехвърлят в чисти, отделни флакони за автоматично вземане на проби.
Анализ на данни
Статистическите сравнения на телесното тегло и нивата на глюкозата бяха проведени с помощта на еднопосочни ANOVA или двустранни t тестове, където е подходящо. Плазмените нива на флуоксетин и оланзапин се анализират чрез t-тест на Student. Нивото на вероятност, интерпретирано като значимо, е P ≤ 0,05.
Принос на авторите
JAP и JMC са участвали в in vivo проучванията и в биохимичните анализи. BHH и JMH участваха в проектирането на проучванията и извършиха статистическия анализ. GT изготви ръкописа, замисли проучването и участва в неговото проектиране и координация. Всички автори прочетоха и одобриха окончателния ръкопис.
Благодарности
Благодарим на Eli Lilly за щедрото дарение на оланзапин, използвано в тези проучвания върху животни. Тази работа беше подкрепена отчасти чрез награда за ресурси на NYCOM за GT и от грант на NIH (# 1R15MH6413-01A1) за JMH. Авторите са задължени на Арън Милър (Институт за нови медии, колеж „Медейл“) за отличната му техническа помощ.
- Лекарството; Флуоксетин; за отзиви за отслабване и съвети
- Динамика на загуба на тегло
- Отслабване IV Лечение Body Bar MedSpa в Колумб
- Тренировки за 13-годишни за отслабване Продажба на изгаряне на мазнини Лазерно лечение Отслабване Rally Centeret
- Какво представлява лечението с панчакарма и как помага панчакармата при отслабване от Prakruti Health