Аида Медина-Урутия
1 Departamento de Endocrinología, Juan Badiano 1, полк. Sección XVI, Tlalpan, Мексико Сити, Мексико
Ангел Р. Лопес-Урибе
1 Departamento de Endocrinología, Juan Badiano 1, полк. Sección XVI, Tlalpan, Мексико Сити, Мексико
Мохамед Ел Хафиди
2 Departamento de Biomedicina Cardiovascular, Juan Badiano 1, полк. Sección XVI, Tlalpan, Мексико Сити, Мексико
Мария дел Кармен Гонсалес-Салазар
1 Departamento de Endocrinología, Juan Badiano 1, полк. Sección XVI, Tlalpan, Мексико Сити, Мексико
Розалинда Посадас-Санчес
1 Departamento de Endocrinología, Juan Badiano 1, полк. Sección XVI, Tlalpan, Мексико Сити, Мексико
Естебан Хорхе-Галарца
1 Departamento de Endocrinología, Juan Badiano 1, полк. Sección XVI, Tlalpan, Мексико Сити, Мексико
Леонардо дел Вале-Мондрагон
3 Departamento de Farmacología, Juan Badiano 1, полк. Sección XVI, Tlalpan, Мексико Сити, Мексико
Хуан Г. Хуарес-Рохас
1 Departamento de Endocrinología, Juan Badiano 1, полк. Sección XVI, Tlalpan, Мексико Сити, Мексико
Свързани данни
Съгласно политиката на BMC, бихме искали да информираме, че всички набори от данни, анализирани по време на настоящото проучване, са достъпни от съответния автор при разумно искане.
Резюме
Заден план
Безалкохолната мастна чернодробна болест (NAFLD) е проблем на общественото здраве, в който липсва одобрено фармакологично лечение. Омега-3 мастните киселини показват, че обръщат NAFLD. Чиа е семе, богато на α-линоленова киселина (ALA), антиоксиданти и фибри; следователно би било полезно да се лекува NAFLD.
Методи
В експериментално проучване с едно рамо, ефектът от 25 g/ден смлян чиа е оценен при 25 пациенти с NAFLD. След две седмици на диетично стабилизиране (основно състояние) и осем седмици на допълнена с чиа изокалорична диета, черният дроб: индексът на затихване на далака и висцералната коремна мазнина (VAF) бяха измерени чрез компютърна томография. Определени са също липиди, липопротеини, свободни мастни киселини (FFA) и ALA плазмени концентрации.
Резултати
Въведение
Успоредно с епидемията от затлъстяване, разпространението на безалкохолната мастна чернодробна болест (NAFLD) значително се е увеличило през последните години [1]. Последните епидемиологични проучвания установиха, че един от трима възрастни има НАЖБП, което е свързано с група метаболитни аномалии [1, 2]. Както беше отбелязано, некачествените диети, характеризиращи се с високо съдържание на фруктоза и недостатъчна консумация на омега-3 мастни киселини, оскъдна физическа активност, излишък във висцерални коремни мазнини (VAF), инсулинова резистентност и генетична чувствителност, се оказаха важни фактори, определящи това чернодробно разстройство [2–4]. Установено е, че захарният диабет тип 2 (T2DM) и коронарната артериална болест (CAD) са най-честите усложнения на NAFLD; въпреки това може да прогресира до цироза и чернодробен карцином [1, 2]. Следователно NAFLD се счита за мултисистемно заболяване и проблем на общественото здраве [1].
Въпреки че нито едно лекарство не е специално одобрено за лечение на NAFLD, последните проучвания показват, че хранителните добавки с омега-3 мастни киселини от морски произход (ейкозапентаенова киселина [EPA]/докозахексаенова киселина [DHA]) и диетата в средиземноморски стил са полезни за лечение на NAFLD [4, 5]. EPA и DHA намаляват интрахепаталното съдържание на мазнини и подобряват метаболитния профил, наблюдаван при тези пациенти, дори при липса на диети за ограничаване на калориите [5]. Въпреки това, поради социално-икономическите и социокултурните характеристики на някои популации, консумацията на тези храни е сложна, увеличавайки интереса към търсене на алтернативи на омега-3 мастни киселини от растителни източници [6].
Терапиите, които се фокусират върху използването на функционални храни, богати на разнообразни фитохимикали, моно/полиненаситени мастни киселини, антиоксиданти, минерали и фибри, са показали антиоксидантни, противовъзпалителни и понижаващи липидите ефекти [7, 8], които може да бъде полезен при пациенти с NAFLD [6]. Семената от чиа (Salvia hispanica) са най-богатият растителен източник на омега 3-мастни киселини, антиоксиданти и фибри [9]. Въпреки че някои животински модели предполагат, че чиа може да се използва като алтернатива за намаляване на интрахепаталното съдържание на мазнини [10, 11], ефектът му върху пациентите с NAFLD все още не е проучен. Следователно целта на настоящото проучване е да се анализира дали консумацията на изокалорична диета, допълнена с чиа, може да подобри NAFLD, VAF и метаболитни аномалии при пациенти с NAFLD.
Материали и методи
Участници
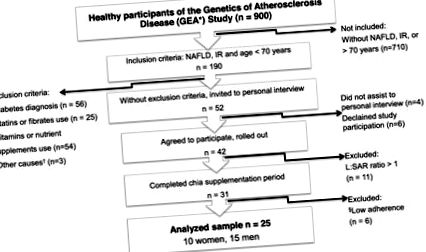
Участниците бяха избрани от контролната група на изследването за генетика на атеросклеротична болест (GEA, за инициалите на испански), проведено в Института за национална кардиология на Игнасио Чавес в Мексико Сити, Мексико (фиг. 1). Допустими субекти бяха тези на възраст под 70 години (30–69 години) с диагноза NAFLD, потвърдена чрез компютърна томография (КТ) и с инсулинова резистентност, оценена чрез индекса на инсулинова резистентност на хомеостатичния модел (HOMA-IR) [12]. Критерии за изключване бяха предишна диагноза на диабета, употреба на хипогликемични или хиполипидемични лекарства, нестабилно телесно тегло (вариация> 5% в рамките на предходния 3-месечен период), консумация на витамини, билкови или хранителни добавки, стомашно-чревни, бъбречни или чернодробни заболявания и наличие на хранителни, психиатрични или когнитивни нарушения, които биха затруднили разбирането на инструкциите за изследване и тяхното съответствие. Кандидатите, които са приели да участват в проучването, са подписали писмен формуляр за информирано съгласие преди попълването на каквато и да е оценка.
Хранителна намеса и оценка на приема на храна
Антропометрична оценка
Антропометричните измервания са получени в съответствие с разпоредбите на Международното общество за напредък на кинантропометрията (ISAK) от сертифициран диетолог. Теглото и височината на пациентите са регистрирани преди 8:00 сутринта в условия на гладно; участниците трябваше да свалят обувки и всички външни кърпи и тежки джобни предмети. Използвани са цифрова везна (Soehnle Professional Design 7830, Leifheit, Насау, Германия) и стенен стадиометър SECA 220 (seca GMBH и Co. KG, Хамбург, Германия), с точност съответно 0,1 kg и 0,1 cm. Индексът на телесна маса (ИТМ) се изчислява като тегло (kg)/височина (m 2). Обиколката на талията беше измерена с неразтегната лента (Lufkin W606PM 6 mm × 2 m, Zapopan, Jal. Mexico). Измерването е направено в два екземпляра, като пациентът е без дрехи около кръста, по средата между най-ниското ребро и илиачния гребен, средните стойности са средни; обаче беше направено трето измерване, ако те се различаваха повече от 0,5 cm.
Лабораторни изследвания
След 10-часово гладуване и 20 минути в седнало положение, венозна кръв се събира в епруветки за анализ без антикоагулант и в епруветки с K2-EDTA (1,8 mg/ml). Концентрации на глюкоза, общ холестерол (TC), триглицериди (TG), липопротеинов холестерол с висока плътност (HDL-C), аланин аминотрансфераза (ALT), аспартат аминотрансфераза (AST), гама глутамил транспептидаза (GGT) и пикочна киселина (UA) бяха определени с помощта на директни стандартни ензимни колориметрични методи (Roche Diagnostics, Mannheim, Германия), в анализатор COBAS c311. Концентрацията на липопротеиновия холестерол с ниска плътност (LDL-C) е оценена с помощта на формулата на DeLong [15]. Възпроизводимостта и прецизността на тези определяния са оценени от Центъра за контрол и предотвратяване на заболяванията Програма за стандартизация на липидите (LSP-CDC, Атланта, Джорджия, САЩ). Свободните мастни киселини (FFA) се определят в плазмата чрез ензимно-колориметричен анализ (Wako Diagnostics, Chuo-Ku Osaka, Япония).
Стойностите на чернодробните ензими се считат за високи, когато ALT, AST или GGT са ≥ процентил 75 (ALT: 23 U/L и 30 U/L, AST: 27 U/L и 29 U/L, GGT: 21 U/L и 28 U/L, за жени и мъже; съответно). Тези гранични стойности са получени от 101 мъже и 180 жени в проучването GEA, без затлъстяване и нормални стойности на липидите, глюкозата и кръвното налягане.
Анализ на общата мастна киселина в плазмата (TFA)
Към 100 μL плазма, 50 μL разтвор на хептадеканова киселина (C17: 0, Sigma Co., Сейнт Луис, МО, САЩ) (1 mg/ml) в хлороформ се добавя като вътрешен стандарт. Всички разтворители и химикали са с аналитично качество от J. T Baker (Avantor Performance Materials, Central Valley, PA, USA). Впоследствие плазмените липиди бяха екстрахирани три пъти със смес хлороформ: метанол (1: 2 v/v), чрез енергично завихряне за 1 min, съгласно метода на Folch’s [16]. След центрофугиране органичният слой се събира, комбинира и разтворителят се изпарява при 40 ° С под азотен поток. Трансметилирането на мастна киселина се извършва незабавно при 80 ° С, в 2-милилитрова смес от метанол: H2SO4 (2%). Метиловите естери на мастните киселини се екстрахират три пъти с 2 ml n-хексан, който се отделя и суши под азот. Сухият остатък се разтваря в 50 μL н-хексан и 1 μL се анализира в газов хроматограф Shimadzu GC-8A, снабден с пламъчен йонизационен детектор (Shimadzu, Киото, Япония) и капилярна колона SP2330 с дължина 25 m и 0,25 mm вътрешен диаметър (SUPELCO, Bellefonte, PA, САЩ). Пиковете на мастните киселини бяха идентифицирани чрез използване на компонента FAME Mix на Supelco 37 (> CRM47885, SUPELCO, Bellefonte, PA, USA). При всеки тест за екстракция се пуска плазмена контролна проба; Изменението на коефициента на ALA между анализите е по-ниско от 13%.
Състав на мастните киселини на Chia
Семената от чиа се смилат и анализират за съдържание на мастни киселини съгласно процедурите AOAC [17], модифицирани в нашата лаборатория. Накратко, 100 mg смлени семена в присъствието на 100 μg хептадеканова киселина (C17: 0), като вътрешен стандарт, бяха разбъркани в 2 ml смес хлороформ/метанол (2: 1, v/v), съдържаща 0,002% бутилиран хидрокситолуен (BHT) като антиоксидант, в ледено легло за една нощ. В края на този период се добавят 1 mL разтвор на NaCl (0.8%) и се завихря за 1 минута; разтворителят се декантира и събира. Тази стъпка се повтори два пъти. Органичният слой се дехидратира с анхидрид натриев сулфат, филтрува се и се изпарява под лек поток от азот. Мастните киселини на остатъка се транстерифицират до съответния метилов естер и се анализират чрез газова хроматография, както е описано по-горе.
Изследване с компютърна томография
Компютърната томография е валидиран метод за измерване на VAF [18] и оценка на NAFLD [19]. В настоящото проучване тези измервания са получени с помощта на 64-срезов скенер (Somatom Cardiac Sensation 64, Forchheim, Бавария, Германия). За да се определи съотношението на затихване на черния дроб: далак (L: SAR), беше получено еднорезово CT сканиране на ниво T11 – T12 или T12 – L1. Мастният черен дроб се определя като съотношение на затихване на черния дроб/далака под 1,0, което е предложено като праг за откриване на умерена или тежка стеатоза (≥30%) от хистологията [19]. За да се изчисли количеството на общата мастна тъкан в корема (TAF) и VAF, беше извършено сканиране с един резен на нивото на L4 – L5 и площта беше изразена в квадратни сантиметри (cm 2). Подкожната коремна мастна тъкан (SAF) се изчислява чрез изваждане на VAF от зоната на TAF.
Статистически анализ
Данните са представени като средно ± стандартно отклонение, медиана (интерквартилен обхват) или разпространение. Сравненията бяха направени чрез сдвоени тестове на Student’s t, Wilcoxon matched-двойки с ранг или Chi-квадрат, според случая. P стойности 1. Всички пациенти завършиха задоволително 8 седмици чиа интервенция при 25 g/ден, със средно придържане от 93 ± 8%. Характеризирането на мастните киселини на чиа разкрива, че ALA (65%), линолова (20%), олеинова (6%), палмитинова (6%) и стеаринова (3%) киселини са основните компоненти на семената. След добавяне на чиа се регистрира увеличение на ALA в плазмата (75% [40–125%]) и по-висока консумация на диетични фибри (55% [17–92%]) (Таблица 2). В началото на проучването четирима пациенти съобщават за скромно и преходно стомашно-чревно разстройство, което не заслужава оттеглянето им от проучването.
маса 1
Общи характеристики на изследваните пациенти и разпределение на мазнините в корема в тялото на изходно ниво и след 8 седмици от 25 g/ден консумация на чиа
| Възраст (години) | 58,0 ± 7,7 | ||||||||||||||||
| Мъже жени | 15/10 | ||||||||||||||||
| Придържане (%) | 93,0 ± 8,0 | ||||||||||||||||
| ИТМ (kg/m 2) | 30,6 ± 3,5 | 29,9 ± 3,5 | 2) | 538 (433–631) | 501 (410–568) | 2) | 317 (255–394) | 308 (248–386) | 2) | 188 (164–230) | 180 (150–234) | a (%) | 26,3 ± 5,6 | 30,4 ± 4,4 | 0,001 | ||
| Въглехидрати а (%) | 51,1 ± 7,2 | 48,8 ± 5,5 | NS | ||||||||||||||
| Протеин а (%) | 22,6 ± 4,9 | 20,8 ± 3,6 | NS | ||||||||||||||
| Общо фибри (g/ден) | 17,3 (13,8–33,4) | 30,2 (21,7–34,6) | a Изразен като процент от общата консумирана енергия (1 kcal = 4,186 kJ) * сдвоен t-тест на Student или тест на Wilcoxon за съвпадение на двойки, както съответства | ||||||||||||||
Промените в метаболитния профил след интервенция с чиа бяха умерени, със значително намаляване на общия холестерол, не-HDL холестерола и FFA (Таблица 3). Допълнителен анализ показа, че при пациенти с първоначални високи концентрации на триглицериди (TG ≥ 150 mg/dL, n = 16), подобрението на FFA (mmol/L) е по-голямо (базално: 0.74 [0.59–0.85], пост-хиа: 0,57 [0,47-0,64]; P = 0,02). По отношение на тестовете за чернодробна функция, няма разлика в средните концентрации (Таблица (Таблица 3), 3) или в разпространението на анормални стойности (данните не са показани) след добавяне на чиа.
Таблица 3
Биохимични параметри на изходно ниво и след 8 седмици от 25 g/ден консумация на чиа
| TC (mmol/L) | 4,8 (4,3–5,2) | 4,6 (4,2–4,6) | (Таблица 1). 1). Анализът на коремното разпределение на мазнините разкрива намаляване на TAF, главно поради по-голямата загуба на VAF (- 9%) по отношение на депозита на SAF (- 5%). Освен това, 52% от пациентите показват регресия на NAFLD (фиг. 2, панел А), с увеличение от 22% в съотношението затихване на черния дроб: далак (фиг. (Фиг. 2, 2, панел Б). Подобрението в индекса на затихване е по-забележим при пациенти със затлъстяване (24%) в сравнение с тези с наднормено тегло (9%). Това подобрение е съпътстващо с по-голямо увеличение на ALA и консумацията на фибри (панел C и D). |
Ефекти от добавките с чиа върху разпространението на алкохолна мастна чернодробна болест (NAFLD) (а), черен дроб: съотношение на затихване на далака (L: SAR) (б), плазмен ALA (° С) и прием на диетични фибри (д). NAFLD се дефинира като L: SAR 150 mg/dL). Тези открития предполагат подобрение на чувствителността към инсулин на мастната тъкан и намаляване на de novo липогенезата в резултат на приема на чиа.
Силни страни и ограничения
Основната сила на настоящото проучване беше томографският анализ на коремните мазнини, който позволи да се оцени ефектът на чиа отвъд телесното тегло и неговият ефект върху мастните депа с по-голяма патофизиологична трансцендентност. Въз основа на предишни проучвания е приложена адекватна доза смляно семе, което позволява по-голяма бионаличност на неговите хранителни вещества и максимален прираст в ALA; освен това придържането към лечението е било по-високо от 90% и това е потвърдено чрез количествено определяне на ALA в плазмата.
Най-важното ограничение беше липсата на контролна група; предишни проучвания обаче се съгласяват относно трудността да се получи адекватно плацебо. В плацебо контролирано проучване на чиа, авторите анализират заслепения дизайн на участниците, установявайки, че 60% от участниците в плацебо рамото са признали, че са на плацебо лечение [20]. От друга страна, контролираните проучвания използват източник на фибри като плацебо, въпреки че не е изяснено дали ALA и фибрите имат независими или синергични благоприятни ефекти. Изследвания с кръстосан дизайн могат да бъдат подходящи за потвърждаване на настоящите резултати. За да се избегнат нежелани реакции от страна на стомашно-чревния тракт, се препоръчва консумация на смлян чиа от закуска до обяд (винаги преди 18:00 ч.); обаче абсорбцията на липиди и метаболизмът могат да бъдат по-високи в началото на активния/будния период [35]. Следователно балансът между тези въпроси трябва да бъде разгледан при по-нататъшни проучвания. И накрая, допълнително ограничение е, че подобрението на NAFLD е оценено чрез томография. Въпреки че чернодробната биопсия е златният стандарт за това измерване, показа се, че томографията е метод, който позволява да се идентифицират интрахепаталните мастни натрупвания, по-високи от 30%, с чувствителност и специфичност от 80% [36].
Заключения
Резултатите от настоящото проучване показват, че 25 g/ден смлян чиа подобрява NAFLD. Поради своя състав, чиа може да бъде достъпен растителен източник на омега-3 мастни киселини, антиоксиданти и фибри. Тези фитохимикали имат потенциала да предотвратят появата на метаболитни аномалии, напреднали стадии на NAFLD и развитие на T2DM и CAD при пациенти с NAFLD. Функционалните храни се предлагат като част от иновативни терапии за лечение на кардиометаболитни заболявания. Въпреки че резултатите от настоящото проучване разширяват тази информация, са необходими още проучвания, за да се консолидират тези хранителни вещества като терапевтични алтернативи.
Благодарности
Авторите благодарят на персонала на отделите по ендокринология и томография на Националния институт по кардиология Игнасио Чавес, както и на участниците в изследването.
- Борете се с безалкохолната мастна чернодробна болест с тези храни във вашата диета - здраве - Hindustan Times
- Ефектите на мелатонин без пълни текстове върху безалкохолните мастни чернодробни заболявания са свързани с
- Обезщетения за инвалидност за безалкохолни мастни чернодробни заболявания Изисквания за допустимост Gillette Law
- Добавка на Чиа и безалкохолна мастна чернодробна болест - изглед в пълен текст
- Диета с мазнини на черния дроб Диета с мастни заболявания на черния дроб 5 най-добри храни, които ще ви помогнат да отслабнете и да намалите мазнините в