1 Секция за разследваща медицина, Медицински факултет, Имперски колеж в Лондон, 6-ти етаж, сграда на Британската общност, болница Хамърсмит, Du Cane Road, Лондон W12 0NN, Великобритания
Резюме
Затлъстяването е основен проблем за общественото здраве в световен мащаб. Настоящите фармакологични лечения са до голяма степен неуспешни. Определянето на сложните пътища, които регулират приема на храна, може да подпомогне разработването на нови лечения. Оста хипоталамус-хипофиза-щитовидна жлеза (HPT) има добре известни ефекти върху разхода на енергия, но нейната роля в регулирането на приема на храна е по-слабо характеризирана. Данните сочат, че оста HPT може пряко да повлияе на приема на храна. Дисфункцията на щитовидната жлеза може да има клинично значими последици върху апетита и телесното тегло. Класически се смяташе, че тези ефекти се медиират от периферните ефекти на тиреоидния хормон. Напоследък обаче се смята, че местната регулация на хормона на щитовидната жлеза в централната нервна система (ЦНС) играе важна роля за физиологично регулиране на апетита. Тази статия се фокусира върху ролята на HPT и хормона на щитовидната жлеза в апетита и предоставя доказателства за потенциални нови цели за агенти срещу затлъстяването.
1. Въведение
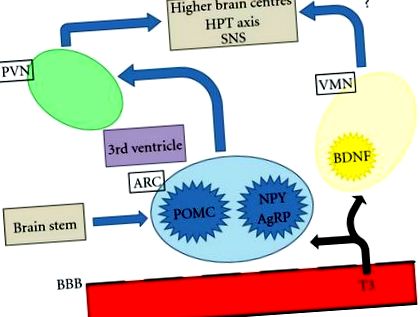
Затлъстяването, неговите усложнения и свързаната с това смъртност са основните проблеми на общественото здраве в световен мащаб. Основните области на централната нервна система (ЦНС), важни за регулирането на апетита, са хипоталамусът и мозъчният ствол. Хипоталамусът интерпретира и интегрира аферентни сигнали от периферията и мозъчния ствол, за да модулира еферентни сигнали, които регулират приема на храна и разхода на енергия. Невронните и хормоналните периферни сигнали предават информация, включително остри хранителни състояния и енергийни запаси. Хипоталамусът е подразделен на редица взаимосвързващи ядра, включително паравентрикуларното ядро (PVN), вентромедиалното ядро (VMN) и дъговидното ядро (ARC), които са особено важни за регулирането на енергийната хомеостаза. ARC се намира в близост до средната височина, където кръвно-мозъчната бариера е непълна и по този начин е в добра позиция да реагира на циркулиращите фактори, участващи в апетита и приема на храна [1]. Последните данни показват, че хормоните на щитовидната жлеза могат да имат достъп до ARC и други региони на хипоталамуса, за да регулират апетита (Фигура 1).
Добре установено е, че оста хипоталамус-хипофиза-щитовидна жлеза (HPT) регулира телесното тегло. Известно е, че тиреоидните хормони влияят на скоростта на метаболизма. Дисфункцията на щитовидната жлеза може да има клинично значими последици върху апетита и телесното тегло. Хипотиреоидизмът класически причинява намален базален разход на енергия [2] с увеличаване на теглото [3, 4]. И обратно, хипертиреоидизмът увеличава енергийните разходи и намалява телесното тегло [5–7]. Традиционно се предполага, че именно това намалено телесно тегло задвижва хиперфагията, която може да бъде характерна особеност при хипертиреоидизъм. Последните данни обаче показват, че оста HPT може да играе пряка роля в хипоталамусната регулация на апетита, независимо от ефектите върху енергийните разходи. Класически хипоталамусният тиреотропин-освобождаващ хормон (TRH) стимулира освобождаването на тиреоид-стимулиращия хормон (TSH) от предната част на хипофизната жлеза, което след това стимулира освобождаването на двата тиреоидни хормона, три-йодотиронин (Т3) и тироксин (Т4). Докладите предполагат, че всички тези сигнални молекули могат пряко да повлияят на приема на храна [8-11]. Подобреното разбиране на ролята на оста на HPT и хормона на щитовидната жлеза в апетита може да идентифицира нови цели за агенти за затлъстяване.
2. Ефекти на тиреоидните хормони върху приема на храна (Таблица 1)
Има добре характеризирани ефекти на гладуването върху експресията на хипоталамусния TRH. Смята се, че това основно регулира оста на HPT в периоди на ограничена наличност на храна, като по този начин намалява приема на храна. Съобщава се обаче, че TRH има преки аноректични ефекти, което предполага, че може да регулира приема на храна, независимо от ефектите върху оста на HPT. При гризачите централното приложение на TRH намалява приема на храна [8, 12, 13]; подобни ефекти върху приема на храна се наблюдават след периферно приложение [14].
Доказано е също, че TSH намалява приема на храна, когато се инжектира централно в плъхове [8]. Има доказателства, че TSH от pars tuberalis участва в фотопериодичния отговор при птици и гризачи и по този начин е възможно TSH да участва в сезонните промени в приема на храна и телесното тегло, които се срещат при някои видове [15–17].
Хиперфагията, свързана с хипертиреоидизъм, може да е резултат от хормони на щитовидната жлеза, действащи директно върху апетитните вериги на ЦНС. Т3 стимулира директно приема на храна на нивото на хипоталамуса. При модели на гризачи, периферното и централното приложение на хипоталамуса на Т3 увеличава приема на храна [9-11].
Има няколко механизма, постулирани да медиират орексигенните ефекти на хормоните на щитовидната жлеза. ARC съдържа две различни невронални популации, регулиращи хомеостазата на енергията. Една субпопулация изразява про-опиомеланокортин (POMC) ген, който кодира аноректичния невропептид алфа-меланоцит-стимулиращ хормон (α-MSH). Другият изразява орексигенните фактори невропептид Y (NPY) и свързания с агюти протеин (AgRP). Съобщава се, че периферното приложение на Т3 увеличава хипоталамусната NPY иРНК и че интрацеребровентрикуларното (ICV) приложение на NPY Y1 рецепторен антагонист притъпява индуцираната от Т3 хиперфагия, което предполага, че Т3 може да повиши апетита чрез NPY [10]. Съобщава се също, че приложението на Т3 също намалява експресията на POMC на хипоталамуса [10]. Друго проучване не открива промени в експресията на хипоталамусния невропептид в отговор на периферното приложение на Т3, въпреки че това може да отразява различните дози на Т3, приложени [9].
Въпреки това, ефектите на хормоните на щитовидната жлеза върху приема на храна може да не бъдат медиирани директно от ARC. Директното приложение на T3 във VMN, но не и ARC, увеличава приема на храна при плъхове [9]. Тъй като е известно, че веригите за регулиране на апетита в ARC се променят от промени в HPT, може да има индиректен ефект на ARC чрез VMN, което позволява на intra-VMN T3 да увеличи приема на храна. В съответствие с това има възбуждащи входове в POMC невроните, които произхождат от VMN [18].
Счита се, че ензимът 5 'аденозин монофосфат-активирана протеин киназа (AMPK) действа като сензор, който регулира хомеостазата на клетъчната енергия. AMPK се активира чрез фосфорилиране, а AMPK активирането в ARC увеличава приема на храна [25]. Периферно прилаганият Т3 увеличава фосфорилирането на хипоталамусния AMPK, което по този начин може да медиира орексигенните ефекти на Т3 [11].
Производните на щитовидната жлеза също са замесени в регулирането на апетита. G-свързан с протеин рецептор 1, свързан с амин (TAAR1), се експресира в хипоталамуса на плъхове и е свързан с регулирането на енергийната хомеостаза. Производното на тиреоидния хормон 3-йодотиронамин (T1AM), ендогенен биогенен амин, е мощен агонист на TAAR1. Изследванията на гризачи показват, че T1AM значително увеличава приема на храна при плъхове, когато се прилага интраперитонеално, ICV или директно в ARC [26]. Физиологичното значение на тези ефекти обаче остава неизвестно.
Рецепторите на тиреоидния хормон (TR) или рецепторите, които медиират ефекта на тиреоидните хормони върху апетита, са неизвестни. Има два основни типа рецептори за тиреоиден хормон - рецептор за тиреоиден хормон α (THRA) и тиреоиден хормон рецептор β (THRB), всеки кодиран от отделен ген. Тези гени се сменят последователно, за да генерират три основни силно хомоложни изоформи на ядрен рецептор (TRα1, TRβ1 и TRβ2) със специфични тъканни разпределения [27]. Трите основни изоформи свързват Т3 с висок афинитет и регулират медиираната от щитовидната жлеза транскрипция. TRα е основната изоформа, регулираща Т3 активността в сърцето, скелетните мускули, костите и мозъка; TRβ е основната изоформа, регулираща Т3 активността в черния дроб. Мастната тъкан изразява и двете TRα и TRβ. TRβ1 се изразява в повечето тъкани, докато TRβ2 се изразява единствено в хипоталамуса, хипофизата, кохлеята и ретината [28, 29]. И трите изоформи се експресират в човешкия хипоталамус в редица ядра, включително инфундибуларното ядро, човешкият еквивалент на ARC и супраоптичните и паравентрикуларните ядра.
Въпреки че хормоните на щитовидната жлеза могат директно да увеличат приема на храна в хипоталамуса, доказано е, че селективно насочените подтипове TR имат полезни метаболитни ефекти. Активиране на TRβ рецептор намалява телесното тегло при затлъстели плъхове [30], което може да е резултат от увеличаване на скоростта на метаболизма. Следователно, TRβ агонисти са предложени като лечения за затлъстяване. Насочване на TR с TRβ-селективният агонист може да определи дали тези агенти адресират метаболитните ефекти на тиреоидния хормон, без ефекти върху TRα-експресиращи тъкани като сърцето [30]. Периферно приложение на TRβ-селективният агонист на плъхове по време на хранене с диета с високо съдържание на мазнини предотвратява очакваното увеличаване на мастната маса, непоносимост към глюкоза и хипертриглицеридемия [31]. Тези ефекти могат да отразяват увеличения разход на енергия, наблюдаван при гризачи, третирани с TRβ-селективен агонист, а не ефектите на тиреоидните хормони върху апетита [32]. Необходима е по-нататъшна работа за идентифициране на рецептора, отговорен за орексигенните ефекти на Т3 в хипоталамуса.
3. Ефекти от хранителното състояние върху тиреоидните хормони
Намаляването на TRH в отговор на гладуване може да бъде важно, тъй като TRH има пряк аноректичен ефект, когато се инжектира в хипоталамуса [13]. Възможно е да има различни TRH невронални популации, регулиращи оста на HPT и регулиращи апетита.
В периоди на ограничена наличност на храни има централно регулиране на оста на HPT. Нивата на серумните Т4 и Т3 падат по време на гладуване при хора [33] и гризачи [34, 35]. Тъй като по-голямата част от Т3 при гризачите идва от щитовидната жлеза, смята се, че лишаването от храна може да доведе до спад в освобождаването на Т4 и Т3. Това вероятно е вторично за намаляването на хипоталамусната експресия на TRH, ефект, който може да бъде медииран от мастния хормон лептин (Фигура 2).
Лептинът е адипоцитокин, който циркулира пропорционално на бялата мастна тъкан и съобщава на ЦНС информация относно запасите от телесни мазнини. Прилагането на лептин може да обърне предизвиканите от глад промени в оста на HPT [34, 36, 37]. Прилагането на лептин частично предотвратява намаляването на общия Т4, ясно наблюдавано при гладни мишки [34]. Хората и мишките с мутации на лептинов рецептор или самият лептин проявяват централен хипотиреоидизъм [38, 39], който се подобрява при хора с дефицит на лептин чрез прилагането на лептин [40]. Лептинът може директно да регулира експресията на TRH в PVN и може индиректно да регулира TRH чрез ефекти в ARC. Лептинът се увеличава α-Освобождаване на MSH и намаляване на освобождаването на AgRP, което води до понижаване на регулацията на експресията на TRH. Съществуват също така нови доказателства за съществуването на независим от меланокортин път, по който лептинът може да повлияе на HPT оста; съвместното лечение с мощен антагонист на меланокортин 4 рецептора (MC4R) намалява, но не блокира напълно действието на лептина при възстановяване на общия Т4 в модел на гризачи [41].
Промените в оста на HPT и нивата на периферните тиреоидни хормони са в противоречие с докладваните ефекти на тиреоидните хормони върху апетита. Ако хормоните на щитовидната жлеза физиологично повишат апетита, ще се предвиди, че те ще се увеличават, а не намаляват в глада. Данните сочат, че вместо системните нива на щитовидните хормони, локалните концентрации на тиреоидни хормони в ЦНС са важни за регулирането на апетита.
4. Централни промени в нивата на T3, опосредствани от D2 и D3
Група ензими, известни като дейодинази (тиоредоксин фолд ензими) регулира активирането и инактивирането на Т3 и Т4. Тези ензими са отговорни за регулирането на нивата на централния щитовиден хормон. Има три вида дейодиназа, всеки с активен център, съдържащ аминокиселината селеноцистеин, която е критична за реакцията на дейодиране, катализирана от тези ензими. Дейодиназите действат чрез селективно отстраняване на йод от Т4 и неговите производни. Йодът може да бъде отстранен от вътрешния (тирозил) или външния (фенолен) пръстен. Дейодиназа 1 (D1) се експресира предимно в черния дроб, бъбреците и щитовидната жлеза при хора и гризачи. Дейодиназа 2 (D2) и дейодиназа 3 (D3) обаче са силно експресирани в ЦНС, с известна периферна експресия. Експресията на всеки ензим се регулира индивидуално от хормона на щитовидната жлеза. В рамките на хипоталамуса експресията и активността на D2 и D3 зависят от хранителните обстоятелства, което води до специфични за тъканите промени в наличността на хипоталамуса Т3, които могат да бъдат важни при регулирането на приема на храна и разхода на енергия (Фигура 3).
Експресията на хипоталамус D2 не се регулира само от състоянието на щитовидната жлеза. При гризачите гладуването също увеличава експресията и активността на хипоталамуса D2 [9, 37] и този ефект не се обръща от системното приложение на Т4 [45]. Той обаче може да бъде обърнат чрез прилагане на лептин [37], което предполага, че той е по-важен в енергийната хомеостаза от оста на HPT. Лептинът възстановява хипоталамусните и хипофизните компоненти на оста на HPT по време на гладуване, но директно притъпява отговора на щитовидната жлеза, което води до ниски плазмени Т4 и Т3 [37]. Следователно, нормализирането на тиреоидния хормон може да зависи от промени в дейностите на дейодиназата и дългосрочната стимулация на щитовидната жлеза от TSH, за да се противопостави на тези директни инхибиторни ефекти на лептина върху щитовидната жлеза.
Активността на D2 е особено висока в ARC и средната възвишеност [52], където се изразява в астроцитите и таницитите. Процесите на съдържащите D2 таницити са в пряк контакт с NPY/AgRP невроните на ARC, които също експресират UCP2 [53]. Смята се, че отделящият протеин 1 (UCP1) е неразделна част от процеса на свързаната с кафяви мазнини неотклоняваща се термогенеза, тъй като той разсейва енергията под формата на топлина [54]. Ролята на вътрешния митохондриален мембранен разединителен протеин 2 (UCP2) е по-слабо дефинирана и специфична за тъканите, но тя подлежи на регулиране от Т3 [55].
5. Обобщение
Локалната регулация на хормоните на щитовидната жлеза в ЦНС може физиологично да регулира апетита. Превключването между индуцирането на експресия на D2 и D3 може фино да контролира концентрациите на хипоталамусния тиреоиден хормон. Сега е необходима по-нататъшна работа, за да се характеризират пътищата, по които хормоните на щитовидната жлеза регулират приема на храна. Определянето на механизмите, чрез които хормоните на щитовидната жлеза регулират енергийната хомеостаза, може да подпомогне разработването на терапии за управление на затлъстяването.
Съкращения
| Т2: | 3 ′, 3′-дийодтиронин |
| AMPK: | 5 ′ аденозин монофосфат активирана протеин киназа |
| AgRP: | Агути-свързан протеин |
| α-MSH: | Алфа-меланоцит-стимулиращ хормон |
| ДЪГА: | Дъговидно ядро |
| BBB: | Кръвно-мозъчна бариера |
| BDNF: | Мозъчен невротрофичен фактор |
| ЦНС: | Централна нервна система |
| D1: | Дейодиназа 1 |
| Dio1: | Ген на дейодиназа 1 |
| D2: | Дейодиназа 2 |
| Dio2: | Ген на дейодиназа 2 |
| D3: | Дейодиназа 3 |
| Dio3: | Ген на дейодиназа 3 |
| HPT: | Хипоталамо-хипофизарно-щитовидна жлеза |
| ICV: | Интрацеребровентрикуларна |
| IP: | Интраперитонеално |
| MC4R: | Меланокортин 4 рецептор |
| MCT8: | Монокарбоксилатен транспортер 8 |
| NPY: | Невропептид Y |
| OATP1C1: | Органичен анион, транспортиращ полипептид 1с1 |
| PVN: | Паравентрикуларно ядро |
| POMC: | Про-опиомеланокортин |
| rT3: | Обратен T3 |
| SF1: | Стероидогенен фактор-1 |
| TR: | Рецептор на щитовидната жлеза |
| TSH: | Тиреостимулиращ хормон |
| TRH: | Тиротропин освобождаващ хормон |
| T4: | Тироксин |
| T3: | Три-йодотиронин |
| UCP1: | Отделяне на протеини 1 |
| UCP2: | Отделяне на протеин 2 |
| VMN: | Вентромедиално ядро. |
Благодарности
A. Amin се подкрепя от схемата за финансиране на Центъра за биомедицински изследвания на Националния институт за здравни изследвания (NIHR). W. S. Dhillo се финансира от награда на Националния институт за здравни изследвания и специалист по научни изследвания и награда Wellcome Trust Value in People. К. Г. Мърфи получава финансиране от Съвета за изследване на биотехнологиите и биологичните науки (BBSRC). Департаментът се финансира от Националната схема за финансиране на НИПЧ за биомедицински изследвания, BBSRC и по FP7-ЗДРАВЕ-2009-241592 (Европейски съюз) EurOCHIP.
Препратки
- Значението на хормоните, щитовидна жлеза; Диета за имунната система Las Colinas Compounding; Уелнес
- Централната нервна система, панкреатичните хормони, храненето и затлъстяването - ScienceDirect
- Ефектите от диетата върху тежестта на заболяването на централната нервна система Една част от лаборатория към лаборатория
- Изненадващо въздействие на вашите хормони върху вашето зрение
- Суши, свързано със заболяване на щитовидната жлеза