Резюме
Вътреутробната метаболитна среда на майката е важна както за краткосрочното, така и за дългосрочното развитие на потомството. Въпреки че лошият растеж на плода остава важен фактор по отношение на дългосрочния резултат, свръхрастежът на плода придобива по-голямо значение поради увеличаването на затлъстяването в популациите на света. Затлъстяването на майката и гестационният диабет са най-честите метаболитни усложнения на бременността, свързани с прекомерно израстване на плода и по-точно затлъстяване.
Жените с гестационен диабет имат повишена инсулинова резистентност и неадекватен инсулинов отговор в сравнение с контролите, съобразени с теглото. Гестационният диабет увеличава риска от майчино хипертонично заболяване (прееклампсия), както и от цезарово сечение. При раждането новороденото е повишило затлъстяването и е изложено на риск от нараняване при раждане. Многобройни проучвания съобщават, че децата на жени с гестационен диабет имат по-голямо разпространение на детското затлъстяване и непоносимост към глюкоза; дори при концентрации на глюкоза, по-ниски от използваните в момента за определяне на гестационен диабет, в сравнение с нормогликемичните жени.
Затлъстелите жени също имат повишена инсулинова резистентност, инсулинов отговор и възпалителни цитокини в сравнение със средно тежки жени преди и по време на бременност. Те също са изложени на повишен риск от нарушения на метаболитния синдром по време на бременност, което е хипертония, хиперлипидемия, глюкозна непоносимост и нарушения на коагулацията. Аналогично на жените с гестационен диабет, новородените при жени със затлъстяване са по-тежки при раждането, поради повишената мастна тъкан, а не слабата телесна маса. По същия начин тези деца имат повишен риск от детско затлъстяване и метаболитна дисрегулация. Следователно, предубедителният и перинаталният период предлага уникална възможност за промяна както на краткосрочните, така и на дългосрочните рискове както за жената, така и за нейното потомство.
Въведение
Таблица 1А.
ATP III клинична идентификация на метаболитния синдром 2
| Коремно затлъстяване, дадено като обиколка на талията | |
| Мъже | > 102 см (> 40 инча) |
| Жени | > 88 см (> 35 инча) |
| Триглицериди | > 150 mg/dl |
| HDL холестерол | |
| Мъже | 130 /> 85 mmHg |
| Глюкоза на гладно | > 110 mg/dl |
HDL, липопротеин с висока плътност.
Гестационен диабет
Патофизиология
Гестационният диабет е определен от 4-тата международна работна среща-конференция по GDM е: „непоносимост към въглехидрати с различна степен на тежест, с начало или първо разпознаване по време на бременност“. 6 Въпреки това, през 2009 г. Международната асоциация по диабет в проучвателни групи за бременност, международна консенсусна група диабетолози и акушер-гинеколози, включително Американската диабетна асоциация, препоръча на високорисковите жени, за които е установено, че имат диабет при първоначалното си посещение, да получат диагноза явна а не GDM, използвайки критериите, препоръчани в таблица 2. 7 За разлика от жените с нормален глюкозен толеранс, основната патофизиология на GDM е налице преди бременността. Онези, предназначени да развият GDM, показват намалена инсулинова чувствителност преди бременността, като последната е с наднормено тегло и затлъстяване. 8 Тези жени също имат неадекватен инсулинов отговор за поддържане на нормогликемия, 9 колкото биха открили при лица с диабет тип 2. Много малък брой случаи на GDM могат да представляват или появата на диабет тип 1, или наследствени генетични дефекти, каквито могат да бъдат открити при зрелостния диабет на младите. 10
Таблица 1Б.
Клинични критерии на СЗО за метаболитен синдром 3,4
Диабет тип 2
Нарушена глюкоза на гладно
Влошен глюкозен толеранс
Или за тези с нормални нива на глюкоза на гладно (140 mmHg/систолично или> 90 mmHg диастолно)
Плазмени триглицериди> 150 mg/dl (> 1,7 mmol/l)
HDL холестерол 30 kg/m и/или талия: съотношение на тазобедрената става> 0,9 при мъжете и> 0,85 при жените.
Скорост на екскреция на албумин в урината> 20 μg/min или съотношение на албуминкреатинин> 30 mg/g.
HDL, липопротеин с висока плътност; ИТМ, индекс на телесна маса.
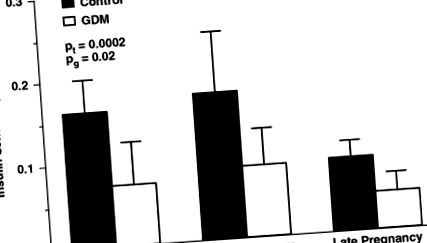
Бременността сама по себе си е състояние на намалена инсулинова чувствителност с 50% -60% намаление на инсулиновата чувствителност и дву до трикратно увеличение на инсулиновия отговор при жени с нормален глюкозен толеранс 11 (Фигури 1 и и2). 2). Следователно жените, изложени на риск от GDM, най-често имат намалена чувствителност към инсулин, включително такива като наднормено тегло или затлъстяване. Поради тяхната субклинична намалена инсулинова чувствителност и β-клетъчна дисфункция, гореспоменатият метаболитен стрес на бременността прави клинично проявление на клиничното разстройство, определено като GDM. Въпреки че първоначално схващаме диабет като нарушение на метаболизма на глюкозата, при жени с GDM има съобщения и за отклонения в метаболизма на липидите и аминокиселините, които също могат да повлияят на растежа на плода. 12 Намаляването на чувствителността към инсулин по време на бременност е свързано с майчините цитокини, особено с концентрациите на циркулиращ тумор некрозис-α (TNF-α) 13, както и с повишените концентрации на свободни мастни киселини. 14 Тъй като чувствителността към инсулин значително се подобрява веднага след раждането, 15 плацентата е замесена да играе важна роля в промените в метаболизма на майката по време на бременност при човека.
Надлъжните промени в инсулиновата чувствителност при жени с гестационен диабет (GDM) и нормален глюкозен толеранс (контрол). Pt, променя се с времето; Pg, разлики между групите. (Адаптирано от Catalano, Am J Obstet Gynecol, 1999).
Надлъжните промени в инсулиновия отговор на интравенозно глюкозно предизвикателство при жени с гестационен диабет (GDM) и нормален глюкозен толеранс (контрол). (а) първа фаза инсулинов отговор, (б) втора фаза инсулинов отговор. Pt, променя се с времето; Pg, разлика между групите. (Адаптирано от Catalano, Am J Obstet Gynecol, 1999).
Майчина
Зародиш
Детето на жените с GDM често се характеризира като голямо или макрозомично. Терминът голям за гестационна възраст (LGA) обикновено се определя като тегло, по-голямо от 90-ия процентил за гестационна възраст, пол и расова група. Макрозомията се определя по различен начин като тегло при раждане над 4000 g до 4500 g. Бебетата на жени с GDM, особено ако са родени с LGA или са макрозомични, са изложени на повишен риск от краткосрочни усложнения. По време на раждането, поради големия им размер и трудността при преминаване през родовия канал, може да възникне дистоция на рамото, от време на време последвана от парализа на Erb. 21 Веднага след раждането те са изложени на повишен риск от хипогликемия поради вътреутробната хиперинсулинемия. 22 Други заболявания при новороденото на жената с GDM включват хипокалциемия, хипербилирубинемия и дихателен дистрес. 23.
При оценката на телесния състав на кърмачета при жени с GDM тези новородени са по-тежки при раждането поради увеличаване на мастната маса, но не и поради увеличаване на чистата телесна маса 24 (фиг. 3). Отново въз основа на резултатите от проучването HAPO, повишаването на концентрациите на глюкоза при майките, по-малко от използваните в момента за определяне на GDM, също се свързва не само с увеличаване на теглото при раждане, но и с нарастване на новороденото затлъстяване. 25 Трябва да се отбележи, че при изследване на профила на генния масив на плацентата от затлъстели GDM и нормални глюкозно толерантни жени се наблюдава увеличаване на плацентарната генна експресия на ензими, свързани с липидния метаболизъм, което предполага потенциала на липидите като хранителни източници на повишено новородено затлъстяване. 26 Тези промени в новородения растеж/затлъстяване могат да бъдат един от основните фактори, водещи до дългосрочните усложнения, наблюдавани при деца на жени с GDM.
Тегло при раждане, чиста телесна маса и мастна маса на доносени новородени жени с гестационен диабет (GDM) n = 195 и нормални глюкозоустойчиви жени (NGT), n = 220. Тегло P = 0,26, чиста телесна маса P = 0,74 и мазнини маса P = 0,0002. (Адаптирано от Catalano, Am J Obstet Gynecol, 2003).
Дете
Децата на жени с GDM са изложени на повишен риск от дългосрочно затлъстяване и непоносимост към глюкоза. Въз основа на ранни проучвания на Pettitt et al. децата на Pima жени с диабет по време на бременност са имали значително увеличение както на диабет, така и на затлъстяване. 27 Този риск се запазва, когато потомството на жените с диабет в сравнение с техните братя и сестри, родени преди майката, развива непоносимост към глюкоза. 28
По-късно тези проучвания са потвърдени и разширени от Dabelea et al. също в индийско население от Пима. 29 Всъщност най-силният рисков фактор за диабет при индийските деца от Pima е майчиният диабет в утробата, независимо от затлъстяването на майката и теглото при раждане. 30–32 При предимно кавказка популация, Boney et al. съобщава, че не само големите деца за гестационна възраст на жените с GDM са имали повишен риск от диабет и затлъстяване, но че 50% от тези деца са имали доказателства за метаболитен синдром. 33 В скорошно мултиетническо проучване Hiller et al. съобщава, че с увеличаване на нивата на хипергликемия, особено хипергликемия на гладно по-малко от диагностиката на GDM, това е свързано с повишен риск от детско затлъстяване. 34
Съвсем наскоро Clausen et al. съобщава, че рискът от наднормено тегло се е удвоил при потомството, на възраст 18–27 години, при жени с диетично доверено GDM или диабет тип 1 в сравнение с контролна група от същата популация. Освен това, рискът от метаболитен синдром при същите тези потомци се е увеличил четири пъти в сравнение със същата популация. 35 В обобщение, бебето на жените с GDM има значително по-голям риск да стане по-тежко при раждане поради повишено затлъстяване. Тези деца също са изложени на повишен риск от детско затлъстяване, непоносимост към глюкоза и свързана с това метаболитна дисрегулация. Въпреки това, въз основа на клинични проучвания на Crowther 36 и Landon 37, лечението на жени с GDM по време на бременност може да намали някои от неблагоприятните неонатални резултати. Потенциалното подобрение в дългосрочните резултати от детството очаква по-нататъшно проучване.
Затлъстяване на майката
Патофизиология
Надлъжните промени в инсулиновата чувствителност при средностатистически жени с наднормено тегло и затлъстяване, преди зачеването (pregravid) и в началото (12–14 седмици) и късно (34–36 седмици) бременност. Промяна във времето, P = 0,0001. Жените със затлъстяване са по-малко чувствителни към инсулин от жените със средно тегло (P = 0,001) и жените с наднормено тегло (P = 0,0004). (Прието от BJOG, 2006). ИТМ показва индекса на телесна маса.
Както беше отбелязано по-рано, има подобрение в инсулиновата чувствителност веднага след раждането. 15 По същия начин, при сравняване на промените в инсулиновата чувствителност 1 година след раждането, се наблюдава значително подобрение на инсулиновата чувствителност при жени с нормално тегло, които са се върнали към теглото си преди бременността. 40 За разлика от това, при жени със затлъстяване с нормогликемия по време на бременност, които не успяват да се върнат към теглото си преди бременността, тези жени имат малка или никаква промяна в инсулиновата си чувствителност в сравнение с техните проучвания в края на бременността. Освен това, плазмените концентрации на TNF-α и експресията на генната експресия на TNF-α в скелетните мускули на тези жени остават по-високи 1 година след раждането в сравнение с контролите с нормално тегло. 41 Тези данни осигуряват правдоподобна връзка между затлъстяването, възпалението и инсулиновата резистентност както по време на бременност, така и при небременни индивиди като рискови фактори за непоносимост към глюкоза.
Майчина
Зародиш
Тегло при раждане, чиста телесна маса и мастна маса на доносените новородени средно (BMI 25) n = 76 жени. Тегло P 5 0,051, чиста телесна маса P = 0,22, мастна маса P = 0,006. (Адаптирано от Sewell, Am J Obstet Gynecol, 2006).
Детето на затлъстелите жени е не само по-тежко при раждане поради повишено затлъстяване, но има доказателства за повишена инсулинова резистентност, използвайки оценки на модела на хомеостаза за оценка на инсулиновата резистентност в сравнение с новородените със средно тегло жени. Освен това концентрациите на лептин и интерлукин-6 в пъпната връв на плодовете на затлъстелите жени са значително по-големи от кръвта на пъпната връв на плодовете на слабите жени. Имаше силна корелация между феталното затлъстяване и инсулиновата резистентност. 52 Тези данни предполагат, че затлъстяването на майката само по себе си представлява значителен риск за следващото поколение с метаболитен компромис, който вече е очевиден при раждането.
Дете
Както затлъстяването при майката преди бременността, така и прекомерното наддаване на тегло по време на бременност са свързани с повишено затлъстяване при деца. Понастоящем има сериозни доказателства, че потомството на затлъстелите жени е изложено на повишен риск от детско затлъстяване. Whittaker съобщава, че децата, родени от жени със затлъстяване, са се увеличили 2,5 пъти и са увеличили риска от затлъстяване на възраст 2–4 години въз основа на критериите на Центъра за контрол и превенция на заболяванията в сравнение с тези деца, родени от майки без наднормено тегло. 53 По същия начин, Boney et al. съобщава, че децата на затлъстели жени са имали двукратен риск не само от затлъстяване, но и от метаболитен синдром на възраст от 11 години, в сравнение с деца на жени със затлъстяване. 33 И накрая, Mingrone et al. в последващо проучване на млади възрастни, отбелязва, че потомството на затлъстелите жени е по-затлъстело и устойчиво на инсулин в сравнение с потомството на жени с нормално тегло по време на тяхното раждане. 54 Освен това, Oken et al. съобщава, че увеличеното гестационно наддаване на тегло е свързано с увеличаване на ИТМ на потомството и мерките за кожни гънки на възраст от 3 години. Жените с адекватно или прекомерно наддаване на тегло (критерии на IOM 1990) са имали четирикратно увеличаване на шанса да имат дете с наднормено тегло (ИТМ> 95 процентила), използвайки 2000 CDC референтни данни. 55
Въз основа на нашите собствени дългосрочни последващи проучвания при деца на жени с нормален глюкозен толеранс и GDM по време на бременност, майчиното затлъстяване е важен рисков фактор за детско затлъстяване и метаболитна дисрегулация. Няма значителна разлика в Центъра за контрол и превенция на процентите на теглото или телесния състав между децата на жените с нормален глюкозен толеранс по време на бременност и GDM на деветгодишна възраст. Най-силният перинатален предиктор за дете, намиращо се в горната част на затлъстяването, базиран на метода на рентгенова абсорбтометрия с двойна енергия, е съотношението на шансовете на ИТМ на майката (OR) 5.45 (95% CI1.62–18.4, P = 0.006). Тази връзка се подобрява след коригиране на пола (OR 6.36; 95% CI 1.77–22.88, P = 0.004) и/или пол и ако майката има GDM (OR7.75; 95% CI 1.51–37.74, P = 0.01). Силата на тези взаимоотношения не се променя, когато в анализа са включени измервания за затлъстяване при новородени. Прегравираното затлъстяване при майките, независимо от състоянието на глюкозата при майката, е най-силният предиктор за детското затлъстяване. 56
Въпреки че прегледът е фокусиран изключително върху човешкия модел, има множество проучвания върху животни, обясняващи механизмите, свързани с наблюдаваните физиологични промени. Van Assche et al. изследва метаболитните ефекти върху диетата на кафенето на майката, използвайки модел на плъх. Индуцираното от диетата затлъстяване води до увеличаване на инсулиновата резистентност при небременните кафетерии, хранени с плъхове, което се влошава от бременността. Ефектът на затлъстяването е по-голям от ефекта на бременността върху инсулиновата резистентност при този модел. Използвайки подобен миши модел, Samuelsson et al. съобщава, че индуцираното от диетата затлъстяване при женски мишки води до затлъстяване на потомството, свързано с хипертрофия на адипоцитите и променена експресия на иРНК на β-адренорецептори 2 и 3, 11 BHSD-1 и PPAR-δ2. Тези промени в метаболизма на адипоцитите могат много добре да играят роля за затлъстяването на потомството. Дългосрочните ефекти, включително нарушена регулация на сърдечно-съдовата и метаболитната функция. 58 И накрая, Plagemann съобщава, че в зависимост от критичните периоди на развитие, хормоните като инсулин и лептин могат да действат като „ендогенни функционални тератогени“. Например хиперинсулинемията може да повлияе на неправилно програмиране на невроендокринните системи, регулирайки апетита, телесното тегло и енергийните разходи. 59
Обобщение
GDM при майката и затлъстяването споделят множество метаболитни аномалии и може добре да представляват спектър от метаболитна дисрегулация на майката. За майчиното затлъстяване и GDM увеличава риска от „метаболитен синдром на бременността“, което е повишен риск от хипертонични, липидни и коагулационни нарушения, което увеличава перинаталната заболеваемост и смъртност. Потомците на тези жени също са изложени на повишен риск както за неонатална заболеваемост, така и за дългосрочни последици, свързани с анормална вътреутробна метаболитна среда. В идеалния случай промяната в начина на живот на диетата и активността за постигане на нормално тегло преди зачеването е идеалната цел за намаляване на риска от тези проблеми. 38 Въпреки това, постигането на препоръчително наддаване на тегло по време на бременност и избягването на прекомерно наддаване на тегло при бременност, както наскоро беше отбелязано в ревизираните насоки на МОМ, може да намали перинаталната заболеваемост, като задържане на теглото на майката и следователно намаленото тегло преди бременността е последваща бременност. 38 Перинаталният период предлага възможност за подобряване на краткосрочното и дългосрочното здраве на жената и нейното потомство. Ако целта е да се предотврати, а не да се лекува хронично метаболитно заболяване, тогава оптималната грижа за жените преди и по време на бременността е необходим компонент на здравето и благосъстоянието.
Таблица 1С.
AACE Клинични критерии за диагностика на синдрома на инсулинова резистентност 5
- Влиянието на майчиното затлъстяване и гестационното наддаване на тегло върху липидите в началото и средата на бременността
- Въздействието на предзачатъчното затлъстяване върху траекториите на майчините липиди по време на бременността
- Гестационната диета за диабет, приемаща въглехидрати от изкуството на бременна дама; Списание Smithsonian Culture
- Актуализиран списък на списанията за затлъстяване с висок вестник
- Влиянието на юношеското затлъстяване върху височината на възрастните - Резюме - Хормонални изследвания в педиатрията 2017