Субекти
Резюме
Въведение
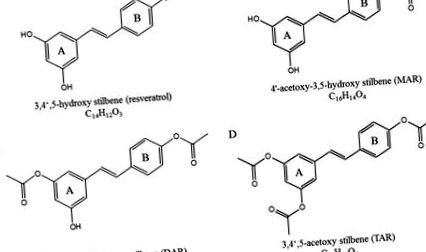
Химични структури на ресвератрол (A), моно-ацетокси ресвератрол (Б.), ди-ацетокси ресвератрол (° С) и три-ацетокси ресвератрол (д).
Резултати
Метаболизъм на тестостерон в клетъчната линия Caco-2/TC7
Окисляването на тестостерон от CYP3A4 е последвано от измерване на остатъчния тестостерон в реакционната среда по време на инкубация с клетки Caco-2/TC7 (фиг. 2). При експерименталните условия се наблюдава линейна скорост на реакция през първите 6 часа от инкубацията. Тестостеронът е количествено определен с помощта на HPLC анализ и калибрационна крива.
Метаболизъм на тестостерон в клетъчната линия Caco-2/TC7.
Данните са средно ± S.E. от три повторения.
Инхибиране на CYP3A4-медиирания метаболизъм на тестостерон в клетъчната линия Caco-2/TC7 от ацетокси стилбени
Ефектите на MAR, DAR и TAR върху жизнеспособността на клетки Caco-2/TC7 бяха измерени, както е описано. Нито едно от съединенията не причинява намаляване на жизнеспособността на Caco-2/TC7, когато се прилага до ниво от 100 μM, с изключение на 100 μM TAR, което причинява незначително намаляване на клетъчната пролиферация (Фиг. 3). Концентрацията от 100 μM е избрана като най-високата концентрация, която да бъде включена в по-късните експерименти, като се има предвид лекото намаляване на жизнеспособността на клетките, причинено от 100 μM TAR.
Клетъчна жизнеспособност на Caco-2/TC7, когато в средата присъстват различни концентрации на моно/ди/три-ацетокси ресвератрол.
Метаболизмът на тестостерон от клетки Caco-2/TC7 в културата се използва за изследване на взаимодействието на ацетокси стилбени с CYP3A4. Всички изследвани ацетокси стилбени инхибират метаболизма на тестостерона по зависим от дозата начин, значително различен от контрола и максимално инхибиране е постигнато чрез прилагане на 50 μM (Фиг. 4). Въпреки това, TAR има най-слабата способност за инхибиране от всички тествани съединения. Изразяването на резултатите от прилагането на 10 μM от всяко съединение като процент от контролата разкрива подобна тенденция, при която редът на способността за инхибиране е DAR> MAR> TAR, с изчислени проценти от 45%, 24% и 10%, съответно (фиг. 5). Ресвератролът проявява по-силен инхибиторен капацитет от всички ацетокси стилбени, като 10 μM ресвератрол намалява ензимното окисление на тестостерона с повече от 80% след 2 часа инкубация. Това инхибиране е подобно на това, наблюдавано за кетоконазол, добре познат специфичен инхибитор на CYP 3A (фиг. 5). След 2 часа инкубация, скоростта на инхибиране беше намалена при всички лечения, но все пак беше значително по-ниска от контролата, измерена при всяко инкубационно време.
Инхибиране на метаболизма на тестостерон в клетки Caco2/TC7 чрез различни концентрации на моно-ацетокси стилбен (A), ди-ацетокси стилбен (Б.) и три-ацетокси стилбен през време на инкубация в сравнение с контрола. Данните са средни ± S.E. от три повторения.
Инхибиране на метаболизма на тестостерон в клетки Caco2/TC7 от ацетокси аналозите, ресвератрол и кетоконазол, при концентрация 10 μM, в сравнение с контролите във времето.
Инхибиране на активността на микрозома-CYP3A от ацетокси стилбени
Показано е, че всички тествани стилбени инхибират микрозомалната активност на CYP3A, измерена като намаляване на отделянето на тритирана вода чрез хидроксилиране на тестостерон [1,2,6,7-3 Н (N)] (Фиг. 6). Скоростите на инхибиране, изразени като процент спрямо контролата, показват, че най-силно инхибиране се наблюдава след прилагането на кетоконазол, който има стойност на IC50 от 14 μM. В тази система, IC50 на ресвератрола, както се изчислява от кривите концентрация-отговор, беше установено, че е 28 μM. Стойностите на IC50 за MAR, DAR и TAR в тази система не могат да бъдат изчислени поради ниските нива на инхибиране, индуцирани от тези вещества. В съгласие с резултатите, получени за ТС7 клетки, TAR показва най-ниския капацитет на инхибиране и прилагането на 10 μM TAR води до същата степен на инхибиране като 100 μM. DAR и MAR демонстрират сходни потенции, когато се прилагат в концентрация от 100 μM, техните потенции (съответно 44% и 48% инхибиране) са подобни на тези на ресвератрола (фиг. 6).
Инхибиране на CYP3A-медиирано образуване на тритирана вода.
Изчислителен анализ
Ориентацията и остатъчната връзка на кетоконазол, изведени от рентгеновата структура на човешкия CYP3A4 (PDB код 2V0M), служи като модел за изчисляване на взаимодействията на ресвератрол и молекулите, синтезирани тук. За да потвърдим пригодността на избрания модел на докинг, първо закачихме кетоконазол и се уверихме, че свързването му със свързващото място на CYP3A4 е възстановено до първоначалното състояние, както в оригиналната структура 2V0M. Според симулацията за докинг на кетоконазол, мястото на свързване може да бъде описано по отношение на три основни характеристики: твърда хидрофобна област, донори/акцептори на Н-връзки и електростатични взаимодействия. Хидрофобният клъстер включва алкил и алкил-пи взаимодействия между остатъци CYP3A4 Leu210, Phe241, Ile301, Ala305 и Leu482 и хлориран ароматен пръстен и имидазолов пръстен на кетоконазоловата молекула. Основният остатък на донор на Н-връзка е CYP3A4 Arg372, който взаимодейства с кетонния кислороден атом на кетоконазол; като има предвид, че кислородните атоми на Ala370 служат като акцептори на Н-връзка. Азотният атом от групата на хема осигурява допълнително закрепване към молекулата чрез нейните електростатични взаимодействия (анион-пи) с имидазоловия пръстен на кетоконазола (Фигури 7А и 8А, В).
Резултати от докинг на лигандите на мястото на свързване на CYP3A4, показващи взаимодействащите остатъци: кетоконазол (A, Енергия на CDOCKER = -40,752 kcal/мол; Енергия на взаимодействие на CDOCKER = -60,612 kcal/мол) и ресвератрол (Б., Енергия на CDOCKER = -25,504 kcal/мол; Енергия на взаимодействие на CDOCKER = -33.960 ккал/мол). Лигандите са показани като сиви пръчки, а остатъците от рецептори са зелени пръчки. Връзките са показани като пунктирани линии, цветно кодирани, както следва: хидрофобни взаимодействия в магента, електростатично взаимодействие в кафяво и водородни връзки в зелено.
Карти на хидрофобността (A, C) и водородни връзки (B, D) на мястото на свързване на CYP3A4, докирано с различните лиганди: кетоконазол (А, Б); ресвератрол (C, D). Лигандите са показани като сиви пръчки, а остатъците от рецептори са зелени пръчки.
Резултати от докинг на лигандите на мястото на свързване на CYP3A4, показващи взаимодействащите остатъци: MAR (A, Енергия на CDOCKER = -21,741 kcal/мол; Енергия на взаимодействие на CDOCKER = -29,358 kcal/мол), DAR (Б., Енергия на CDOCKER = -25,733 kcal/мол; Енергия на взаимодействие на CDOCKER = −34,376 kcal/мол) и TAR (° С, Енергия на CDOCKER = -29,487 kcal/мол; Енергия на взаимодействие на CDOCKER = −36.707 kcal/мол). Лигандите са показани като сиви пръчки, а остатъците от рецептори са зелени пръчки. Връзките са показани като пунктирани линии, цветно кодирани, както следва: хидрофобни взаимодействия в магента, електростатично взаимодействие в кафяво и водородни връзки в зелено.
Карти на хидрофобността (A, C, E) и водородни връзки (B, D, F) на мястото на свързване на CYP3A4, докирано с различните лиганди: MAR (А, Б), DAR (C, D) и TAR (E, F). Лигандите са показани като сиви пръчки, а остатъците от рецептори са зелени пръчки.
Дискусия
В последните проучвания се натрупват доказателства, които показват, че съществуват мощни взаимодействия от клинично значение между CYP3A4 и диетичните полифеноли, включително флавоноиди, фенолни киселини, фенолни алкохоли, стилбеноиди и лигнани 4. Инхибиторните ефекти на т-ресвератрол на CYP3A4, и двете инвитро и in vivo, са добре документирани в литературата 15,16,17,18,19,37 и клиничните изпитвания са установили, че прилагането на ресвератрол увеличава плазмените концентрации на няколко лекарства 20,27. Няколко проучвания за QSAR и фармакофорно картографиране сочат значението на липофилността, а също и ролята на Н-връзките при определяне на това как различните молекули взаимодействат с CYP3A4 28,29,31,33 .
Предишно проучване описва ефекта на липофилността на молекулата върху нейните взаимодействия с CYP3A4, използвайки синтетични модификации на ресвератрол. Това проучване установи, че метокси-стилбените имат по-ниски стойности на IC50 и по-голям афинитет към CYP3A4 в сравнение с родителския ресвератрол и неговите глюкозиди 17. Неотдавнашната ни работа разкри, че въвеждането на алдехидна група в А пръстена на ресвератрол намалява способността му да инхибира CYP3A4, както е показано при използване инвитро и в силико модели. Това откритие подчертава значението на електростатичните взаимодействия на молекулата в активното място на ензима, в допълнение към хидрофобните и Н-връзките 37. За разлика от хидроксилната група, ацетокси групата е голяма и е силен акцептор на Н-връзка 39. По този начин, постепенното заместване на хидроксилните групи с ацетокси групи може не само да увеличи липофилността на молекулата, но и да въведе акцептори на Н-връзка в молекулата. Тук ацетоксилираните стилбени служат за диференциране на липофилността от връзката структура-активност при инхибиране на CYP3A4, като се използват два различни биологични модела и симулационен софтуер.
CYP3A4-медиираният метаболизъм на тестостерон, използвайки клетки Caco-2/TC7, е проектиран да продължи 8 часа, за да представи оптимално преминаването през червата. Линейна крива се наблюдава в продължение на 2 до 6 часа инкубационен период, което води до избора на този интервал от време за изследване на инхибирането на човешкия чревен CYP3A4. Наблюдавахме консумацията на субстрат и в този контекст обработките се различаваха значително от контролните през всички изследвани инкубационни периоди. Ресвератролът инхибира CYP3A4 по начин, подобен на този на кетоконазол, с изчислени стойности на IC50 в съответствие с тези, представени в предишни разработки 16,40,41,42,43. Повишаването на липофилността за постигане на по-високо инхибиране се оказва правилно за трансформацията на MAR в DAR, но не и за ресвератрол в MAR, или за допълнителното ацетилиране, за да се получи TAR. Всъщност не можахме да изчислим стойностите на IC50 за ацетокси стилбените, тъй като не можахме да постигнем достатъчно инхибиране в TC7 клетките или в RLM анализа. Горните резултати ясно показват значението на структурните свойства при определяне на способността за инхибиране на тясно свързани полифеноли срещу CYP3A4.
В скорошно проучване изследването на докинг на кетоконазол, ресвератрол и ресвератрол-алдехид на мястото на свързване демонстрира ролята, която играят хидрофобните и електростатичните взаимодействия при взаимодействията на полифеноли с CYP3A 37. По подобен начин изчислителните инструменти служат за описване на взаимодействията на оцветители за храна с човешки серумен албумин 44. Тук, използвайки докинг симулация, ние показахме, че кетоконазолът участва в силни хидрофобни взаимодействия на активното място, в допълнение към неговото електростатично взаимодействие с хема и няколко Н-връзки (Фигури 7А и 8А, В). Значението на липофилността на CYP3A4-лиганда и способността му да установява хидрофобни взаимодействия са добре документирани 4,17,31. Ресвератролът има по-малко хидрофобни взаимодействия от кетоконазола, което може да обясни по-високата му CDOCKER енергия. Ресвератролът обаче има силни хидрофобни и електростатични взаимодействия с хем групата и нейните атоми желязо/азот и Н-връзки с повече остатъци от кетоконазола на активното място (Фигури 7B и 8C, D). Ролята на хем-желязото в метаболитния начин на действие на ензимите CYP е добре установена 45,46,47,48, както и приносът на електростатичните взаимодействия с групата на хема към афинитета на лиганда към CYP3A4 37 .
В заключение, тази работа за първи път демонстрира, че индуцирана от субстрат модификация на активното място на CYP3A4 може да бъде предсказана с помощта на симулационни модели. Тези прогнози са в съгласие с резултатите, постигнати при използване на кристалография за обилно лекарство, напр. еритромицин и неговите взаимодействия с CYP3A4 49. Всъщност ниският инхибиционен капацитет на TAR както в човешката клетъчна линия, така и в микрозомите на черния дроб на плъх може да се обясни с тези резултати от симулацията. Следователно, такива резултати могат да предоставят уникална илюстрация на важността на близостта на лиганда до активното място на ензима. Като цяло, използването на софтуерно базирани прогнози, заедно с изчерпателни познания за начина на действие на ензима и биологичните анализи, позволяват по-задълбочено разбиране на сложните взаимодействия ензим-субстрат.
Методи
Стандарти и химикали
т-Ресвератрол (транс-3,4 ′, 5-трихидроксистилбен, 99%), тестостерон (99%) и кетоконазол (98%) са закупени от Sigma Aldrich, Израел. Тестостеронът [1,2,6,7-3 Н (N)] е закупен от (Perkin Elmer, САЩ). Всички други химикали и реактиви са закупени от Sigma Aldrich, освен ако не е посочено друго.
Ацетилиране на ресвератрол
Синтезът на ацетоксилирани аналози на ресвератрол се извършва с помощта на реакции на ацетилиране, както е описано от 50. Разтвор на ресвератрол (0,6 g, 2,63 mmol), ацетил хлорид (0,56 ml, 7,88 mmol) и триетеламин (1,009 ml, 7,88 mmol) се разбърква в 50-милилитрова колба с кръгло дъно с ацетон (20 ml) като разтворител. След като разтворът се разбърква в продължение на една нощ, той се подкислява (1Н NMR и 13C NMR спектри на продуктите се получават с 200-MHz ЯМР спектрометър Bruker (Bruker Biospin GmbH, Rheinstetten, Германия).
ЯМР анализ
Моно-ацетокси ресвератрол (MAR)
(4′-ацетокси-3,5-хидрокси-стилбен): 1 Н ЯМР (200 MHz, MeOD, ppm): δ 2,26 (s, ЗН), 6,21 (t, J = 2,2 Hz, 1H), 6,49 (d, J = 2,2 Hz, 2H), 6,99–7,08 (m, 4H), 7,49–7,54 (m, 2H). 13 C NMR (200 MHz, MeOD, ppm): δ 20,9 (CH3), 103,2, 106,1, 116,5, 122,9, 128,3, 130,2 (CH), 135,1, 136,6, 148,0, 151,6, 159,7, 171,2, 178,2 (C).
Ди-ацетокси ресвератрол (DAR)
(3,4′-ацетокси-5-хидрокси-стилбен): 1 Н ЯМР (200 MHz, MeOD, ppm): δ 2.27 (s, 6H), 6.45 (t, J = 2.2 Hz 1H), 6.78 (q, J = 1.8 Hz, 1H), 6.86 (t, J = 1.8 Hz, 1H ), 7.04–7.15 (m, 4H), 7.51–7.57 (m, 2H). 13 C NMR (200 MHz, MeOD, ppm): δ 20,9 (CH3), 109,3, 111,8, 111,9, 124,8, 127,6, 129,2, 129,5 (CH), 136,9, 140,8, 151,7, 153,4, 157,1, 159,6, 171,1 (C).
Три-ацетокси ресвератрол (TAR)
(3,4 ′, 5-ацетоксистилбен): 1 Н ЯМР (200 MHz, MeOD, ppm): δ 2,30 (s, 9H), 6,83 (t, J = 2 Hz, 1H), 7,07–7,26 (m, 6H), 7,56–7,61 (m, 2H). 13 C NMR (200 MHz, MeOD, ppm): δ 20,9 (CH3), 115,7, 118,1, 120,4, 123,1, 128,1, 128,7 (CH), 130,7, 137,7, 151,9, 152,9, 170,7, 171,1, 174,8 (C).
Поддръжка на клетките Caco-2/TC7
Caco-2/TC7, подклон на Caco-2, изразява високо ниво на ензим CYP3A4, което е доста често в човешкото черво 51,52,53. Клетъчната линия TC7 обикновено се използва за изследване на CYP3A4-медииран метаболизъм 54,55,56. Клетките Caco-2/TC7, използвани в това проучване, са подарък от д-р М. Русе (INSERM U505, Париж) 52. По време на експеримента тези клетки се поддържат при асептични условия в модифицираната среда на Dulbecco Eagle (DMEM) при 37 ° С с 5% CO2 и 95% въздух. DMEM беше допълнен с 20% фетален говежди серум, 100 единици/ml пеницилин (Biological Industries, Израел), 100 μg/ml стрептомицин (Biological Industries), 1% разтвор на несъществени аминокиселини (концентриран 100X, Biological Industries) и 1 % Разтвор на L-глутамин (200 mM, Biological Industries). Средата беше предварително затоплена до 37 ° С преди контакт с клетките. Клетките Caco-2/TC7 се използват между пасажи 25 и 35 и се отглеждат в 75-сантиметрови колби. Посяват се нови колби при концентрация 3–4 × 104 клетки/cm2 .
Метаболизъм на тестостерон в клетки Caco-2/TC7
HPLC анализ
Анализът на течна хроматография под високо налягане (HPLC) беше извършен върху Surveyor HPLC система (Thermo Finnigan, САЩ), използвайки RP-C18 Luna колона 250 mm × 4.6 mm × 5 μm (Phenomenex, САЩ). Елуирането се извършва с вода (разтворител А) и ацетонитрил (разтворител В) при скорост на потока 0,7 ml/min. Градиентът на подвижната фаза беше модифициран, както следва: B в A (v/v), от 5-25% за 5 минути, от 25-75% за 10 минути, от 75-95% за 5 минути, последвано от задържане за 2 мин., падна отново до 5% за 1 мин. и се задържа 4 мин. Пробите бяха изследвани с детектор с фотодиодна решетка при 244 nm за тестостерон и неговия метаболит и при 280 nm и 306 nm за ресвератрол и неговите производни. Пиковете са сканирани между 196 и 450 nm.
Анализ на жизнеспособността на клетките
Ефектите на аналозите на ацетокси стилбен върху пролиферацията на клетки Caco-2/TC7 бяха оценени чрез MTT анализа. Клетките се засяват върху 96-ямкови плаки с плътност 10 4 клетки на гнездо и се инкубират в продължение на 24 часа. След това клетките бяха третирани с DMEM (контрола) и аналозите на ацетокси стилбен MAR, DAR и TAR при различни концентрации (5, 10, 25, 50, 100 μM) за допълнителни 8 часа. Клетките се инкубират с 3- (4,5-диметилтиазол-2-ил) -2,5-дифенил тетразолиев бромид (МТТ, 0,5 mg/ml) в продължение на 1 час и последващо инкубиране с DMSO в продължение на 20 минути. Образуването на оцветеното багрило формазан се оценява колориметрично при 550 nm в четец за микроплаки ELX 808 Ultra (BIO-TEK Instruments, Лондон, Великобритания), използвайки софтуера KCJunior (Йорк, Великобритания).
Приготвяне на микрозоми на черния дроб на плъх
Метаболизъм на тестостерон чрез микрозомен CYP3A
Софтуер за изчислително моделиране и симулация
Допълнителна информация
Как да цитирам тази статия: Basheer, L. и др. Инхибиране на цитохром P450 3A от ацетоксилирани аналози на ресвератрол в инвитро и в силико модели. Sci. Представител. 6, 31557; doi: 10.1038/srep31557 (2016).
- Инхибирането на транспортера на урея подобрява уремичната кардиомиопатия при хронично бъбречно заболяване - Kuma
- Съдържание на лутеин и in vitro антиоксидантна активност на различни сортове цвете от индийски невен
- Как да се подготвим за ин витро оплождане 13 стъпки
- Месни аналози „Голяма възможност“ за подобрено качество
- Проучването in vitro показва положителни ефекти на кетогенната диета върху митохондриалната функция при синдром на Leigh