Одра Кларк
Югозападен медицински център на Тексаския университет, бул. Хари Хайнс 5323, Далас, Тексас 75390 САЩ
Джонатан Имран
Югозападен медицински център на Тексаския университет, бул. Хари Хайнс 5323, Далас, Тексас 75390 САЩ
Тарик Мадни
Югозападен медицински център на Тексаския университет, бул. Хари Хайнс 5323, Далас, Тексас 75390 САЩ
Стивън Е. Улф
Югозападен медицински център на Тексаския университет, бул. Хари Хайнс 5323, Далас, Тексас 75390 САЩ
Свързани данни
Резюме
Тежкото изгаряне причинява значителни метаболитни нарушения, които правят хранителната подкрепа уникално важна и предизвикателна за изгарящите пациенти. Травмата от изгаряне причинява трайно и продължително хиперметаболитно състояние и повишен катаболизъм, което води до увеличаване на загубата на мускули и кахексия. Скоростта на метаболизма на пациентите с изгаряния може да надмине два пъти нормата и неспазването на тези енергийни изисквания причинява нарушено заздравяване на рани, дисфункция на органите и податливост към инфекция. Адекватната оценка и осигуряване на хранителни нужди е наложително за грижата за тези пациенти. Няма консенсус относно оптималното време, път, количество и състав на хранителната подкрепа за пациенти с изгаряния, но повечето клиницисти се застъпват за ранно ентерално хранене с високо въглехидратни формули.
Хранителната подкрепа трябва да бъде индивидуализирана, наблюдавана и коригирана по време на възстановяването. Необходими са допълнителни проучвания относно оптималната хранителна подкрепа и точните хранителни крайни точки и цели.
Заден план
Хранителната подкрепа е критичен аспект на лечението на пациенти с изгаряния. Скоростта на метаболизма на тези пациенти може да бъде по-голяма от два пъти нормалната скорост и този отговор може да продължи повече от една година след нараняването [1, 2]. Тежкият катаболизъм придружава хиперметаболитното състояние и води до огромна загуба на чиста телесна маса, както и до спад на имунната функция на гостоприемника [3]. Значителната хранителна подкрепа за посрещане на увеличените енергийни разходи е жизненоважна за оцеляването на пациентите с изгаряне. За съжаление знанията ни относно сложната физиология на храненето са непълни и хранителните режими варират значително в отделните центрове. Все още съществуват много въпроси относно оптималния път, обем и състав на диетата при изгарянето. Тази статия ще направи преглед на текущото състояние на хранене след нараняване.
Преглед
Хиперметаболитното състояние
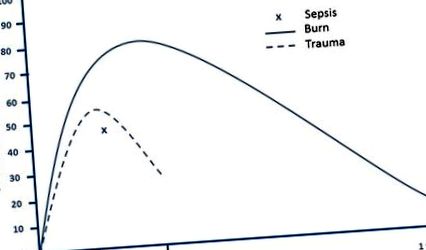
Тежките изгаряния причиняват дълбока патофизиологична реакция на стрес и радикално повишена скорост на метаболизма, която може да продължи години след нараняване. Травмата и сепсисът също водят до хиперметаболизъм, макар и в много по-малка степен и за значително по-кратка продължителност (фиг. 1). Веднага след тежко нараняване, пациентите имат период на намален метаболизъм и намалена тъканна перфузия, известен като фаза „отлив“. Скоро след това те навлизат във фазата на хиперметаболитни скорости и хипердинамична циркулация, наричана „състояние на потока“ [4]. Това хиперметаболитно състояние отразява увеличаване на потреблението на кислород в цялото тяло и пациентът обикновено се счита за хиперметаболитен, когато енергийният разход (REE) е над 10% над нормалния [5]. Във фазата на острото нараняване след изгаряне, пациентите с изгаряне, което обхваща повече от 40% от общата телесна повърхност (TBSA), имат REE между 40 и 100% над нормалното [6, 7]. Важно е да се смекчи тази реакция на стрес и да се подкрепят значително увеличените метаболитни нужди на пациента, тъй като непровереният хиперметаболизъм води до огромна загуба на чиста мускулна маса, имунен компромис и забавено зарастване на рани.
Хиперметаболитен отговор след тежко изгаряне, травма и сепсис. Адаптирано от препратки [5, 6, 123, 124]
Хиперметаболизмът след изгаряне е много сложен и все още не е напълно изяснен. Основните механизми на тази огромна метаболитна, хормонална и възпалителна дисрегулация все още се изследват активно. На клетъчно ниво, увеличената консумация на кислород в цялото тяло поддържа по-голям обмен на аденозин трифосфат (АТФ) и термогенеза. Реакциите, консумиращи АТФ, представляват приблизително 57% от хиперметаболитния отговор на изгаряния, включително АТФ оборот за синтез на протеини, производство на АТФ за чернодробна глюконеогенеза и циклиране на глюкоза и мастни киселини [8]. Тъй като оборотът на АТФ не отчита напълно хиперметаболизма, предизвикан от изгаряне, това предполага, че консумацията на митохондриален кислород надвишава производството на АТФ след тежко изгаряне. Това вероятно се случва чрез разединяване на митохондриалното дишане от ADP фосфорилирането, което води до производство на топлина [5]. Тази теория се подкрепя от неотдавнашната констатация, че отделящият протеин 1 (UCP1), митохондриален трансмембранен протеин и основен медиатор на термогенезата, е много по-обилен в мастната тъкан на пациенти с изгаряне в сравнение със здрави индивиди [9, 10].
Няколко проучвания включват катехоламините като основен медиатор на хиперметаболизма [11, 12]. Повишаването на катаболните хормони епинефрин, кортизол и глюкагон водят до инхибиране на протеиновия синтез и липогенезата [13]. Разграждането на протеините се превръща в необходим и голям източник на енергия, а кахексията на скелетните мускули е резултат от дълготраен дисбаланс между синтеза на протеини и разграждането. Дисрегулацията на кинетиката на скелетните мускули продължава една година или повече след тежко изгаряне и се съобщава за намалена чиста телесна маса при пациенти до 3 години след нараняване [14–16].
Изследвани са много други терапии за подобряване на индуцирания от изгаряне хиперметаболизъм. Управлението на околната среда с затоплянето на стаите на пациентите и оклузивните превръзки за рани отслабват хиперметаболитния отговор, тъй като пациентите с изгаряне са загубили кожната си бариера и следователно трябва да произвеждат повече топлина, за да поддържат топлинна неутралност. Ранното изрязване на рани и присаждането доведоха до подобрения в смъртността, намалена ексудативна загуба на протеин, по-нисък риск от инфекция на рани от изгаряне и намален мускулен катаболизъм [19, 23]. Това може да се дължи на намаляване на нивата на циркулиращи възпалителни цитокини като интерлевкин (IL) -6, IL-8, C3 комплемент и фактор на туморна некроза (TNF) -α [24].
Няколко доказани фармакологични метода могат да бъдат използвани за намаляване на хиперметаболитния отговор на изгаряне. Бета-адренергичната рецепторна блокада, обикновено с пропранолол, намалява сърдечната честота и метаболизма при пациенти с тежки изгаряния [25–27]. Наскоро беше показано, че лечението с пропранолол за 1-годишно изгаряне подобрява периферното натрупване на чиста телесна маса [28]. Доказано е, че оксандролонът, синтетичен андроген, притъпява хиперметаболизма, подобрява минералното съдържание и плътност на костите и увеличава нарастването на чистата телесна маса при деца с тежко изгаряне [29–32]. Установено е, че рекомбинантен човешки растежен хормон (rHGH) намалява хиперметаболизма и подобрява нарастването на чистата телесна маса след изгаряне, но употребата му е ограничена поради две многоцентрови проучвания, показващи, че терапията с растежен хормон увеличава смъртността при критично болни възрастни [33–35]. Необходими са повече изследвания относно ефикасността и безопасността на употребата на rHGH при пациенти с изгаряне.
График на хранителната подкрепа
Калорийни изисквания
Основната цел на хранителната подкрепа при пациенти с изгаряне е да изпълни повишените калорични изисквания, причинени от хиперметаболичното състояние, като същевременно избягва прекомерното хранене. През годините са разработени и използвани множество формули за оценка на калоричните нужди на жертвите на изгаряне [42]. Един от най-ранните примери е формулата на Curreri [43]. Той е предложен през 1972 г. и е създаден чрез проучване на 9 пациенти и пресмятане на обратното, за да се сближат калориите, които биха били необходими за компенсиране на загубата на тегло на пациентите. Формулата на Curreri и много други по-стари формули надценяват настоящите метаболитни изисквания и са предложени по-сложни формули с различни променливи (Таблица 1) [44]. Едно проучване на 46 различни формули за прогнозиране на калорични нужди при пациенти с изгаряне установи, че никой от тях не корелира добре с измерения енергиен разход при 24 пациенти [1]. Разходът на енергия се променя след изгаряне и фиксираните формули често водят до недохранване по време на периоди на най-високо използване на енергия и до прехранване в края на курса на лечение.
маса 1
Общи формули, използвани за изчисляване на калорийните нужди на пациентите с изгаряне
| Формули за възрастни | Kcal/ден | Коментари |
| Харис Бенедикт | Мъже: 66,5 + 13,8 (тегло в кг) + 5 (височина в см) - 6,76 (възраст в години) Жени: 655 + 9,6 (тегло в кг) + 1,85 (височина в см) - 4,68 (възраст в години) | Оценява базалните енергийни разходи; може да се регулира както по активност, така и по фактор на стрес, умножен по 1,5 за обща корекция на стреса при изгаряне |
| Формула на Торонто | −4343 + 10,5 (TBSA) + 0,23 (прием на калории през последните 24 часа) + 0,84 (оценка на Харис Бенедикт без корекция) + 114 (температура) - 4,5 (брой дни след изгаряне) | Полезен при остър стадий на изгаряне; трябва да се коригира с промени в параметрите за мониторинг |
| Дейвис и Лилиедал | 20 (тегло в кг) + 70 (TBSA) | Надценява калоричните нужди при големи наранявания |
| Иретън-Джоунс | Вентилиран пациент: 1784 - 11 (възраст в години) + 5 (тегло в кг) + (244, ако е мъж) + (239, ако е травма) + (804, ако е изгорено) Невентилиран пациент: 629 - 11 (възраст в години) + 25 (тегло в кг) - (609 при затлъстяване) | Сложна формула, която интегрира променливи за състоянието на вентилация и нараняване |
| Curreri | Възраст 16–59: 25 (тегло в кг) + 40 (TBSA) Възраст> 60: 20 (тегло в кг) + 65 (TBSA) | Често надценява калоричните нужди |
| Педиатрични формули | ||
| Галвестън | 0–1 година: 2100 (телесна повърхност) + 1000 (телесна повърхност × TBSA) 1–11 година: 1800 (телесна повърхност) + 1300 (телесна повърхност × TBSA) 12–18 години: 1500 (телесна повърхност) + 1500 (телесна повърхност × TBSA) | Фокусира се върху поддържането на телесното тегло |
| Курери младши | 1.0. Това обяснява едно опасно усложнение на прехранването: трудно отбиване от вентилационната опора [46]. Въпреки тази загриженост, едно проучване установи, че диетите с високо съдържание на въглехидрати в група пациенти с детско изгаряне водят до намаляване на загубата на мускулна маса и не водят до RQs над 1,05 или някакви дихателни усложнения [47]. |
Субстрати
Метаболитният процес включва създаването и разграждането на много продукти, необходими за биологичните процеси. Метаболизмът на три макронутриенти - въглехидрати, протеини и липиди - осигурява енергия по различни пътища (фиг. 2).
- Амбулаторни хранителни услуги за онкологични пациенти
- Храненето е „основен“ компонент на грижите за пациенти с рак на главата и шията
- Храненето в отборните спортове - FullText - Анали за храненето и метаболизма 2010, кн
- Храненето при пациенти с муковисцидоза европейски консенсус - ScienceDirect
- Управление на храненето за пациенти с котешка онкология - Ветеринарно здраве на Етос