Мън Ву
1 Център за геномни науки и системна биология, Медицински факултет на Вашингтонския университет, Сейнт Луис, МО 63108 САЩ
2 Център за чревни микробиоми и изследвания на храненето, Медицински факултет на Вашингтонския университет, Сейнт Луис, МО 63108 САЩ
Нейтън П. Макналти
1 Център за геномни науки и системна биология, Медицински факултет на Вашингтонския университет, Сейнт Луис, МО 63108 САЩ
Дмитрий А. Родионов
3 Център за инфекциозни и възпалителни заболявания, Институт за медицинско откритие Sanford-Burnham-Prebys, La Jolla, 92037 CA USA
4 Институт по проблеми на предаването на информация А. А. Харкевич, Руска академия на науките, Москва 127994, Русия
Матвей С. Хорошкин
4 Институт по проблеми на предаването на информация А. А. Харкевич, Руска академия на науките, Москва 127994, Русия
Николас У. Грифин
1 Център за геномни науки и системна биология, Медицински факултет на Вашингтонския университет, Сейнт Луис, МО 63108 САЩ
2 Център за чревни микробиоми и изследвания на храненето, Медицински факултет на Вашингтонския университет, Сейнт Луис, МО 63108 САЩ
Джие Ченг
1 Център за геномни науки и системна биология, Медицински факултет на Вашингтонския университет, Сейнт Луис, МО 63108 САЩ
2 Център за чревни микробиоми и изследвания на храненето, Медицински факултет на Вашингтонския университет, Сейнт Луис, МО 63108 САЩ
Фил Латрей
5 Monsanto Company, Сейнт Луис, МО 63167 САЩ
Randall A. Kerstetter
5 Monsanto Company, Сейнт Луис, МО 63167 САЩ
Никола Терапон
6 Architecture et Fonction des Macromolécules Biologiques, Centre National de la Recherche Scientifique & Aix-Marseille Université 13288 Marseille cedex 9, Франция
Бернард Хенрисат
6 Architecture et Fonction des Macromolécules Biologiques, Centre National de la Recherche Scientifique & Aix-Marseille Université 13288 Marseille cedex 9, Франция
7 Департамент по биологични науки, Университет Крал Абдулазиз, Джеда, Саудитска Арабия
Андрей Л. Остерман
3 Център за инфекциозни и възпалителни заболявания, Институт за медицинско откритие Sanford-Burnham-Prebys, La Jolla, 92037 CA USA
Джефри И. Гордън
1 Център за геномни науки и системна биология, Медицински факултет на Вашингтонския университет, Сейнт Луис, МО 63108 САЩ
Свързани данни
Резюме
Библиотеките с десетки хиляди транспозонни мутанти, генерирани от всеки от четирите щама на човешките чревни Bacteroides, два от които представляват един и същи вид, бяха въведени едновременно в мишки с гнотобиотик, заедно с 11 други щама от див тип, за да генерират 15-членна изкуствена микробиота на човешкото черво Мишките получават една от двете различни диети монотонно или и двете в подредена последователност. Количественото определяне на изобилието от мутанти в различен контекст на диетата позволи характеризиране на генно ниво на детерминантите за фитнес, ниша, стабилност и устойчивост и даде пребиотик (арабиноксилан), който позволи целенасочена манипулация на общността. Описаният подход е обобщаващ и би трябвало да бъде полезен за определяне на критични механизми за поддържане и/или подходи за умишлено преконфигуриране на силно адаптивната и трайна връзка между човешката чревна микробиота и гостоприемника по начини, които насърчават здравето.
Човешката микробиота е много разнообразна (1–3). Съвременното мнение е, че щамовете, придобити от индивида в началото на живота, продължават десетилетия и че щамовете се споделят между членовете на семейството. Микробиотата може бързо да се адаптира към променящите се условия, но степента, до която дадени групи щамове споделят или се конкурират за нишово пространство в чревната екосистема, е слабо разбрана. Идентифицирането на генетичните фактори, които определят нишата на даден организъм, е важно за разбирането на механизмите, които определят събирането на общността, реакциите на общността и възстановяването след различни смущения и хранителните мрежи, които свързват микробите един с друг и с техния гостоприемник. Откриването на тези фактори трябва да породи нови подходи за умишлено манипулиране на функционалните свойства на микробиотата.
Този подход не само ни позволи да разгледаме събранието на 15-членната изкуствена общност, но и да характеризираме реакциите на диетични смущения и възстановяване след тези смущения (стабилност и устойчивост) на ниво общност, отделни видове/щам, както и генно ниво. Ние идентифицираме общи, както и специфични за видовете и щамовете генетични и метаболитни характеристики, които влияят върху годността на Bacteroides в чревната среда.
Характеризиране на множество мутантни библиотеки на транспозон едновременно in vivo (multitaxon INSeq)
Всяка библиотека, която генерирахме от четирите бактериални щама, беше съставена от 87 000–167 000 изогенни транспозон (Tn) мутанти. Всеки мутант съдържа едно място за вмъкване на Tn елемента. 81,5–91,8% от отворените рамки за четене (ORF) в тези четири Bacteroides съдържат Tn вмъкване, което ни позволява да заключим, че нарушаването на тези гени не е попречило на растежа в богатата среда, използвана за изграждане на библиотеките (вж. Допълнителни резултати за анализ на „основни“ гени, които не са представени в различните библиотеки на мутанти, с фокус върху тези, които участват във въглехидрати, аминокиселини и биосинтез/катаболизъм на витамин/кофактор).
Сбор на общността, стабилност и устойчивост в отговор на различни диети
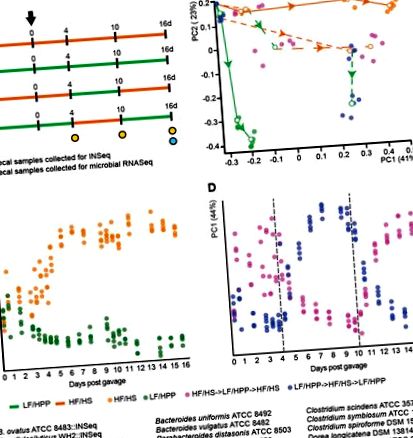
Възрастни (от 10 до 12 седмици) мъжки мишки без зародиши C57BL/6J бяха поставени или на нискомаслена/високо-растителна полизахаридна (LF/HPP) чау, или на диета, при която калориите бяха до голяма степен получени от хидрогенирано скъсяване на зеленчуци и говеждо месо лой и където въглехидратите бяха ограничени до захароза, царевично нишесте и малтодекстрин (плюс несмилаемо целулозно свързващо вещество) [диета с високо съдържание на наситени мазнини/висока проста захар (HF/HS)]. Диетите бяха въведени 7 дни преди животните да получат единичен орален манифест на изкуствената общност, съдържащ четирите мутагенизирани библиотеки от щамове и 11 щама от див тип (фиг. 1А). Контролните експерименти използват 15-членна общност, съставена от всички щамове див тип, или 15-членни общности, които съдържат само една мутантна библиотека (фиг. S4A). Групи мишки с единична клетка бяха поддържани на диета LF/HPP или HF/HS по време на експеримента, докато други групи бяха подложени на реципрочен набор от диетични трептения (LF/HPP → HF/HS → LF/HPP или HF/HS → LF/HPP → HF/HS) (n = 5 мишки/диетично лечение/тип общност/гнотобиотичен изолатор; фиг. 1А). Кратко четено секвениране на пушка (COmmunity PROfiling by Sequencing; COPRO-Seq) на ДНК, приготвена от фекални проби, събрани по време на всеки експеримент, беше използвано за определяне на относителното изобилие на всеки член на общността.
Когато се разглежда като цяло, всяка мутантна библиотека действа подобно на родителския щам от див тип по отношение на пропорционалното му изобилие в общността (Фиг. S4B, Таблица S3). И в двете монотонно хранени лечебни групи относителното изобилие от B. cellulosilyticus WH2 е високо, макар и значително по-голямо при животни, хранени с LF/HPP чау (36 ± 1,6% срещу 16 ± 3,1% след 16 дни на диети; p 2 = 0,676, р = 0,001). Относителното изобилие от мутанти на B. celulosilyticus беше забележително последователно между мишки с индивидуална клетка, монотонно хранени с дадена диета, включително групи мишки, настанени в различни гнотобиотични изолатори (несдвоен t-тест на Student; фиг. S6A). Тази последователност на групата в рамките на лечението се запазва, тъй като конфигурацията на мутантната популация еволюира през следващите 11 дни на монотонна консумация на диета [Фиг. 1В, фиг. S6B, С; тъй като сравнихме библиотека INSeq на даден единичен вид/щам след in vivo селекция при различни диетични лечения, използвахме нефилогенетичната метрика на Хелингер (11), за да изчислим различията между библиотеките в рамките на или между лечебните групи].
Мулти-таксон INSeq на фекални проби, събрани в края на 16 дни на монотонна диета, дава 550 HF/HS специфични за диетата детерминанти на B. cellulosilyticus и 34 LF/HPP диетични детерминанти: 244 от 550 HF/HS диета- специфични гени са имали назначения по KEGG Orthology (KO); сред тази група имаше значително обогатяване на гени, принадлежащи към категориите KEGG „Мембранен транспорт“ (например, един оперон, участващ в транспорта на желязо, друг, участващ в транспорта на фосфати), „Метаболизъм на кофактори и витамини“ [напр., седем гена в пътят на биосинтеза на кобаламин, съобразен с мнението, че способността за синтезиране и използване на кобаламин и други заместени корени е важен фактор, определящ оцеляването в червата (9, 12)], и „Сгъване, сортиране и разграждане на протеини“ (вж. таблица S4A за функционалните анотации и индексите за годност на тези гени).
Последващият анализ на INSeq на същите проби от фекална ДНК, използвани за COPRO-Seq, даде възможност едновременно да се характеризира степента, до която съвкупните колекции от мутанти на B. cellulosilyticus и B. ovatus са били в състояние да продължат и да се възстановят от диетично нарушение (INSeq- базирана дефиниция за устойчивост и стабилност) и вариацията при такова възстановяване между животните (INSeq-базирана мярка за стохастичност). Библиотеката на B. cellulosilyticus WH2 INSeq показа висока устойчивост на кратките диетични смущения в смисъл, че библиотеката като цяло се запази по време на експеримента, въпреки че някои отделни мутанти не. Той обаче не показа същата стабилност, каквато имаше 15-членната общност; при мишките, които са имали диетични трептения, разстоянията на Хелинджър показват, че библиотеката от мутанти не се е сближила до същото състояние като при монотонно хранени мишки, а по-скоро се е запазила като преконфигурирана популация. Това може да се види от разстоянията на Хелинджър между библиотеките в края на експеримента, когато диетата обяснява 38,7% от дисперсията, но взаимодействието между диетата и лечението обяснява 35,1% (PERMANOVA, p = 0,001, фиг. S7B) - a стойност много по-голяма от неговата обяснителна сила преди трептенето на диетата (R 2 = 8,2%).
Идентифициране на основни in vivo фитнес детерминанти в четири щама Bacteroides
Гените, които са запазени сред четирите щама Bacteroides и които показват значителен ефект върху фитнес във всички щамове и в двата диетични контекста, могат да бъдат определени като основен набор от in vivo детерминанти за тези членове от този род; като такива те ни информират за ресурсните изисквания и селективния натиск, който тези таксони изпитват в червата в този контекст на общността и при тези две диетични условия.
Идентифициране на хранителна добавка, която може конкретно да манипулира изобилието на B. cellulosilyticus
B. cellulosilyticus WH2 е снабден с повече въглехидратни активни ензими (CAZYmes), посветени на смилането на гликани, отколкото който и да е друг секвениран геном на Bacteroidetes, докладван до момента (7). Неговите 510 CAZYmes, съдържащи гликозидни хидролази, полизахаридни лиази, въглехидратни естерази и свързани, некаталитични модули за свързване на въглехидрати, са разпределени между 113 PUL. Забележително е, че само един от 113 PUL (BcellWH2_04321-4327) функционира като важен фитнес детерминант в контекста на HF/HS диета (Фиг. 3А). Индексите за годност на 127 Tn мутанти, които са картографирани на шестте гена в този PUL, са забележително еднакви между отделните клетки в клетка като функция от тяхната диета. Освен това, както беше отбелязано по-горе, относителното изобилие от тези мутанти е по-високо при мишки, които са претърпели HF/HS-LF/HPP-HF/HS диетично трептене, отколкото при мишки, монотонно хранени с HF/HS диета (Фиг. 3А). Този PUL се съдържа в област от генома, обхващаща BcellWH2_04292-BcellWH2_04327, която съдържа три хибридни двукомпонентни системи (вж. Допълнителни резултати и фиг. S12 за анализ на предполагаемите регулатори на HTCS в този геномен регион).
(A) Анализът INSeq разкрива, че всички гени в PUL BcellWH2_04321-4327 имат значими индекси за фитнес (z-стойности) в контекста на HF/HS диета. BACWH2_04327, кодиращ регулатор на хибридна двукомпонентна система (HTCS), е единственият ген в този PUL, който има значителен фитнес ефект върху диетата LF/HPP. Показани са функционални анотации за гени в PUL заедно с посоката на тяхната транскрипция. Индексите за фитнес за всеки ген в различния контекст на диетата (оранжев, HF/HS; зелен LF/HPP) са нанесени като средни стойности ± SEM. Хоризонталната пунктирана линия показва границата за значимост (p Фиг. 3A, фиг. S12A, B). GC/MS анализ на продуктите на киселинна хидролиза от HF/HS диетата разкрива малки количества ксилоза и арабиноза (61,2 ± 7,5 µg/g и 62,8 ± 6,2 µg/g, съответно). Нашите предишни проучвания за растеж in vitro на B. cellulosilyticus WH2, култивирани в минимална среда, допълнена с един от 31 отделни въглехидратни субстрата, плюс анализ на RNA-Seq на бактерията, възстановена в средата на логарита от тези минимални среди, които поддържат нейния растеж, разкриват, че това PUL се индуцира от ксилан и арабиноксилан (7; Фиг. S13A). Арабиноксиланите са направени от ксиланов гръбнак с α-L-арабинозни странични вериги. Те също така съдържат ферулова киселина и други фенолни киселини, които са ковалентно свързани с тях чрез естерни връзки. Вероятна роля за продукта на член на семейството BcellWH2_04321 в контекста на този специфичен PUL би била отстраняването на феруловите естери от арабиноксилан. Ксиланазата GH10 е насочена към гръбнака на ксилана, докато ензимът GH35 вероятно премахва α-свързаните L-арабинозни странични вериги (α-L-арабинозата е идентична с β-D-галактозата, с изключение на C-6 частта).
B. ovatus, единственият друг щам на Bacteroides в изкуствената общност, който може да расте в минимална среда, съдържаща пречистен арабиноксилан като единствен източник на въглерод (фиг. S13B), съдържа PUL (Boavatus_01723-32), който се индуцира, когато тази среда се допълва с арабиноксилан (или ксилан) (6). Мулти-таксон INSeq на фекални проби, събрани от мишки, приютяващи 15-членна общност, показа, че за разлика от индуцируемия ксилан и арабиноксилан B. cellulosilyticus PUL BcellWH2_04321-27, този PUL не е необходим за оцеляване на B. ovatus при HF/HS диета контекст (т.е. Tn мутантите в неговите гени SusC и ксиланаза не произвеждат значителни дефекти във фитнеса; фиг. S13C).
Анализът на COPRO-Seq на фекални проби, събрани в края на всеки 14-дневен период на лечение, показва, че арабиноксилан води до значително увеличение на изобилието на B. cellulosilyticus при мишки, хранени с диета HF/HS (коригирана р-стойност, фиг. 3С), но няма значителни ефект в контекста на LF/HPP диета (вж. ден 30 спрямо ден 14 времеви точки за група С). В съответствие с резултатите от INSeq, които показват, че използването на арабиноксилан PUL при B. ovatus не е определящ за фитнеса в контекста на HF/HS диета, не наблюдаваме значителни ефекти от лечението с арабиноксилан върху относителното изобилие на този член на общността (Фиг. 3C). Ние потвърдихме тези констатации в отделен експеримент, при който две групи мишки с гнотобиотици, приютяващи 15-членна общност, бяха лекувани в продължение на 56 дни с HF/HS диета със или без добавяне на питейната си вода с 15% (w/v) арабиноксилан. При тази по-висока доза, по-голяма продължителност, монотонен диетичен експеримент, изобилието от B. cellulosilyticus WH2 се е увеличило значително (както и нивата на цекални късоверижни мастни киселини и деконюгирани жлъчни киселини), докато B. ovatus не е показал отговор (Фиг. S14A, B ). Лечението с арабиноксилан не е довело до статистически значима разлика в общото телесно тегло (t-тест на Student).
Общо 27 гена бяха идентифицирани в генома на B. cellulosilyticus, който функционираше като значими детерминанти на фитнеса, когато мишките получават HF/HS диета плюс арабиноксилан, но не и когато животните получават само HF/HS диета (Таблица S11A). Те включват: (i) всички гени в оперон (BcellWH2_00893-895), който включва сулфотрансфераза и сулфатна трансфераза (EC 3.7.74), в съответствие с наблюдаваното увеличение на деконюгираните жлъчни киселини, документирано от UPLC-MS на цекулното съдържание (Фиг. S14C) и (ii) няколко гена, които подчертават как увеличаването на наличността на арабиноксилан засилва значението на използването на амоний за синтез на аминокиселини и протеини в тази общност и диетичен контекст [амониев транспортер (BcellWH2_05255), плюс глутамин и глутамат синтетази ( BcellWH2_5244 и BcellWH2_05271, съответно)]].
Въпреки че B. ovatus не е показал значителна промяна в относителното си изобилие, когато мишките са получавали вода с добавка на арабиноксилан, мулти-таксон INSeq разкрива 41 гена, които не са определящи фитнеса, когато мишките консумират диета HF/HS, но „придобиват“ значителна z- резултати при въвеждането на арабиноксилан (за списък вж. таблица S11B). Те включват седем тясно свързани гена на гликозилтрансфераза (Bovatus_03504-11), което предполага, че този организъм променя своите стратегии за използване на гликан, когато срещне арабиноксилан в чревната среда.
Проспект
Не можем да различим прякото въздействие на дадена диета или диетични трептения върху даден член на общността от основния ефект на тази диета или смущения в диетата върху един или повече други членове на общността, които взаимодействат с члена/щама, показващ промени в изобилието му. Можехме да се ограничим до моноколонизации, за да установим директни ефекти от диетата върху тези характеристики, но бихме загубили способността си да описваме тези реакции и да установяваме нишите на тези организми в по-„естествения“ контекст на микробна общност.
- Генетични доказателства за човешката адаптация към сготвена диета
- Диета за човешките същества Видео - Опция за директно изтегляне
- Характеризиране на калциевите съединения в Opuntia ficus indica като източник на калций за човешка диета
- Диетични съвети, работещи върху здравето на яхта; Фитнес PYTUSA
- Диетата, в която липсва цинк, е вредна за здравето на хората и животните. Дори умереният дефицит на цинк е лош