Резюме
Заден план
Животинските модели на безалкохолен стеатохепатит (NASH) са важни инструменти в предклиничните изследвания и откриването на лекарства. Gubra-Amylin NASH (GAN) индуцирани от диета затлъстели мишки (DIO) представляват модел на фиброзиране на NASH. Настоящото проучване директно оценява клиничната преносимост на модела чрез сравнение главата до главата на хистологични и транскриптомни промени на чернодробна биопсия при пациенти с мишка GAN DIO-NASH и хора NASH.
Методи
Мишките C57Bl/6 J са хранени с чау или с диета GAN, богата на наситени мазнини (40%), фруктоза (22%) и холестерол (2%) в продължение на ≥38 седмици. Бяха оценени метаболитните параметри, както и биомаркерите в плазмата и черния дроб. Хистологията на чернодробната биопсия и подписите на транскриптома са сравнени с проби от хора с постно тегло и пациенти, диагностицирани с NASH.
Резултати
Чернодробните лезии при мишки GAN DIO-NASH показват сходни морфологични характеристики в сравнение с набора за валидиране на пациентите с NASH, включително макростеатоза, лобуларно възпаление, дегенерация на балониране на хепатоцити и перипортална/перисинусоидална фиброза. Хистоморфометричният анализ показва сравними увеличения на маркерите за чернодробно натрупване на липиди, възпаление и отлагане на колаген при мишки GAN DIO-NASH и проби от пациенти с NASH. Чернодробните биопсии от мишки GAN DIO-NASH и пациенти с NASH показват сравнима динамика в няколко пътища на генна експресия, участващи в патогенезата на NASH. В съответствие с клиничните характеристики на NASH, мишките GAN DIO-NASH демонстрираха ключови компоненти на метаболитния синдром, включително затлъстяване и нарушен глюкозен толеранс.
Заключения
Моделът на мишка GAN DIO-NASH демонстрира добра клинична преносимост по отношение на хистопатологичните, транскрипционните и метаболитните аспекти на човешкото заболяване, подчертавайки пригодността на модела мишка GAN DIO-NASH за идентифициране на терапевтични цели и характеризиране на нови лекарствени терапии за NASH.
Заден план
Безалкохолната мастна чернодробна болест (NAFLD) включва континуум от чернодробни лезии, вариращи от проста стеатоза до неалкохолен стеатохепатит (NASH), който в допълнение към стеатозата се характеризира с лобуларно възпаление и дегенерация на хепатоцелуларен балон [1]. NASH се очерта като основно предизвикателство за общественото здраве поради нарастващото му разпространение в световен мащаб, трудностите при диагностицирането, риска от тежки усложнения и липсата на ефективни терапии. Наличието на метаболитен синдром, по-специално затлъстяването и диабет тип 2, е най-силният предразполагащ фактор за развитие и прогресия на NAFLD [2]. Докато обикновената стеатоза обикновено има доброкачествен ход, пациентите с NASH и фиброза носят повишен риск от чернодробни усложнения, включително цироза, хепатоцелуларен карцином и краен стадий на чернодробно заболяване. В резултат на това NASH се очаква скоро да стане водеща индикация за чернодробна трансплантация [3].
Настоящото проучване има за цел да потвърди допълнително клиничната преносимост на индуцирани от диетата GAN чернодробни лезии чрез сравняване на чернодробна биопсия хистопатологични и транскриптомни характеристики при мишки GAN DIO-NASH и хора NASH пациенти.
Методи
Човешки субекти
Животни
Датската инспекция за опити с животни одобри всички експерименти, които бяха проведени, използвайки международно приети принципи за използване на лабораторни животни (лиценз № 2013-15-2934-00784). C57BL/6 J мишки (на 5 седмици) бяха от лаборатории Janvier (Le Genest Saint Isle, Франция) и бяха настанени в контролирана среда (12 часа цикъл светлина/тъмнина, светлини в 3 часа сутринта, 21 ± 2 ° C, влажност 50 ± 10%). Всяко животно беше идентифицирано чрез имплантируем подкожен микрочип (PetID Microchip, E-vet, Haderslev, Дания). Мишките са имали свободен достъп до чешмяна вода и чау (3,22 kcal/g, Altromin 1324, Brogaarden, Hoersholm, Дания) или Gubra Amylin NASH диета [GAN диета, 4,49 kcal/g, 40 kcal-% мазнини (от тези 46% наситени мастни киселини по тегло), 22% фруктоза, 10% захароза, 2% холестерол; D09100310, Изследователски диети]. Мишките са били хранени с чау или GAN диета в продължение на 38–44 седмици. Животните бяха прекратени чрез сърдечна пункция под изофлуранова анестезия.
Точкуване по хистопатология
Полуколичествено хистопатологично точкуване е извършено при оцветени с HE- и PSR хора (здрави индивиди с нормално тегло, н = 14; Пациенти с NASH, н = 16) и мишка (мишки, хранени с чау, н = 10; GAN DIO-NASH мишки, н = 25) чернодробни проби по заслепен начин от опитни хепато-хистопатолози, използващи NAFLD Activity Score (NAS) и система за определяне на фиброза съгласно критериите на Brunt, модифицирани от Kleiner et al. [27]. Резултатът от NAS е дефиниран като непретеглена сума от оценките за стеатоза (0–3), лобуларно възпаление (0–3) и балониране (0–2), като по този начин варира от 0 до 8. Чернодробната фиброза се оценява въз основа на петстепенна скала, т.е. липса на фиброза (етап 0), перисинусоидална или портална фиброза (етап 1), перисинусоидална и портална/перипортална фиброза (етап 2), септална или свързваща фиброза (етап 3), цироза (и етап 4).
Чернодробна хистоморфометрия
Човешки чернодробни биопсии (здрави индивиди с нормално тегло, н = 14; Пациенти с NASH, н = 11) и лобуларни проби на мишки (мишки, хранени с чау, н = 10; GAN DIO-NASH мишки, н = 25) бяха фиксирани за една нощ в 4% параформалдехид, вградени в парафин и разрязани (3 μm дебелина). Секциите бяха оцветени с хематоксилин-еозин (HE), анти-галектин-3 (кат. 125 402, Biolegend, Сан Диего, Калифорния) или picro-Sirius Red (PSR, Sigma-Aldrich, Broendby, Дания), използвайки стандартни процедури [28, 29]. Фракционната (%) площ на чернодробните липиди (HE-оцветяване), възпалението (галектин-3) и фиброзата (PSR) е изразена спрямо общата площ на секцията.
Анализ на секвениране на РНК на черния дроб
Резултати
Сравними чернодробни хистопатологични белези GAN DIO-NASH мишки и пациенти с NASH
Индивидуалните хистопатологични резултати при биопсии на черен дроб при мишки и хора са посочени в Таблица 1. Здравите индивиди с нормално тегло са имали чернодробна хистология с нормален обхват. Пациентите с NASH показват умерено-тежка стеатоза (степен 2-3), леко лобуларно възпаление (степен 1) и леко до видно балониране на хепатоцитите (степен 1-2). 13 от 16 пациенти с NASH са диагностицирани с фиброза, варираща от лек до умерен стадий (F1-F2). В сравнение с нормалната чернодробна хистология при контролни мишки, хранени с чау, всички GAN DIO-NASH мишки показват тежка стеатоза (степен 3) с различна тежест на лобуларното възпаление. Когато е налице, балонната дегенерация на хепатоцитите е лека (степен 1). 22 от 25 GAN DIO-NASH мишки са развили чернодробна фиброза, почти всички с лек до умерен стадий на фиброза (F1-F2). Сравнително сходната тежест на заболяването при пациенти с NASH и мишки с GAN DIO-NASH се отразява чрез сравними резултати от активността на NAFLD (пациенти с NASH, NAS 5–6; мишки с GAN DIO-NASH, NAS 4–7), вижте Таблица 2. HOMA-IR беше значително се увеличава при пациенти с NASH (7,6 ± 1,0, стр Таблица 1 Сравнение на резултатите от хистопатологията на чернодробна биопсия при пациенти с NASH при хора и GAN DIO-NASH мишки
Сравними количествени хистопатологични промени в черния дроб при GAN DIO-NASH мишки и пациенти с NASH
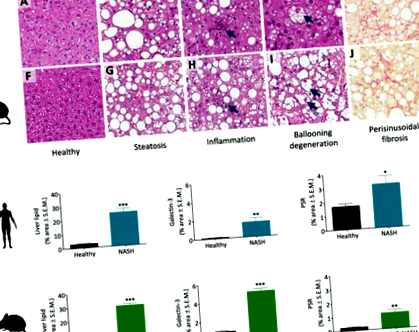
Количествените нива на чернодробна мастна тъкан (HE оцветяване), възпалителна клетъчна инфилтрация (galectin-3 IHC) и отлагане на колаген (PSR оцветяване) са сравнени при чернодробни биопсии при хора и мишки (фиг. 1). Пациенти с NASH (н = 11) демонстрира значително увеличение на фракционната (%) площ на чернодробната мазнина (8-кратно увеличение; 24,2 ± 2,6 срещу 2,9 ± 0,4%, стр Фиг. 2
Регулиране на свързани с болестта кандидат-гени при пациенти с NASH и мишки GAN DIO-NASH. а Гени, свързани с болестта, свързани с черния дроб, б Избрани чернодробни гени, представляващи различни лекарствени цели за NASH. Цветовите градиенти показват значително увеличена (червен цвят) и понижена (син цвят) генна експресия при пациенти с NASH (н = 16) и GAN DIO-NASH мишки (н = 25) в сравнение със съответната контролна група (здрави човешки индивиди с нормално тегло, n = 14; мишки, хранени с чау, н = 10). Кандидат-гените са изброени в таблица S1
Мишките GAN DIO-NASH демонстрират нарушен глюкозен толеранс
В сравнение с контроли, хранени с чау, мишките GAN DIO-NASH показват значително повишено телесно тегло, увеличена маса на цялото тяло (затлъстяване) и хепатомегалия при прекратяване (фиг. 4A-4D). IpGTT беше извършен при мишки, хранени с чау и GAN DIO-NASH, една седмица преди прекратяване. Докато изходните и пиковите нива на глюкоза са сходни при мишки, хранени с чау и GAN DIO-NASH, екскурзии с глюкоза (t = 60–120 минути, стр = 0,0029–0,0002) и нива на AUC на глюкоза (стр = 0,0062) са значително повишени при GAN-DIO NASH мишки, което означава нарушен глюкозен толеранс при GAN DIO-NASH мишки (Фиг. 4д). GAN DIO-NASH мишки демонстрираха хиперинсулинемия и съответно значително увеличиха HOMA-IR индекса в сравнение с мишки, хранени с чау (фиг. 4f, g). Мишките GAN-DIO NASH също проявяват хиперлептинемия и хиперхолестеролемия (фиг. 4h, i). Докато нивата на свободни мастни киселини в плазмата са склонни да бъдат повишени (стр = 0,05), плазмените концентрации на TG са непроменени (стр = 0,75) при GAN DIO-NASH мишки (фиг. 4j, k).
Биохимични промени в плазмата и черния дроб при мишки GAN DIO-NASH
Други анализирани биохимични параметри на плазмата и черния дроб са посочени в Таблица 3. GAN DIO-NASH мишките показват значително повишени нива на плазмени маркери за чернодробно увреждане (ALT, AST; и двете стр Таблица 3 Повишени биохимични маркери в плазмата и черния дроб при мишки GAN DIO-NASH
Повишени нива на циркулиращи и чернодробни цитокини/хемокини при GAN DIO-NASH мишки
Плазмените и чернодробните нива на цитокини/хемокини са показани в Таблица 4. Както плазмените, така и чернодробните концентрации на TNF-α (плазма, p Таблица 4 Повишени плазмени и чернодробни нива на цитокини при GAN DIO-NASH мишки
Дискусия
Като се има предвид липсата на основани на доказателства ефективни терапии за NASH, има подчертана необходимост от животински модели, които да рекапитулират по-добре основните характеристики на заболяването. Следователно настоящото проучване оценява клиничната преносимост на модела на мишка GAN DIO-NASH, като извършва сравнение на хистологични и транскриптомни промени в чернодробни биопсии от мишки GAN DIO-NASH и хора NASH при пациенти. Основните открития са значителна клинична преносимост на модела на мишка GAN DIO-NASH по отношение на хистопатологичните, транскрипционните и метаболитните аспекти на човешкия NASH. Това подчертава пригодността на модела на мишката GAN DIO-NASH за идентифициране на терапевтични цели и характеризиране на нови лекарствени терапии за NASH.
Тъй като резултатите от NAS и фиброза са полуколичествени и осигуряват ограничен обхват от данни за отговора, за обективна количествена оценка на хистологичните промени е приложена образна хистоморфометрия. Количественият хистологичен анализ потвърждава подчертано липидно натрупване, повишена инфилтрация на имунни клетки и значително отлагане на колаген при мишки GAN DIO-NASH и пациенти с NASH. В съответствие с по-високите хистопатологични резултати в кохортата GAN DIO-NASH в сравнение с пациентите с NASH, мишките GAN DIO-NASH показаха относително по-големи количествени промени в хистопатологичните белези на NASH.
Заключения
В заключение, мишката GAN DIO-NASH демонстрира добра клинична преносимост по отношение на физиологичните, метаболитни и хистопатологични аспекти на фиброзирането на NASH, заедно със силно съответствие с чернодробния транскриптомен подпис на човешкото заболяване. Следователно, ясните метаболитни и хистопатологични отличителни белези на NASH подчертават пригодността на модела GAN DIO-NASH за определяне на терапевтични цели и характеризиране на нови лекарствени терапии за NASH.
Наличност на данни и материали
Данните за последователността на РНК са достъпни в базата данни на NCBI GEO под номер на присъединяване. GSE126848. Други набори от данни, използвани и/или анализирани по време на настоящото проучване, са достъпни от съответния автор при разумна заявка.
- Джиан-Ган-Сяо-Джи отварата подобрява високомаслените високо-въглехидратни диети, предизвикани от диета
- Повишените плазмени нива на липидите обострят мускулната патология в модела mdx мишка на Дюшен
- Диетите с високо съдържание на мастни киселини и високо съдържание на захар могат да причинят мишки с безалкохолен стеатохепатит с
- Идентифициране на нови мРНК и lncRNAs, свързани с експериментален колит на мишки и човек
- Екстрактът от зелено кафе модифицира телесното тегло, серумните липиди и TNF-α при затлъстяване, предизвикано от диета с високо съдържание на мазнини