Сузане М. де ла Монте
1 Отделение по патология, болница Роуд Айлънд и Медицинското училище Уорън Алперт към Университета Браун, Провиденс, Род Айлънд
2 Катедра по клинична неврология, болница Роуд Айлънд и Медицинското училище Уорън Алперт към Университета Браун, Провиденс, Род Айлънд
3 Катедра по медицина, болница Род Айлънд и Медицинското училище Уорън Алперт към Университета Браун, Провиденс, Род Айлънд
Джак Р. Жезли
3 Катедра по медицина, болница Род Айлънд и Медицинското училище Уорън Алперт към Университета Браун, Провиденс, Род Айлънд
Резюме
Въведение
Интересът към изясняване на ролята на T2DM, инсулинова резистентност и хиперинсулинемия във връзка с когнитивно увреждане, свързани с AD невронални цитоскелетни лезии или APP-Aβ отлагания в мозъка започна около 2000 г., 4,8,14,19–24, но оттогава 2005, това поле буквално избухна с нова информация и нова концепция, т.е. че първичната мозъчна резистентност към мозъка и дефицитът на инсулин медиират когнитивното увреждане и AD. 5,10,25–29 Тази идея се подхранва от доказателства, че тау генната експресия и фосфорилирането се регулират чрез сигнални каскади на инсулин и инсулиноподобен растежен фактор (IGF). 23,24 В допълнение, изследванията, проведени в нашата лаборатория, показаха, че много ключови аспекти на дегенерацията на централната нервна система (ЦНС), които се появяват при АД, могат да бъдат постигнати чрез нарушена инсулинова сигнализация. 30–33
Като преглед инсулинът и IGF-1 медиират своите ефекти чрез активиране на сложни вътреклетъчни сигнални пътища, започвайки с свързване на лиганд с рецепторите на клетъчната повърхност, последвано от автофосфорилиране и активиране на вътрешните рецепторни тирозин кинази. 34–36 Инсулин/IGF-1 рецепторни тирозин кинази фосфорилират IRS молекули, 34,37–39, които предават сигнали надолу по веригата чрез активиране на извънклетъчната свързана със сигнала киназа/митоген-активирана протеин киназа (ERK/MAPK) и PI3 киназа/Akt пътища, и инхибират гликоген синтазата киназа 3β (GSK-3β). Основните биологични отговори на сигнализирането чрез IRS молекули включват повишен клетъчен растеж; оцеляване, енергиен метаболизъм и експресия на холинергичен ген; и инхибиране на оксидативния стрес и апоптозата. 39–46 Същите тези сигнални пътища се активират в различни видове клетки, тъкани и целеви органи, които експресират инсулинови и IGF рецептори и следователно са практически универсални. Освен това, тези пътища са филогенетично запазени и имат критична роля в регулирането на развитието, растежа, оцеляването, стареенето, канцерогенезата и невродегенерацията.
Потенциални роли на затлъстяването и захарен диабет тип 2 при патогенезата на болестта на Алцхаймер
Епидемиологичните проучвания предоставят убедителни доказателства за значителна връзка между T2DM и MCI или деменция и освен това предполагат, че T2DM е важен рисков фактор за развитие на AD. 47,69–73 Въпреки това, тези констатации не са без противоречия, 74 и в надлъжно проучване изследователите установяват, че въпреки че граничните диабетици са имали значително повишен риск за бъдещо развитие на диабет, деменция или AD, рисковите ефекти са по-скоро независими, отколкото свързани. Това, което означава, е, че инсулиновата резистентност, т.е. нарушената способност да се реагира на инсулинова стимулация, може да варира между целевите органи и да присъства само в един или два органа, а не в други, феномен, който може да обясни липсата на пълно припокриване между T2DM и AD. Съответно, констатацията, че затлъстяването (индекс на телесна маса [ИТМ]> 30) без T2DM води до трикратно увеличаване на риска за последващо развитие на АД, докато субектите с наднормено тегло, но неблагоприятни (BMI 25–30) имат двукратно увеличение на рискът за AD 76 поставя под съмнение специфичните ефекти на затлъстяването и T2DM спрямо все още неизвестен свързан фактор във връзка с патогенезата на AD.
Болестта на Алцхаймер е диабет тип 3: доказателства от изследвания върху хора
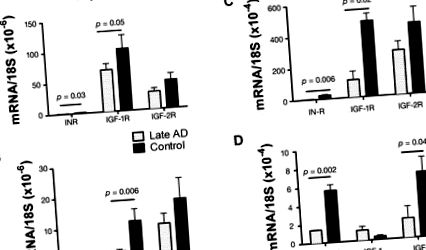
Нарушен инсулин и IGF (A, C) рецептор и (B, D) експресия на полипептиден ген в късен/краен стадий на AD (A, B) темпорална кора и (C, D) хипокампус. 5 Експресията на гени се измерва чрез qRT-PCR, като се използва РНК, изолирана от темпоралната кора или хипокампуса от хистопатологично потвърдени случаи на тежко АД или нормално стареене след смъртта. Ние обърнахме транскрипция на иРНК и получената сДНК беше PCR амплифицирана. Продуктите се откриват непрекъснато с многоцветна система за откриване на PCR в реално време BIO-RAD iCycler. Експресията на гена се нормализира до 18S rRNA, измерена в същите проби. Графиките изобразяват средното ± стандартно отклонение на резултатите, получени от 28 AD и 26 контролни случая. Данните бяха анализирани с помощта на t-тестове на Student. Значителните р-стойности са посочени над лентите. Обърнете внимание, че експресията на ген на инсулин не е открита в темпоралната кора.
Още преди публикуването на първоначалното проучване беше осъзнато, че ако мозъчната инсулинова/IGF резистентност и дефицитът на инсулин/IGF са причинени в патогенезата на AD, свързаните с тях аномалии трябва да бъдат открити в ранните стадии на заболяването и евентуално да се влошат с напредването на заболяването . Изследванията бяха разширени, за да се изследват мозъците на пациенти с различна степен, т.е., стадии на Braak, 86,87 от AD. 10 В това проучване измерихме експресията на гени, кодиращи инсулин, IGF-1, IGF-2 полипептиди и съответните им рецептори, както и тау и амилоиден предшественик протеин (APP). В допълнение, ние използвахме конкурентни анализи за равновесие и насищане, за да характеризираме по-нататък степента, до която сигнализирането, предадено от растежен фактор, беше нарушено в мозъка с различна тежест на AD. И накрая, проучването включва измерване на стационарни нива на аденозин трифосфат и гени, регулиращи ацетилхолиновата хомеостаза и енергийния метаболизъм.
Използвайки споменатите по-горе подходи, ние демонстрирахме прогресивно намаляване на експресията на инсулин, IGF-1 и IGF-2 на рецепторите, зависещо от етапа на Braak, с по-изразено влошаване на инсулина и IGF-1 в сравнение с IGF-2 рецепторите и най-ниските нива на генна експресия в мозъка с AD Braak Stage 6 ( Фигура 2 ). Следователно загубата на инсулин и невроните, носещи IGF-1 рецептор, започва рано и прогресира с болест, така че в напредналите стадии дефицитът е тежък и глобален. Тези резултати предоставиха допълнителни доказателства, че аномалиите в AD не са ограничени до инсулиновите сигнални пътища, тъй като те също включват IGF-1 и IGF-2 стимулирани механизми. Анализът на полипептидните гени на растежен фактор също разкрива AD Braak зависими от етапа увреждания на експресията на инсулин, IGF-1 и IGF-2 полипептид, съответстващи на прогресивно отнемане на трофичния фактор ( Фигура 2 ). Отново, резултатите подкрепят хипотезата, че аномалиите в инсулиновите и IGF сигналните механизми започват в началото на AD и следователно вероятно имат важна роля в неговата патогенеза.
Дефицитът и резистентността на мозъчния инсулин и IGF се увеличават с прогресирането на AD. 10 Postmortem хистопатологични проучвания категоризират мозъците като нормално стареене (Braak 0–1) или леко (Braak 2–3), умерено до тежко (Braak 4–5) или краен стадий (Braak 6) AD. Използвахме иРНК, изолирана от прясно замразена тъкан на фронталния лоб, за измерване на инсулин, IGF-1 или IGF-2 (А) полипептид или (Б) експресия на рецепторния ген чрез qRT-PCR. Резултатите бяха нормализирани до 18S рРНК, измерена в същите проби. (° С) За конкурентните анализи на равновесно свързване екстрактите от мембранни протеини на фронталния лоб се инкубират с белязан с [125 I] инсулин, IGF-1 или IGF-2 в присъствието или отсъствието на излишен студен лиганд. Радиоактивността в мембранните протеинови утайки се измерва в гама брояч. Специфичното свързване (fmol/mg) беше изчислено с помощта на софтуера GraphPad Prism 4. Всички графики изобразяват средното ± стандартно отклонение на резултатите, получени от 9-12 случая на група. Направени са междугрупови сравнения, като се използва дисперсионен анализ (ANOVA) с post hoc тестове за значимост на Tukey-Kramer. Значителните р-стойности са посочени над лентите. Забележете пробив на оста Панел Б.
Евентуалната оскъдност на експресията на гена на локален растежен фактор може значително да наруши сигнализирането на растежен фактор и да доведе до състояние на отнемане на растежен фактор, което е добре установен механизъм на невронна смърт. Следователно, за да допълним молекулярните данни, извършихме конкурентни анализи за равновесие и насищане, за да определим дали намалените нива на експресия на рецептор на растежен фактор са свързани и може би медиирани от нарушено свързване на лиганд-рецептор, както се случва при инсулин/IGF резистентност. Тези разследвания демонстрираха прогресивно намаляване на равновесието ( Фигура 2 ) и свързване на най-високо ниво (Bmax) с инсулиновите, IGF-1 и IGF-2 рецепторите, но или непроменен, или повишен афинитет на свързване, което предполага, че нарушените действия на инсулин/IGF в мозъците на AD са медиирани от намалена експресия на полипептид и рецепторни гени поради до загуба на клетки.
Болестта на Алцхаймер е диабет тип 3: Резултати от експериментални животински модели
Изследванията на човешкия мозък след смъртта свързват много от характерните молекулярни и патологични характеристики на AD с намалената експресия на гените на инсулин и IGF и съответните им рецептори. Въпреки това, без директно експериментиране, което генерира причинно-следствени данни, заключенията, направени от изследвания върху хора, ще останат по-скоро корелативни, отколкото механистични. Следователно, ние използвахме експериментални модели, за да покажем, че молекулярните и биохимичните аномалии от типа на захарен диабет могат да се получат в невроните на ЦНС и мозъка чрез излагане на стрептозотоцин (STZ). Стрептозотоцинът е 2-дезокси-2D-глюкопираноза, т.е. След като се метаболизира, N нитрозоурейдото се освобождава и причинява увреждане на ДНК чрез генериране на реактивни кислородни видове като супероксид, водороден пероксид и азотен оксид. 99 100 стрептозотоцин причинява диабет, тъй като се приема от клетки, произвеждащи инсулин, като бета клетки, в панкреатичните островчета.
Ние лекувахме плъхове с една интрацеребрална инжекция на STZ (ic-STZ) и оставихме плъховете да остареят за 2 до 8 седмици. Плъховете бяха подложени на тестове за воден лабиринт на Morris за пространствено обучение и памет и мозъците им бяха изследвани за хистопатологични, биохимични и молекулярни индекси на невродегенерация от тип AD.
Въпреки че подобен модел е генериран много по-рано от други изследователи, 101–104 и е отбелязано, че леченията с ic-STZ намаляват използването на церебрална глюкоза 104 и окислителния метаболизъм, 101 инхибира функцията на инсулиновите рецептори 95 и причинява прогресивни дефицити в обучението, памет, когнитивно поведение и мозъчен енергиен баланс, не са положени 94 103 усилия за свързване на тези ефекти на ic-STZ с AD чрез характеризиране на невропатологията, молекулярната патология, аномалии в експресията на гени, свързани с инсулина и IGF-1 сигнализиране в мозъка или чрез оценка на целостта на панкреаса. Нашата цел при генерирането на модела беше да покажем, че невродегенерацията от тип AD с характеристики на T3DM може да бъде произведена при липса на T1DM или T2DM.
Ефекти от интрацеребралното ic-STZ лечение върху експресията на инсулин и IGF в ЦНС (А) гени и (Б) рецептори и (° С) свързване на лиганд с инсулиновите, IGF-1 или IGF-2 рецепторите в тъканта на темпоралния лоб. Кученцата на плъхове получават 50 mg/kg ic-STZ или носител и се жертват 14 дни по-късно. MRNA с темпорален лоб се използва за измерване на генната експресия чрез qRT-PCR и резултатите се нормализират до 18S rRNA, измерена в същите проби. 29 Разбийте оста на бележка Панел А. (° С) Използвани са конкурентни анализи за равновесно свързване за измерване на специфичното свързване към инсулиновите, IGF-1 или IGF-2 рецепторите, както е описано в Фигура 2 . Графиките изобразяват средната стойност ± стандартна грешка на средната стойност на резултатите. Данните бяха анализирани статистически с помощта на t-тестове на Student. Значителните p-стойности са посочени над стълбовидните графики.
Съответно с констатациите в AD, 5 лекуваните с ic-STZ мозъци имат повишени нива на активиран GSK-3β, фосфо-тау, убиквитин, APP и APP-Aβ и намалени нива на тау протеин. Тези резултати са в съответствие с предишни проучвания, доказващи, че тау се регулира от стимулация на инсулин/IGF-1 88,118 и че тау фосфорилирането и убиквитинацията се увеличават с оксидативен стрес и активиране на GSK-3β. 93 По подобен начин, APP иРНК се увеличава с оксидативен стрес и е характеристика на спорадична AD. 5,10 Повишената експресия на APP гена може да обясни натрупването на APP-Aβ в мозъците, лекувани с AD и ic-STZ. Потенциалните източници на оксидативен стрес при AD и моделът ic-STZ включват (1) митохондриална дисфункция; 6,53,95 (2) активиране на микроглиални клетки с повишено освобождаване на цитокини; и (3) нарушено сигнализиране за инсулин/IGF чрез PI3 киназаAkt, което води до повишени нива на активност GSK-3β.
Решаваща стъпка беше да се определи дали ic-STZ може да причини нарушения в ацетилхолиновата хомеостаза и когнитивни увреждания, както се появяват при AD. QRT-PCR и имунохистохимията откриват намалени нива на ChAT и повишени нива на AChE иРНК и протеини в лекувани с icSTZ мозъци спрямо контролните мозъци. Имайте предвид, че енергийният метаболизъм води до производството на ацетил-КоА, който е необходим за производството на ацетилхолин. Тъй като генът ChAT реагира на инсулин и IGF-1 стимулация, дефицитите в сигнализирането на инсулин/IGF и енергийния метаболизъм се насочват в посока на холинергичен дефицит, медииран от нарушен енергиен метаболизъм и намалена експресия на ChAT, които са ключови характеристики при AD. В допълнение, повишените нива на експресия на AChE в мозъците на ic-STZ могат да доведат до повишено разграждане на ацетилхолина, като по този начин се изострят дефицитите на ацетилхолин, причинени от намалената експресия на ChAT. Значимостта на тези резултати се подчертава от забележимите дефицити на обучение и памет, открити при плъхове, лекувани със ic-STZ. 28,29
Диабетът тип 3 може да бъде лечим, предотвратим или лечим с антидиабетни лекарства
Лечението с PPAR агонисти възстановява свързването на мозъчния инсулинов рецептор при плъхове, лекувани с ic-STZ. 28 кученца на дългите Evans бяха третирани с 50 mg/kg ic-STZ или носител и бяха умъртвени 30 дни по-късно, за да се изследват мозъците за инсулин и експресия на полипептид на IGF и рецепторния ген и свързване на инсулин и IGF рецептор. Екстрактите от мембранни протеини на темпоралния лоб бяха използвани в конкурентни анализи за равновесно свързване за измерване на специфичното свързване с (А) инсулин, (Б) IGF-1, или (° С) IGF-2 рецептори, както е описано в Фигура 2 . Графиките изобразяват средната стойност ± стандартна грешка на средната стойност на резултатите. Данните бяха анализирани с помощта на ANOVA с тест за значимост на Tukey – Kramer. Значителните р-стойности са показани във всеки панел.
Лечението с активиран от пероксизомен пролифератор рецептор-5 агонист запазва визуално-пространственото обучение и паметта при плъхове, лекувани с ic-STZ. 28 кученца с дълги Evans бяха третирани с 50 mg/kg ic-STZ или носител, последвано от еднократна интраперитонеална инжекция на PPAR-α (GW7647; 25 µg/kg), PPAR-δ (L-160,043; 2 µg/kg ), или PPAR-γ (FL-Leu; 20 ug/kg) агонист (п = 8 плъхове на група). Четири седмици по-късно плъховете бяха подложени на тестване на воден лабиринт на Морис, при което латентността, необходима за локализиране на скритата платформа, беше измерена за 3 независими изпитания в продължение на 4 последователни дни. Площта под кривата (AUC) е изчислена за 3-те дневни изпитания. Графиките изобразяват средната AUC ± стандартна грешка на средната стойност за латентност (секунди) във всяка група. Данните бяха анализирани с помощта на ANOVA с тест за значимост на Tukey – Kramer. Ефективността в контролната и ic-STZ + PPAR-δ групи беше сходна и на Дни 2, 3 и 4 средните им латентности, необходими за локализиране на скритата платформа, бяха значително по-кратки, отколкото в останалите 3 групи.
Заключения
- Бариатрична хирургия за лечение на хронично бъбречно заболяване при затлъстяване и диабет тип 2
- Алцхаймер; s Диабет тип 3 Д-р
- 10 вредни заблуди относно здравето на диабет тип 2 Лонгевити
- Закуска за диабет тип 2 Смутита, овесени ядки, яйца и др
- 7 дългосрочни цели Всеки с диабет тип 2 трябва да постигне