Катедра по нефрология, артериална хипертония, диализа и трансплантация, Университетски болничен център, Медицински факултет, Университет в Загреб, Загреб, Хърватия
Кореспонденция на: Bojan Jelaković, Медицински факултет, Университет в Загреб, Kišpatićeva 12, 10000 Загреб, Хърватия, тел .: + 385‐95‐9030‐751, E-mail: [email protected] и Иржи Завадил, Международна агенция за изследвания Рак, 150 часа Albert Thomas, 69372 Lyon cedex 08, Франция, Тел .: + 33‐4‐72‐73‐83‐62, ФАКС: + 33‐4‐72‐73‐83‐22, E-mail: zavadilj @ iarc.fr Потърсете още статии от този автор
Група за молекулярни механизми и биомаркери, Международна агенция за изследване на рака, Лион, Франция
Отделение по патология, Обща болница д-р Йосип Бенчевич, Славонски Брод, Хърватия
Група за молекулярни механизми и биомаркери, Международна агенция за изследване на рака, Лион, Франция
Катедра по нефрология, артериална хипертония, диализа и трансплантация, Университетски болничен център, Медицински факултет, Университет в Загреб, Загреб, Хърватия
Група за молекулярни механизми и биомаркери, Международна агенция за изследване на рака, Лион, Франция
Кореспонденция на: Боян Йелакович, Медицински факултет, Университет в Загреб, Кишпатичева 12, 10000 Загреб, Хърватия, тел .: + 385‐95‐9030‐751, E-mail: [email protected] и Иржи Завадил, Международна агенция за изследване на Рак, 150 часа Albert Thomas, 69372 Lyon cedex 08, Франция, Тел .: + 33‐4‐72‐73‐83‐62, ФАКС: + 33‐4‐72‐73‐83‐22, E-mail: zavadilj @ iarc.fr Потърсете още статии от този автор
Катедра по нефрология, артериална хипертония, диализа и трансплантация, Университетски болничен център, Медицински факултет, Университет в Загреб, Загреб, Хърватия
Кореспонденция на: Боян Йелакович, Медицински факултет, Университет в Загреб, Кишпатичева 12, 10000 Загреб, Хърватия, тел .: + 385‐95‐9030‐751, E-mail: [email protected] и Иржи Завадил, Международна агенция за изследване на Рак, 150 часа Albert Thomas, 69372 Lyon cedex 08, Франция, Тел .: + 33‐4‐72‐73‐83‐62, ФАКС: + 33‐4‐72‐73‐83‐22, E-mail: zavadilj @ iarc.fr Потърсете още статии от този автор
Група за молекулярни механизми и биомаркери, Международна агенция за изследване на рака, Лион, Франция
Отделение по патология, Обща болница д-р Йосип Бенчевич, Славонски Брод, Хърватия
Група за молекулярни механизми и биомаркери, Международна агенция за изследване на рака, Лион, Франция
Катедра по нефрология, артериална хипертония, диализа и трансплантация, Университетски болничен център, Медицински факултет, Университет в Загреб, Загреб, Хърватия
Група за молекулярни механизми и биомаркери, Международна агенция за изследване на рака, Лион, Франция
Кореспонденция на: Боян Йелакович, Медицински факултет, Университет в Загреб, Кишпатичева 12, 10000 Загреб, Хърватия, тел .: + 385‐95‐9030‐751, E-mail: [email protected] и Иржи Завадил, Международна агенция за изследване на Рак, 150 часа Albert Thomas, 69372 Lyon cedex 08, Франция, Тел .: + 33‐4‐72‐73‐83‐62, ФАКС: + 33‐4‐72‐73‐83‐22, E-mail: zavadilj @ iarc.fr Потърсете още статии от този автор
Резюме
Съкращения
През последното десетилетие в Хърватския център за ендемична нефропатия е регистрирана по-висока честота на бъбречно-клетъчни карциноми (RCC) с отчетливи епидемиологични и клинични характеристики. 17 По този начин ние имахме за цел да изследваме възможната роля на АА в етиологията на RCC сред пациенти с ХБН от регионите на EN и от близката околност, като анализираме широкоспектърните мутационни спектри в ДНК на тумора.
Материали и методи
Пациентски проби
Бяха анализирани осем пациенти с RCC от фермерските села: петима от EN зона, която преди е била свързана с експозиция на AA поради консумация на замърсен хляб 5, 18 и трима от села в близост до EN региона, в миналото не са докладвани случаи на EN. В допълнение, два случая на RCC от столичния район на Хърватия бяха анализирани като контроли, които е малко вероятно да са били изложени на AA. Клиничните характеристики на пациентите са изброени в таблица 1. Протоколът на проучването включва информираното съгласие на пациентите и етичните одобрения са получени от Етичните съвети на Медицинския факултет на Университета в Загреб, на Общата болница в Славонски Брод и от Комитет по етика на IARC. От осемте пациенти с EN RCC идентифицирахме четирима (EN-01, EN-02, EN-04 и EN-05), които са пекли собствен хляб, трима от които са фермери, прибиращи зърно от местно отглеждана пшеница; един пациент, представен с CTN (EN-01), един с едновременно UTUC (EN-02) и един (EN-06) е бил диагностициран с UTUC пет години преди диагнозата RCC (вж. таблица 1).
| EN ‐ 01 | EN | М | 66 | Изчистване на клетката | 8310/3 | G4 | pT3NxMx | 710 | 5 | 7.0 | Да А а Хронична тубулоинтерстициална нефропатия (CTN). |
| EN ‐ 02 | EN | М | 65 | Изчистване на клетката | 8310/3 | G2 | pT1N0Mx | 162 | 3 | 39.6 | UTUCb б Едновременен тумор. |
| EN ‐ 03 | Близо до EN | М | 42 | Изчистване на клетката | 8310/3 | G2 | pT1N0Mx | 88 | 1 | 93,0 | Не |
| EN ‐ 04 | EN | М | 78 | Изчистване на клетката | 8310/3 | G2 | pT1NxMx | 757 | 5 | 6.4 | Не |
| EN ‐ 05 | Близо до EN | М | 55 | Изчистване на клетката | 8310/3 | G1 | pT1NxMx | 100 | 2 | 72,0 | Yesc ° С Нефролитиаза и RCC в контралатералния бъбрек. |
| EN ‐ 06 | EN | М | 76 | Некласифициран | 8312/3 | G4 | pT3N2Mx | 364 | 4 | 15.1 | UTUCd д UTUC диагностициран 5 години преди RCC. |
| EN ‐ 07 | Близо до EN | F | 64 | Хромофоб | 8317/3 | G3 | pT2NxMx | 75 | 2 | 73,0 | Не |
| EN ‐ 08 | EN | F | 47 | Изчистване на клетката | 8310/3 | G2 | pT2N0Mx | 95 | 3 | 58.1 | Не |
| Ctrl ‐ 01 | Не-EN | F | 56 | Изчистване на клетката | 8310/3 | G3 | pT2N0Mx | 62 | 1 | 91.8 | Не |
| Ctrl ‐ 02 | Не-EN | М | 74 | Изчистване на клетката | 8310/3 | G2 | pT3aN0Mx | 193 | 3 | 31.5 | Не |
- Оценена скорост на гломерулна филтрация въз основа на уравнението за модифициране на диетата при бъбречна болест (MDRD) и не е измерена чрез масово спектрометрично разреждане с изотопно разреждане (IDMS). Последната колона показва бъбречно заболяване на пациента, различно от RCC (UTUC: уротелиален карцином на горните пикочни пътища).
- а Хронична тубулоинтерстициална нефропатия (CTN).
- б Едновременен тумор.
- ° С Нефролитиаза и RCC в контралатералния бъбрек.
- д UTUC диагностициран 5 години преди RCC.
- Съкращения: EN: ендемичен регион; близо до EN: близост; F: женски; М: мъжки; ICD-O: Международната класификация на болестите по онкологичен кодекс; ХБН: хронично бъбречно заболяване; eGFR: изчислена скорост на гломерулна филтрация.
Изолация на ДНК
Препарати на хематоксилин-еозин от фиксирани с формалин парафин-вградени (FFPE) туморни блокове бяха използвани за идентифициране на туморната тъкан без некротични области чрез цифрово сканиране при 20-кратно увеличение (Leica SCN400 Scanner, Leica Biosystems). Туморните области, които трябва да бъдат макродисектирани, са измерени с помощта на безплатния софтуер ImageJ или SlidePath Gateway Client, Leica Biosystems. Десет µm срезове, приготвени от Leica RM 2145 микротом (Leica Microsystems), бяха използвани за изолиране на геномна ДНК (2–3 µg, добив 5–10 ng/mm 2). Преди изолирането на геномна ДНК, предметните стъкла се депарафинизират за 5 минути в 100% ксилен, последвани от 5 минути в абсолютен етанол, 5 минути в 85% етанол, 5 минути в 75% етанол и се държат в milliQ вода. Изолирането на ДНК се извършва с помощта на QIAamp DNA FFPE Tissue kit (Qiagen). Добивът и концентрациите на ДНК се измерват с помощта на анализа Picogreen (Life Technologies) и флуорометъра за микроплаки Fluoroskan Ascent FL (Thermo Fisher Scientific). Чистотата беше оценена от спектрофотометъра NanoDrop 8000 (Thermo Fisher Scientific). Целостта на геномната ДНК се оценява чрез 0,8% агарозна гел електрофореза.
Подготовка на библиотеката и секвениране на цели екзоми (WES)
Последователна обработка и анализ на данни
Четенията за секвениране бяха подравнени от Burrows-Wheeler Aligner, варианти, извикани от инструментариума за анализ на генома (GATK, Broad Institute), анотирани от ANNOVAR и строго филтрирани за премахване на генетични варианти, наблюдавани в общата популация, използвайки данни от публичните проекти 1000 генома (1000ж, http://www.1000genomes.org/), Проект за секвениране на Exome (ESP, http://exome.gs.washington.edu/) и изграждане на база данни SNP 137 (dbSNP, http: //www.ncbi.nlm.nih .gov/SNP /). Варианти, показващи честота по-висока от 0,1% при всеки от 1000ж или ESP бази данни, анотирани в базата данни dbSNP и вътрешен панел от варианти на зародишна линия, генерирани с помощта на данни, получени от 560 случая от Атласа на генома на рака (TCGA, http://cancergenome.nih.gov/), бяха премахнати, както и варианти на картографиране на фрагменти към повтарящи се последователности на генома с хомология по-висока от 90%. Пълният окончателен списък с 4031 варианта на SBS в тестваните, както и контролни проби от RCC ще бъде предоставен при поискване. Необработените данни за секвениране (файловете fastQ и подравняване (.bam)) са депозирани в архива за четене на последователности (SRA, идентификационен номер за достъп SRP049084) на Националния център за биотехнологична информация (NCBI) и могат да бъдат получени чрез базата данни на NCBI за генотипове и Оторизирана система за достъп с фенотипове (dbGaP).
Определяне на мутационния подпис на АА
Резултати
| EN ‐ 01 | 600 | 9.4 | 224 | 3.5 | 37.3 | 23,0 | 1.6 (128/78) | 0,00064 | 0,010 | 228 (38%) | 372 (62%) | Да |
| EN ‐ 02 | 375 | 5.9 | 57 | 0.9 | 15.2 | 11.4 | 2,8 (39/14) | 0,00098 | 0,013 | 256 (68%) | 119 (32%) | Да А а По-нисък процент на A> T и C A G контекст, но поддържан от NMF. |
| EN ‐ 03 | 355 | 5.5 | 17 | 0,3 | 4.8 | 7.0 | 2,5 (10/4) | 0,181 | 0,746 | 355 (100%) | 0 (0%) | - |
| EN ‐ 04 | 249 | 3.9 | 124 | 1.9 | 49.8 | 22.3 | 2,7 (82/30) | 0 | 0 | 0 (0%) | 249 (100%) | Да |
| EN ‐ 05 | 286 | 4.5 | 28 | 0,4 | 9.8 | 8.2 | 1.3 (14/11) | 0,689 | 1 | 231 (81%) | 55 (19%) | - |
| EN ‐ 06 | 977 | 15.3 | 201 | 3.1 | 20.6 | 35,0 | 2.6 (140/53) | 0 | 0 | 623 (64%) | 354 (36%) | Да |
| EN ‐ 07 | 443 | 6.9 | 76 | 1.2 | 17.2 | 23.7 | 1.8 (46/26) | 0,025 | 0,231 | 325 (73%) | 118 (27%) | Да |
| EN ‐ 08 | 159 | 2.5 | 13 | 0.2 | 8.2 | 0,0 | 1,8 (7/4) | 0,546 | 1 | 159 (100%) | 0 (0%) | - |
| Ctrl ‐ 01 | 199 | 3.1 | 15 | 0.2 | 7.5 | 0,0 | 0,6 (5/8) | 0,579 | 1 | 185 (93%) | 14 (7%) | - |
| Ctrl ‐ 02 | 388 | 6.1 | 25 | 0,4 | 6.4 | 7.5 | 0,9 (12/13) | 1 | 1 | 376 (97%) | 12 (3%) | - |
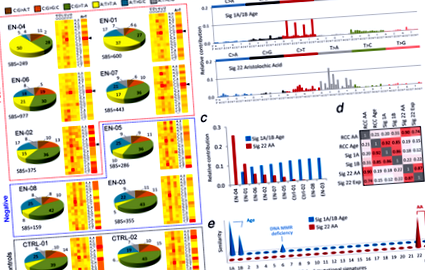
- A> T: A: T> T: A трансверсия; SB A> T: отклонение на нишката, изразено като съотношение на A: T> T: A трансверсии върху нетранскрибираното срещу транскрибирана верига (броят на съответните трансверсии е показан в скоби). % C A G контекст: процент на A: T> T: A трансверсии в най-честия контекст, докладван за подпис на AA. SB стр стойност и процент на фалшиво откриване (FDR) q стойност = мерки за значимост на отклонението на нишката, вижте Материали и методи. Приносът към Sig (Sig = неотрицателна мутационна сигнатура, определена от факторизация на матрицата) се показва като броя на SBS и съответния процент (в скоби) от общия брой на SBS на проба. AA подпис - положителна проба за подпис AA, като се има предвид едновременната поява на ≥50 SBS и ≥15% A> T, ≥20% C A G контекст и неговата значимост (SB стр и/или q стойност) и мутационен принос към Sig 22 (AA).
- а По-нисък процент на A> T и C A G контекст, но поддържан от NMF.
- Съкращение: SBS: замествания с една основа.
Дискусия
Нашето проучване идентифицира специфичния мутационен подпис на АА в набор от пет RCC тумори от пациенти от Балканския регион на EN и в близост, предоставяйки молекулярни доказателства за мутагенен процес, управляван от АА, свързан с канцерогенеза в бъбречната кора и отразяващ АА в етиологията на това тип рак в контекста на ХБН. Докато натоварването с мутация в положителния за подпис на АА EN RCC потвърждава силно мутагенните ефекти на АА, 9, 10, той изглежда по-нисък (4–15 SBS/Mbp) в нашия RCC набор в сравнение с докладваното преди това UTUC с положителен подпис на АА ( 2–65 9 и 8–35 10 SBS/Mbp). Тези разлики налагат по-нататъшни епидемиологични и лабораторни изследвания с използване на по-големи групи пациенти, за да се установи дали те отразяват променливите режими на експозиция на АА във всеки географски регион, скоростите на метаболизиране в отделните типове клетъчни типове, процедурите за вземане на проби, засягащи хетерогенността на тестваните тъкани или други фактори.
Предвид нерегулирания глобален пазар с билки, съдържащи АА, който може да изложи милиони хора на риск, особено в Източна Азия, 3 нашата констатация има потенциално дълбоки последици за повишената информираност за допълнителни видове рак, свързани с AAN. Надеждният дизайн на молекулярно-епидемиологичните изследвания на AAN вече трябва да включва случаи на RCC заедно с пациенти с UTUC и HCC, за да се подобри световното наблюдение на заболяването. Освен това, ние документираме в нов регион и нов тип рак, че чувствителните геномни екрани, съчетани със сложни методи за разлагане на мутационен модел, като NMF, могат да идентифицират АА като фактор за рак на околната среда в AAN и да предоставят стабилна база данни за диагностика и превантивни подходи за премахване на този сериозен проблем на общественото здраве. 3, 25
Благодарности
Благодарим на д-р. Želimir Stipančić и Tvrtko Hudolin за съдействие при събирането на клинични проби и данни, д-р Stephanie Villar и г-жа Christine Carreira за тяхната помощ при обработката на архивирани туморни проби и д-р Magali Olivier за полезни коментари относно анализа на секвениращите данни. Благодарим на Технологичния център за геном на Нюйоркския университет към Нюйоркския университет, Център за рак на Лора и Айзък Перлмутер, за експертна помощ с експериментите за секвениране Illumina HiSeq2500.
- Бърза загуба на тегло с диетично ограничаване на солта при хоспитализирани пациенти с хроничен бъбрек
- Национална фондация за бъбреците с поликистозна бъбречна болест
- Поликистозна бъбречна болест - Palladio Biosciences
- Изследването разглежда загубата на тегло за управление на опасно наследствено бъбречно заболяване UCHealth Today
- Обратно поликистозно бъбречно заболяване Калифорнийски университет