Eftychia Karoutsou 1 *, Petros Karoutsos 2 и Dimitrios Karoutsos 3
1 Ellinon Axiomaticon 17, Kareas, Атина, Гърция
2 Медицински център в Атина, клиника за майчинство Gaia, Vas Sofias 104, Атина, Гърция
3 Катедра по акушерство и гинекология, Обща болница в Ретимно, Атина, Гърция
* Автор-кореспондент: Eftychia Karoutsou
Ellinon Axiomaticon 17, Kareas, Атина, Гърция
Електронна поща: [имейл защитен]
Дата на получаване: 04 ноември 2016 г .; Приета дата: 21 ноември 2016 г .; Дата на публикуване: 28 ноември 2016 г.
Цитат: Karoutsou E, Karoutsos P, Karoutsos D. Затлъстяването и ракът на ендометриума: има ли роля за имунотоксичността? J Clin Epigenet. 2016 г., 2: 4. doi: 10.21767/2472-1158.100032
Резюме
Хроничното възпаление и затлъстяването са реципрочни патофизиологични процеси, лежащи в основата на елемента на имунния отговор. При затлъстяване се смята, че измененията на цитокините допринасят за нискостепенно възпаление в мастната тъкан, засягащо развитието на няколко вторични заболявания. Въпреки че микро-възпалението участва в инициирането на имунен отговор, прекомерното възпаление може да насърчи развитието на тумора. Този преглед ще обсъди рефлексивната връзка между рака на ендометриума и затлъстяването чрез имуномодулиращи ефекти, упражнявани от химикалите в околната среда.
Ключови думи
Химикали за околната среда; Затлъстяване; Цитокини; Хипертония
Въведение
Влияние върху затлъстяването и имунитета
Животинските модели предлагат важна представа за това как метаболитните аномалии, свързани с наднорменото телесно тегло, могат да увредят имунитета. Диета-индуцирани затлъстели животни, с променени имунологични параметри, като лимфопения, по-нисък митогенен отговор на далака и тенденция към понижаване на цитотоксичната активност на NK клетките [3-5]. В допълнение, затлъстелите прасета, които вече са нарушили метаболизма, показват инфилтрация на макрофаги. Тези промени са свързани с глобалното ДНК хиперметилиране както в В-клетките, така и в Т-клетките [6].
Независимо от това, хората със затлъстяване показват повишени рискови фактори за тежки инфекции и дисфункция на имунната система, които могат да влошат имунния отговор към ваксините [7]. Популацията със затлъстяване не реагира на ваксинация срещу хепатит В [8-10] и на тетаничен токсоид [11]. Освен това реакцията на противогрипните ваксини е намалена при затлъстели индивиди [12,13]. Затлъстели индивиди с по-висок брой неутрофили, моноцити, както и общ брой на левкоцитите [13] и потискана реакция на лимфоцитите към митогени [14-16].
Епигенетичните механизми, които свързват затлъстяването с рака, изглеждат многофакторни и включват взаимодействието на метаболитните и имунните фактори; фонът зад тези асоциации едва започва да се разбира. Инсулиновата резистентност е основен фактор, но има няколко други метаболитни кандидати, включително инсулиноподобни растежни фактори и фактори, освобождавани от адипоцитите, като лептин и свързани със затлъстяването маркери за възпаление, т.е. тумор некроза фактор-α и интерлевкин, ядрен фактор каппа бета (NF-κB) система и оксидативен стрес [17-19]. Затлъстяването е състояние на хронично възпаление, характеризиращо се с необичайно производство на възпалителни цитокини с локални и системни ефекти, които могат да допринесат за развитието на тумори [19]. Въпреки че локалното ограничено възпаление може да участва в инициирането на имунни отговори, прекомерното възпаление може да стимулира прогресията на тумора в стационарно състояние [20,21].
| NLRP3, NLRP1, NLRP4 или AIM 2 инфламазоми | Съдови заболявания и мозъчни нарушения |
| CCR5 лиганд и възпалителен хемокин MIP-1 | Езофагогастрален карцином |
| Повишени нива на VEGF и IL-6 по-висок дял на CD8 + Т клетки и NKT клетки | Прогресия на тумора |
| Активирани провоспалителни CD4 + и CD8 + Т клетки | Аденокарцином на хранопровода |
| NF-Kappa B критична връзка | Рак |
| Инсулинова резистентност, хиперинсулинемия, повишен IGF-1 | Рак на гърдата в постменопауза |
| Leptin STAT 3, AP-1, ERK 2 и MARK Инсулинова сигнализация | Рак на дебелото черво |
| Цитокини, ROS, клетъчен стрес | Рак |
| Адипокинезокретомерегулацията на провъзпалителните адипокини | Сърдечно-съдови заболявания |
Маса 1: Интегрираните болестни възпалителни сигнали в отговор на затлъстяването стимулират атеросклерозата и увеличават риска от рак.
Какво е имунотоксичност?
Имунната система е директно интегрирана в организма и тясно взаимодейства с функционирането на много органи и органи. Имунната функция е особено податлива на разрушаване от химикали в околната среда. Въпреки че основните промени в имунната система бързо се изразяват в значителна заболеваемост и дори смъртност на засегнатите организми, те често се предшестват от фини промени в някои от нейните компоненти, които биха могли да се използват като ранни проследяващи вещества или като биомаркери сами по себе си [29]; това е от особен интерес, тъй като тези ефекти обикновено се проявяват при нива, по-ниски от тези, причиняващи токсични реакции на имунната система [30]. Но как химичните вещества в околната среда влияят върху функцията на имунната система? Те обременяват ли ролята на затлъстяването за увеличаване на риска от рак и какъв е случаят с имунотоксичността и рака на ендометриума?
Имуномодулиращи ефекти от химикали в околната среда
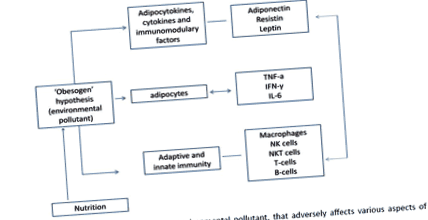
Фигура 1: Обезогенът представлява замърсител на околната среда, който влияе неблагоприятно на различни аспекти на функциите на мастната тъкан.
Епилог
Предложената връзка между органотините и диференциацията на адипоцитите отваря важна нова ера на изследване на епигенетиката на човешкото здраве по отношение на затлъстяването и възникващите заболявания като диабет или неоплазия. Следователно, допълнителни изследвания, насочени към разбиране на действието на химическите обезогени на рецепторно ниво, ще подчертаят връзката между затлъстяването и рака, независимо от дозата на експозиция, и могат също така да разкрият скрити нови механизми, регулиращи развитието на мастната тъкан. В заключение, имунната дисмодулация, упражнявана от химикалите в околната среда, може да бъде първата стъпка в многоетапната канцерогенеза.
- Изобразяване на рак на панкреаса Новата роля на ендоскопското ултразвуково изследване Insight Medical Publishing
- Съвременно медицинско управление на затлъстяването Ролята на фармацевтичната намеса - ScienceDirect
- Туберкулоза на панкреаса Общ преглед Insight Medical Publishing
- Затлъстяването поставя жените в по-висок риск от лечение на рак на ендометриума днес
- Резултат от наднормено тегло, затлъстяване и рак на ендометриума е систематичен преглед и мета-анализ