Резюме
Намаляването на силата и мускулната функция с възрастта - саркопенията - допринася за различни негативни резултати, включително повишен риск от: падания, фрактури, хоспитализация и намалена подвижност при възрастни хора. Базираните на населението оценки на загубата на мускули след 60-годишна възраст показват загуба на
1% годишно, докато загубата на сила е по-бърза при
Физическа активност и стареене
85% от хората не отговарят на указанията за физическа активност (1). Това подчертава потенциала за подобрение, който би могъл да бъде постигнат, като се има предвид потенциалът за повишена физическа активност за намаляване на риска от редица заболявания и смъртност от всички причини (2, 3). Възрастните възрастни са склонни да се занимават с по-малко физическа активност в сравнение с по-младите (4) със забележим спад в нивата на физическа активност през свободното време при по-възрастните възрастни (5-7). Интересното е, че социалната изолация при възрастните хора може да е резултат от множество фактори: невъзможност да напуснат къщата поради лоша мобилност, липса на транспорт или неблагоприятни метеорологични условия, болест на индивида или в неговите социални кръгове, като всички те подчертават сложността на способността за интервенция при възрастни възрастни.
Влошаването на ниските нива на обичайната физическа активност при възрастните възрастни са рязко и рязко намаляване на активността, водещо до по-ниски нива на механично натоварване на мускулите. Острите пристъпи на бездействие, които водят до разтоварване на мускулите, се проявяват поради различни обстоятелства (болест, нараняване, лоши метеорологични условия) и се различават отчетливо от обичайното заседнало поведение. Въпреки че тези остри смущения в дейността могат да изглеждат доброкачествени, ние предполагаме, че натрупаните пристъпи на подчертано бездействие, насложени върху физически неактивна популация, са основен риск за отрицателни физиологични здравни резултати и могат да ускорят саркопенията и развитието на хронични кардиометаболитни състояния, свързани със стареенето.
Саркопения и физическо бездействие
Цикличните пристъпи на изразено бездействие дори при относително здрави хора могат да имат значителни вредни физиологични ефекти върху здравето, особено с напредване на възрастта (8). По-конкретно, острите периоди на физическо бездействие (9–14) водят до намаляване на размера и силата на скелетните мускули, които преходно ускоряват обичайните спадове в резултат на саркопения (15). Базираните на населението оценки на саркопенията показват загуба на мускулна маса, настъпваща със скорост от
1% годишно със загуби в мускулната сила и мощ, по-бързи при темпове от
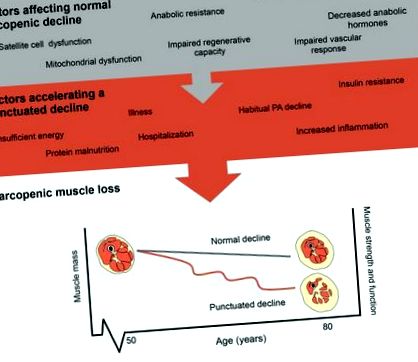
8% годишно, съответно (16, 17). Въпреки че прогресията на саркопенията се разглежда като нормална последица от стареенето, тя може да се ускори поради неактивност, която временно ускорява загубата на мускулна маса (15). Всъщност многобройни фактори могат да повлияят на прогресията на саркопеничната мускулна загуба със събития в неактивност, които допълнително ускоряват мускулната загуба, както е показано на Фигура 1. Факторите на начина на живот, като упражнения и хранене, могат да смекчат прогресията на нормалната мускулна загуба с увеличаване на възрастта. По-специално, намаляването на физическата активност, недостатъчният или излишният енергиен прием и недохранването с протеини могат да действат, за да ускорят синергично спадането на саркопенията и по този начин да увеличат риска от последваща хоспитализация или преустановяване, което води до ускорена мускулна загуба (18). Важното е, че с всяко събитие на отпадане, загубата на мускулна маса намалява и площта на напречното сечение на мускулите драстично намалява с увеличаване на интрамускулното съдържание на мазнини (19). Физическата активност е мощен регулатор на фактори, свързани със стареенето и здравето на скелетните мускули [бездействие и възпаление (14), реактивни кислородни видове, гликемичен контрол (20), загуба на двигателни неврони (21)] и когато се комбинира с правилно хранене (адекватен протеин прием) може да служи за намаляване на скоростта на мускулен спад.
Фактори, влияещи върху прогресията на саркопенията. Представяния за нормална саркопенна загуба на мускули и ускорена загуба на мускули, както е показано чрез прекъснат спад.
Намаляването на стъпките като модел на периодично бездействие
750 стъпки/г), използвани в проучвания, са в съответствие със стъпките, извършени от пациенти в остър болничен престой (34). Тревожно е, че ежедневните стъпки на пациентите в болница (от 708 изследвани дни) надвишават 300 стъпки на ден само 50% от времето; въпреки това средно дневните стъпки на пациент са били
740 (34). Намаляването на физическата активност със SR до тези ниски нива очевидно не би представлявало пълно разстройство на мускулите, но има дълбоки физиологични последици. Важно е, че SR има подобни системни ефекти върху цялото тяло, но очевидно в по-малка степен като почивката в леглото, в сравнение с едностранното обездвижване на крайниците, което до голяма степен е насочено към периферните тъкани (Фигура 3). Освен това епизодите на почивка в леглото (обикновено поради приемане в болница) може да се появят по-рядко от епизодите на неактивност, които се появяват периодично през цялото време поради метеорологични условия или заболявания като грип и вероятно засягат по-голям дял от населението, отколкото е засегнат от пълната почивка в леглото. По този начин, целта на този преглед е да подчертае физиологичните последици, произтичащи от целенасочени намалени ежедневни стъпки при по-млади и възрастни възрастни, с прозрение за скорошни проучвания, използващи SR и потенциала за упражнения и хранене за борба с атрофията в този модел.
Синтез на мускулни протеини (MPS) и разграждане на мускулни протеини (MPB) в отговор на грамове протеин на хранене. Плътните линии означават MPS, прекъснатите линии означават MPB. Сините хеширани зони показват положителен протеинов баланс, докато червените точки показват отрицателен белтъчен баланс. Сините хеширани зони и червените пунктирани области се приравняват на същата площ под кривата, показваща нетен белтъчен баланс.
Есенциалната аминокиселина левцин е мощен стимулатор на mTOR и от своя страна MPS (76) и следователно добавки с високо съдържание на левцин обикновено се използват поради техния анаболен потенциал и потенциален мускулен щадящ ефект по време на атрофия на използване. Към днешна дата обаче резултатите са несъвместими при моделите за почивка в леглото. Ferrando et al. установи, че добавките с 15 g незаменими аминокиселини (5,3 g левцин) три пъти дневно, по време на 10 дни почивка в леглото, не облекчават загубата на LBM при здрави възрастни възрастни в сравнение с контролната група (51). По подобен начин, English et al. установи, че добавките за време на хранене с дози от 4,5 g левцин само частично защитават загубата на LBM след 7 дни почивка в леглото, но не защитават значително LBM в 14 дни почивка в леглото с добавки при по-млади хора (40). Paddon-Jones et al. показа защитен ефект от 16,5 g EAA (3,1 g левцин), осигурен три пъти дневно, по време на 28 дни почивка в леглото върху общия LBM при млади възрастни (72). Като се има предвид, че липсата на съгласие относно ефикасността на аминокиселинните добавки за щаденето на LBM е както при млади, така и при възрастни възрастни по време на почивка в леглото, са необходими много повече изследвания, за да се определи окончателно дали наистина има полза от EAA и добавките с левцин по време на почивка в леглото.
Интересното е, че енергийният баланс изглежда играе съществена роля за загубата на LBM по време на почивка в леглото. Както може да се очаква, консумацията на хипокалорична диета води до ускорена скорост на загуба на LBM по време на почивка в леглото, главно чрез потискане на MPS (42). Всъщност, Biolo et al. показа, че 14 дни почивка в леглото в комбинация с 20% калориен дефицит водят до по-голямо разхищение на LBM в сравнение със същите участници, консумиращи евкалорична диета в кръстосано проучване (68). В последващо проучване обаче Biolo et al. също така изследва ефектите на положителния енергиен баланс по време на почивка в леглото в сравнение с отрицателния енергиен баланс. Тези автори установяват, че по време на 35 дни почивка в леглото, участниците в положителен енергиен баланс са загубили 1,5 кг повече LBM, отколкото участниците в отрицателен енергиен баланс, констатация, която авторите приписват на активиране на възпалителни пътища, свързани с увеличаването на мастната маса, придружаваща положително енергийно балансирано състояние. По този начин, в допълнение към хранителните добавки, трябва да се обмисли насърчаването на поддържането на енергийния баланс по време на периоди на отказ за оптимално хранене, за да се смекчи загубата на скелетна мускулатура.
По-малко изследвания са изследвали ефектите от хранителни интервенции по време на имобилизиране на единични крайници при хора. Две проучвания са изследвали ефектите от добавянето на креатин със смесени резултати. Hespel и сътр. изследва ефектите от ежедневната добавка с 20 g креатин монохидрат или плацебо контрол за 2 седмици едностранно обездвижване на долните крайници (коляното) при млади възрастни. Тези автори установяват значителна загуба при CSA на четириглавия мускул без разлика между допълнителните групи (77). Обратно, Johnston et al. осигури на млади възрастни участници както плацебо контрол, така и впоследствие 20 g креатин по време на 7 дни имобилизация на горния крайник (лакътна става) в кръстосано проучване и креатинът поддържа по-добре чиста тъканна маса в сравнение с плацебо, като същевременно поддържа разнообразие от функционални параметри (78). Въпреки че има много разлики между двете гореспоменати проучвания (време на обездвижване, измерване на мускулна маса), разликата в имобилизирания крайник (носене на тежест спрямо неносещо тегло) затруднява сравнението между двете проучвания и по този начин ефекта на креатина добавките за задържане на LBM с обездвижване изискват допълнителни изследвания.
Добавянето на протеини и аминокиселини не е широко изследвано в литературата, за да компенсира загубата на мускулна маса по време на обездвижване. Dirks et al. показаха, че след 5 дни литационна имобилизация, квадрицепсният CSA е намален с 1,5% в контролите и с 2% при здрави възрастни мъже, консумиращи плацебо или два пъти дневно 20,7 g протеинова добавка, съответно (12). Интересното е, че участниците в това проучване са получили протеинова добавка, която може да е била под оптималните прагове [0,4 g/kg/доза (79)], тъй като въз основа на средната маса може да е по-ефективна доза протеин, близка до 30 g, за намаляване на загубата на ЛБМ с гласово обездвижване на коляното (79).
Наскоро McGlory et al. изследва ефекта на добавките с рибено масло върху задържането на LBM по време на едностранно укрепване на коляното в продължение на две седмици при млади здрави жени. Участниците бяха снабдени с дневна доза от 5 g n-3 мастни киселини или контролно масло (слънчогледово масло) в продължение на 28 дни преди 14-дневно едностранно обездвижване на коляното. След обездвижване, добавянето с n-3 мастни киселини отслабва намаляването на обема на мускулите на квадрицепса с 6% (съответно 14 срещу 8% в контролната група спрямо добавките) и също така насърчава повишаване на MPS над скоростите на контролната група при всички измерени точки от времето (70). По този начин добавянето на добавки с n-3 мастни киселини в допълнение към адекватна доза протеин и енергиен баланс може да послужи за намаляване на спада в LBM по време на едностранно обездвижване на крайниците и почивка в леглото.
Към днешна дата нито едно проучване не е изследвало ефекта от диетичните манипулации върху SR чрез добавки или промени в енергийния прием. Като се има предвид, че протеинът, по-специално висококачественият протеин (с високо съдържание на EAA) в големи количества има мощен анаболен ефект върху по-старите скелетни мускули, наскоро имахме за цел да проучим ефектите от високо протеинова диета за смекчаване на загубата на скелетна мускулатура и намаляването на MPS при здрави възрастни възрастни по време на SR. За да повторим обстоятелствата, свързани с период на SR при възрастни възрастни (т.е. хоспитализация), участниците са били снабдени с високо съдържание на протеин (1,6 g/kg/ден) чрез добавяне или с 60 g дневна доза суроватъчен протеин или колагенови пептиди, и диета с ограничена енергия (-500 kcal, в допълнение към намаляването на енергийния прием, отчетено от SR) по време на 2-седмичен SR период. Добавянето с суроватъчен протеин или изонитрогенно количество хидролизирана колагенова пептидна добавка позволява сравнението на добавките с високо и ниско качество, високо протеин върху LBM промени с SR (14). След само едноседмично ограничаване на енергията няма значителни загуби в LBM, но има значително намаление на MPS от
16% и в двете групи [констатации, подобни на предишни разследвания в SR (20)]. Интересното е, че с ограничаване на енергията и SR не е имало допълнителни намаления на MPS, което показва потенциален защитен механизъм, чрез който здравите възрастни възрастни могат да смекчат адитивните катаболни стимули. Въпреки това, след едноседмично възстановяване, което включваше връщане към нормалните ежедневни стъпки, по време на което участниците поддържаха добавки, суроватъчният протеин се оказа по-добър в стимулиращите скорости на MPS над периода SR, без ефект на добавяне на колаген пептид (14). Липсата на възстановяване на скоростта на MPS в групата, допълнена с колаген, след връщане към нормалната активност е подобна на предишните констатации от нашата лаборатория, в която участниците възобновяват консумацията на обичайните си диети след SR (20). Тези данни подчертават обещаващото наблюдение, че висококачествените протеинови добавки могат да служат за подобряване на здравето на скелетните мускули във връзка с увеличаване на физическата активност при възрастни възрастни след възстановяване, резултати, които биха могли да бъдат допълнително подобрени, когато се комбинират със структурирано обучение за упражнения за устойчивост.
Заключение
Принос на автора
ТАКА подготви оригиналния проект на ръкописа. SO, TH и SP допринесоха за редактирането и подготовката на окончателния ръкопис.
Изявление за конфликт на интереси
SP декларира, че е получил конкурентно безвъзмездно финансиране, хонорари и пътни разходи от Националния съвет за млечни продукти в САЩ и от млекопроизводителите на Канада. Останалите автори декларират, че изследването е проведено при липса на каквито и да било търговски или финансови отношения, които биха могли да се тълкуват като потенциален конфликт на интереси.
Благодарности
SO беше подкрепена от стипендия за висше образование в Онтарио. SP се подпомага от безвъзмездни средства от Канадските институти за здравни изследвания, Националния съвет за научни и инженерни изследвания, Институтът за изследване на остаряването Макмастър и програмата на канадските изследователски столове и благодари на тези източници на финансиране.
- Тези грешки при упражнения и диети убиват усилията ви за отслабване - Stormont Vail Health
- Отслабване Упражнение за отслабване Колко калории можете да изгорите с скачащо въже Здраве
- Тези грешки в протеиновите барове може да саботират усилията ви за отслабване Жени; s Здраве
- Ефектът на пеперудата Въздействието на щитовидната жлеза върху вашето здраве от Марина Тарасова Забележително -
- Подходящото момиче; s Ръководство за протеинови мускули; Фитнес