Резюме
клинично признатите форми на индуцирана от стреса репродуктивна дисфункция включват функционална хипоталамусна аменорея (FHA), анорексия, нервна булимия и свързана с упражнения аменорея. Приблизителната причина за тези форми на репродуктивен компромис е функционално и теоретично обратимо намаляване на централното шофиране към репродуктивната ос, осигурено от хипоталамусния невроендокринен хормон гонадотропин-освобождаващ хормон (GnRH). Наличието на клинични форми на стрес-индуцирана репродуктивна дисфункция повишава риска от други заболявания, включително сърдечно-съдови заболявания, остеопороза, депресия и други психиатрични състояния, както и безплодие (1, 15, 20, 28). Излагането на стрес по време на бременност също може да има отрицателно въздействие върху развитието на плода. Потенциалните фетални последици включват преждевременно раждане, лошо невроразвитие и нарушено психосоциално развитие (26, 31, 35).
Въз основа на тези наблюдения тествахме хипотезата, че комбинация от метаболитни и психосоциални стресори ще действа синергично, за да причини по-голямо увреждане на репродуктивната функция, отколкото би се случило, ако даден индивид изпитва единични стресори. За да проверим тази хипотеза, извършихме проучване, използвайки женски маймуни cynomolgus (Macaca fascicularis), които показват месечни менструални цикли без сезонни вариации, подобно на жените. Моделирахме нашите парадигми на стреса на леките нива на психосоциален стрес и хранителните и упражняващи навици, докладвани от жени с FHA (5, 17, 25).
Животни.
За този експеримент са използвани двадесет и седем възрастни женски маймуни cynomolgus с тегло 2,72–5,26 kg. Маймуните били настанени в изследователската лаборатория за примати на университета в Питсбърг в отделни клетки. Светлините бяха включени от 0700 до 1900; температурата се поддържа на 24 ± 2 ° C. Животните бяха хранени с еднократно дневно хранене при 1100 (~ 300 kcal, № 5045 чау; Ralston-Purina, Сейнт Луис, Мисури) и една четвърт парче пресни плодове (~ 25 kcal) следобед. Те също така получиха нови артикули, като играчки или некалорични храни, приблизително два пъти седмично като част от програма за психологическо обогатяване в съответствие с насоките на Министерството на земеделието на САЩ. Водата се предлагаше ad libitum. Приемът на храна се записва ежедневно. Експериментите бяха разгледани и одобрени от институционалния комитет за грижи и употреба на животните към университета в Питсбърг.
Експериментален протокол.
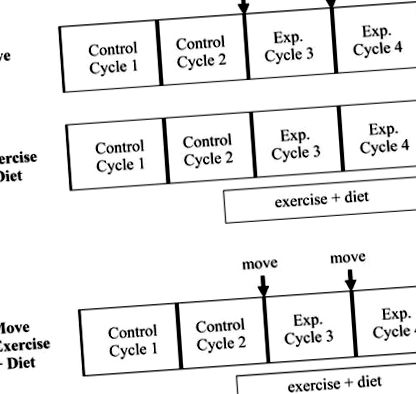
Фиг. 1.Схематична схема на експерименталния дизайн. Всички експериментални групи бяха изследвани за 2 менструални цикъла преди започване на експериментални интервенции [Control (C) 1 и C2] и след това за 2 менструални цикъла, по време на които бяха приложени специфични интервенции (E3 и E4).
Вземане на кръвна проба.
Кръвни проби за серумен LH, FSH, естрадиол (Е2) и прогестерон (Р4) се събират от будни животни през ден, преди тренировка, по време на цялото проучване, както е описано по-рано (38). Пробите се оставят да се съсирят при стайна температура в продължение на 1 час, охлаждат се в продължение на 2 часа и след това се центрофугират при 2500 об/мин за 10 минути. След това серумът се съхранява при -20 ° C в стъклени флакони, докато се извършат анализи. На всеки 6 седмици на животните се дава интрамускулно инжектиране на железен декстран от 0,5 cm 3, за да се поддържа нормален хематокрит. По време на всяко вземане на кръвна проба се претеглят маймуни.
Мониторинг на репродуктивната функция.
Всички животни преди това са били свикнали с ежедневни проверки за менструация, т.е.измиване на вагиналната област с апликатор с памучен връх. По време на проучването, ден 1 от цикъла се счита за първия ден на менструацията. Всяка маймуна е била наблюдавана преди проучването, докато е имала поне три нормални менструални цикъла. Цикълът се счита за нормален, ако е овулаторен, с дължина 25–44 дни и показва изблици на Е2, LH и FSH в средата на цикъла и лутеално покачване на P4> 1 ng/ml. Въпреки че средната продължителност на цикъла на маймуните в това проучване е била 30 ± 0,8 дни, една маймуна постоянно показва овулаторни цикли, които са били с продължителност 44 дни в продължение на няколко месеца преди проучването. Тази маймуна поддържа дълги цикли през цялото проучване и следователно е включена в анализите. Ановулаторните цикли се определят като цикли, които започват с наблюдавани менструации, но не показват нормални овулаторни модели на репродуктивните хормони. За целите на това проучване дефинирахме анормални цикли като тези, които са ановулаторни или цикли с продължителност извън 25–44 дни, независимо дали са овулаторни или не.
Обучение за упражнения.
Животните бяха обучени да бягат на стандартни бягащи пътеки за човешка употреба (Precor, Bothell, WA), използвайки предварително публикувани техники (38). Скоростта и продължителността се увеличават индивидуално, докато животните бягат 1 час/ден със скорост 3,2–4,8 km/h. Индуцираното от тренировки повишаване на кардиореспираторната годност е документирано, като маймуните попълват максимално класифициран тест за упражнения през първите 2 седмици от обучението си и след това отново в края на проучването. Използването на максимално оценен тест за упражнения за оценка на кардиореспираторната годност е добре документирано при хората (41). Протоколът за изпитване на упражненията започва с ниска скорост (1,3 км/ч) и след това се увеличава с 0,32 км/ч на всеки 2 минути след това, докато маймуната прояви признаци на умора (т.е. бягане в задната част на кутията от плексиглас). Промените в нивото на фитнес се определят от промяната в максималната скорост, постигната по време на максимално класирания тест за упражнения от предварителното обучение до посттренинга. Тренировъчните скорости за ежедневни пристъпи на упражнения са изчислени индивидуално при 80% от най-високата скорост, постигната по време на предварителния тренировъчен тест за максимално класифицирано упражнение. Известно е, че както сърдечната честота, така и кортизолът се увеличават значително при хора, трениращи с тази интензивност (16, 41).
Парадигма на психосоциалния стрес.
Формата на психосоциалния стрес, използвана в това проучване, се състоеше в преместването на животните в нова стая, където те бяха настанени в отделни клетки, заобиколени от непознати маймуни. Предишна работа в тази лаборатория показа, че тази форма на стрес води до повишаване на сърдечната честота и нивата на кортизол и може да бъде свързана с нарушаване на нормалната менструална цикличност при малък процент маймуни (32). Експерименталните условия по време на E3 и E4 в групата Move варираха само по отношение на стаята, в която бяха настанени маймуни.
Анализи на хормони.
Концентрациите на серум E2, P4, FSH и LH бяха измерени чрез радиоимуноанализ (RIA) от основната лаборатория на RIA към Центъра за изследвания в репродуктивната физиология към Университета в Питсбърг, използвайки описаните по-рано методи (39). Чувствителността на тестовете за Е2 варира от 2,20 до 3,88 pg/ml (8,08 до 14,2 nmol/l), а коефициентите на вариация на интра- и интра-теста за вариациите на Е2 са съответно 6,1 и 7,7%. Чувствителността на тестовете за Р4 варира от 0,05 до 0,14 ng/ml (0,16 до 0,44 nmol/l), а коефициентите на вариация на интра- и интра-теста за P4 анализите са съответно 5,0 и 6,4%. Чувствителността на тестовете за FSH варира от 1,2 до 3,7 ng/ml (1,2–3,7 IU/l), а коефициентите на вариация на интра- и интра-теста за тестовете на FSH са съответно 6,8 и 8,0%. В хода на това проучване LH беше изследван с помощта на две различни RIAs, с пречистена маймуна LH или рекомбинантна маймуна LH като стандарт (2, 39). Коефициентите на преобразуване за подходящия диапазон на стандартната крива бяха използвани за преобразуване на всички данни, събрани с помощта на втория анализ, в стойности в първия анализ. Чувствителността на тестовете за LH варира от 7,4 до 12,2 ng/ml (7,4–12,2 IU/l), а коефициентите на вариация на интра- и интра-теста за LH анализите са съответно 7,2 и 9,0%.
Анализ на данни.
Преди анализ всички данни бяха проверени за нормалност. За нормално разпределени данни промените във времето бяха анализирани с помощта на дисперсионен анализ с повтарящи се мерки (ANOVA). Базовите сравнения бяха извършени с помощта на еднопосочен ANOVA. Последващото тестване използва теста с най-малко значими квадрати. Ако предположенията за нормалност са били нарушени, са били извършени непараметрични тестове, подходящи за повтарящи се мерки, т.е., тестът на Wilcoxon с ранг. За непараметрични сравнения между групите на изходно ниво е използван тестът на Крускал-Уолис, последван от Ман-Уитни U-тест, за да се определи къде са възникнали ефекти. За данни, сравняващи пропорциите на необичайни цикли между групите, бяха използвани χ2 анализа. За тези анализи аномалия в единия или двата цикъла по време на експерименталната фаза (E3 или E4) се отчита като единична аномалия, когато се комбинират E3 и E4 (E3 + 4). За всички анализи, P ≤ 0,05 се счита за значимо. Всички анализи бяха извършени с помощта на SPSS v. 13.0 (SPSS, Чикаго, IL). Всички данни се отчитат като средни стойности ± SE.
Стресорите за упражнения и диета, използвани в това проучване, доведоха до умерено повишаване на сърдечно-съдовата форма, както се очакваше с прилагането на фитнес тренировки на ниско ниво. При трениращите животни максималните скорости, постигнати по време на теста за упражнения, не се различават между групите на изходно ниво и се увеличават по подобен начин (19–29%) с обучение [F(2,10) = 32,5, P = 0,001], т.е. от 5,8 ± 0,99 до 7,2 ± 0,12 км/ч в групата Упражнение + Диета и от 4,8 ± 1,49 до 6,2 ± 1,77 км/ч в групата Преместване + Упражнение + Диета. Дневните тренировъчни дистанции на отделни маймуни варират от 3,1 до 5,7 км/ден по време на E3 + 4 за двете групи, които тренират, и няма значителна разлика в дневното ниво на упражнения между тези две групи по всяко време. Обучението се увеличи значително от C1 + 2 до E3 + 4 и в двете упражняващи групи [F(1,15) = 531,8, P
Фиг. 2.Промени в телесното тегло (Горна част), изминати километри на ден (средна) и дневен прием на калории (отдолу) в хода на експеримента за всяка експериментална група. а P
Фиг. 3.A: процент на маймуните, показващи ненормални менструални цикли (т.е. или цикли с продължителност> 44 дни, или ановулаторни цикли) в E3 + 4 за всяка от 3-те експериментални групи. * Значителна разлика във времето при сравняване на E3 + 4 с C1 + 2 (Z. = -2.449, P = 0,014) и значителна разлика между групите при сравняване на E3 + 4 (Преместване + Упражнение + Диета спрямо Движение и Упражнение + Диета, χ = 9,613, P = 0,025). Б.: продължителност на менструалния цикъл (Горна част), дължина на фоликуларната фаза (средна) и дължина на лутеалната фаза (отдолу) в хода на експеримента за всяка експериментална група. значителна разлика в групата от C1 + 2 (P b Значителна разлика между групите (Преместване + Упражнение + Диета спрямо двете останали групи, P
маса 1. Промени в репродуктивните хормони с интервенции Move, Exercise + Diet и Move + Exercise + Diet
Стойностите са средства SE. С1 + 2, контролни групи 1 и 2; E3 + 4, експерименти 3 и 4.
* ANOVA значителен времеви ефект; F(1,21) = 12.01, P = 0,002; значим групов ефект F(2,21) = 4,23, P = 0,028; post hoc тестове, Преместване срещу Преместване + Упражнение + Диета (P = 0,014).
† ANOVA значителен времеви ефект; F(1,21) = 6,91, P = 0,016. † ANOVA значителен времеви ефект; F(1,21) = 9,41, P = 0,045; значим групов ефект F(2,21) = 5,97, P = 0,008; post hoc тестове, Упражнение + Диета срещу Движение + Упражнение + Диета (P = 0,002).
§ ANOVA значителен времеви ефект; F(1,23) = 7,03, P = 0,014. Забележка: за да конвертирате естрадиол pg/ml в nmol/l, умножете по 3.671; за превръщане на прогестерон ng/ml в nmol/l, умножете по 3,18; за да конвертирате LH и FSH ng/ml в IU/l, умножете по 1.0.
Нашите открития показват, че излагането на ниско ниво на стресови фактори, които са често срещани в ежедневието на човека (включително лек психосоциален стрес, леко диетично ограничение и умерено упражнение), когато се изпитва самостоятелно, нарушава репродуктивната функция при сравнително малко индивиди (∼10% от населението ). Въпреки това, комбинации от същите тези ниски стресови фактори (напр. Комбиниран психосоциален плюс метаболитен стрес) се синергизират, за да компрометират репродуктивната функция при неочаквано голям процент (~ 70%) от индивидите. В няколко случая прекъсването е драматично, причинявайки продължителен (> 100 дни) период на аменорея само след един експериментален цикъл. Тези резултати осигуряват ясни доказателства, че стресорите на ниско ниво, които сами по себе си имат малко влияние върху физиологичната активност на репродуктивната ос, синергизират, за да компрометират значително нормалната репродуктивна функция при голям процент индивиди, когато се появят едновременно.
Нашето проучване включва излагане на множество стресови фактори за сравнително кратък период от време, т.е. два менструални цикъла, и следователно не е известно дали наблюдаваните ефекти ще се влошат при продължително излагане на стресовите фактори или може би ще бъдат обърнати или подобрени, ако хората се настанят в стресовите фактори . В нашето проучване се виждат някои признаци за приспособяване към стресовите фактори. Две от пет маймуни, които са имали необичайни цикли в Е3, са имали нормални цикли в Е4, може би показващи някакво приспособяване към стреса. И двете маймуни, които показаха необичайно дълги цикли по време на E3 и E4, претърпяха намаляване на продължителността на цикъла от E3 на E4. Ясно е, че са необходими бъдещи проучвания, които изследват въздействието на тези стресови фактори за по-дълги периоди от време, за да се определи дали се случва приспособяване и да се определи основният механизъм за такава адаптация.
Нашето откритие, че стресорите с ниско ниво проявяват синергични ефекти върху репродуктивната ос, наскоро беше използвано за насочване на развитието на поведенческа интервенция за жени с FHA (6). Ние разсъждавахме, че ако комбинираният метаболитен и психосоциален стрес причинява FHA, тогава едновременното справяне както с психосоциалните, така и с метаболитните стресори ще бъде необходимо, за да се обърне FHA. Първоначалното ни проучване, включващо когнитивна поведенческа терапия и консумация на малки, чести ястия, подкрепя тази интерпретация (6). Като алтернатива, бихме могли да заключим от нашите резултати, че единичните стресори са по-малко склонни да влошат репродуктивната функция, отколкото комбинираните стресори; по този начин всяко лечение, което ефективно премахва поне един стрес, ще бъде полезно при лечението на FHA. Въпреки това изглежда разумно да се лекува възможно най-много стресори, които биха могли да допринесат за репродуктивна дисфункция при жени, търсещи лечение на безплодие. В по-широк смисъл, способността на стресорите на ниско ниво да действат синергично предполага, че стресорите на ниско ниво, които често се пренебрегват при получаване на клинична анамнеза или при определяне на план за лечение, могат да окажат значително влияние върху редица процеси, свързани със стреса.
Това проучване беше подкрепено от Националните здравни институти U54-HD-18185, MH-50748, HD-25929 и RR-00163.
СТЪПКИ
Разходите за публикуване на тази статия бяха покрити отчасти чрез плащането на такси за страница. Следователно статията трябва да бъде маркирана с „реклама”В съответствие с 18 U.S.C. Раздел 1734 единствено, за да посочи този факт.
Благодарни сме за съдействието на техническия персонал, включително Сали Кун, Доун Мърфи, Синди Хайлман и Лиза Бенч. Също така благодарим на Кристен Маккормик за помощта при статистически анализи и подготовка на ръкописа. Ресурсите и помощта на персонала на ядрените лаборатории на приматите и RIA на Центъра за изследвания в репродуктивната физиология към Университета в Питсбърг също са високо оценени.
- Здравето на майката и хранителните навици метаболитни последици и въздействие върху здравето на детето - ScienceDirect
- Положителните метаболитни ефекти на избрани пробиотични бактерии върху индуцирано затлъстяване при мишки са
- Масивно затлъстяване, лекувано с периодично гладуване Метаболитно и клинично проучване - ScienceDirect
- Свинско срещу говеждо - Сравнение на въздействието върху здравето и храненето
- Обективна оценка на хранителните модели чрез използване на метаболитен фенотип на рандомизиран, контролиран,