Судхаа Шарма
Катедра по акушерство и гинекология, Суперспециалистична болница, GMC, Джаму, Джаму и Кашмир, Индия
Vishal R. Tandon
1 Катедра по фармакология, Суперспециалистична болница, GMC, Джаму, Джаму и Кашмир, Индия
Шагун Махаджан
2 Нефрологично отделение, Суперспециалистична болница GMC, Джаму, Джаму и Кашмир, Индия
Вивек Махаджан
1 Катедра по фармакология, Суперспециалистична болница, GMC, Джаму, Джаму и Кашмир, Индия
Анил Махаджан
3 Катедра по обща медицина, Държавен медицински колеж, Джаму, Джаму и Кашмир, Индия
Резюме
Остеопорозата и затлъстяването са здравословни проблеми в световен мащаб. Интересното е, че и двете са свързани със значителна заболеваемост и смъртност. И двете заболявания имат обща връзка, тъй като мезенхимните стромални клетки на костния мозък са общите предшественици както за остеобластите, така и за адипоцитите. Стареенето може да промени състава на костния мозък чрез увеличаване на адипоцитите, активността на остеокластите и намаляването на остеобластната активност, което води до остеопороза. Адипоцитите секретират лептин, адипонектин, адипсин, както и провъзпалителни цитокини, които допринасят за патогенезата на остеопорозата. Тази нова концепция подкрепя хипотезата, че положителната корелация на теглото и индекса на телесна маса (ИТМ) с костната минерална плътност (КМП) не се потвърждава от големи проучвания, базирани на популация. По този начин предишната концепция, че затлъстяването е защитно за остеопороза, може да не е същото като отлагането на мазнини в костния мозък (адипогенеза), наблюдавано при затлъстяването, е вредно за здравето на костите.
ВЪВЕДЕНИЕ
Остеопорозата и затлъстяването са здравословни проблеми в световен мащаб, свързани със значителна заболеваемост и смъртност, както се предполага, че и двете са резултат от нарушена регулация на обща прекурсорна клетка, т.е. мезенхимни стромални клетки на костния мозък. [1]
Продължаващият дебат относно предишната концепция, че затлъстяването е защитно за остеопорозата, може да не стои по същия начин с оглед на новата концепция за затлъстяване на костите (адипогенеза), което се счита за вредно за здравето на костите. Тази нова концепция се появи в резултат на факта, че теглото и индексът на телесна маса (ИТМ) имат положителна корелация с костната минерална плътност (КМП), [2,3], но големи проучвания на базата на популация не потвърждават и потвърждават такава положителна корелация между костната маса и ИТМ. [4,5]
Основните фактори, разглеждани в миналото за затлъстяването като защитен фактор за остеопороза, включват повишено натоварване на кортикалния скелет, директно стимулиране на образуването на кост от лептин, по-голяма активност на ароматазата, повишена естрадиол, водеща до намаляване на костната резорбция и стимулиране на костната формация. [6]
Въпреки това, последните данни показват, че детското затлъстяване е свързано с повишен риск от фрактури на долните крайници, въпреки увеличаването на КМП. [7] Друго проучване [8] предполага, че затлъстяването е свързано с по-висока КМП, но защитният му ефект върху риска от фрактури е противоречив. По-високите абсолютни стойности на BMD, кортикалната и трабекуларната архитектура и индексите на силата не са пропорционални на излишъка на BMI при жени със затлъстяване в постменопауза. Затлъстяването е свързано с намален риск от клинични фрактури на гръбначния стълб, тазобедрената става, таза и китката/предмишницата, но повишен риск от множество фрактури на ребрата в сравнение с нормалното население или с по-ниско тегло. [9] Резултатите от изследването показват, че много, ако не и повечето остеопоротични фрактури се наблюдават при жени с наднормено тегло или затлъстяване, допълнително опровергават, че затлъстяването е защитно.
КАК ЗАТЪЛВАНЕТО НА КОСТИТЕ ОБЯСНИ ТЕЗИ ПРОТИВОПОЛОЖЕНИЯ
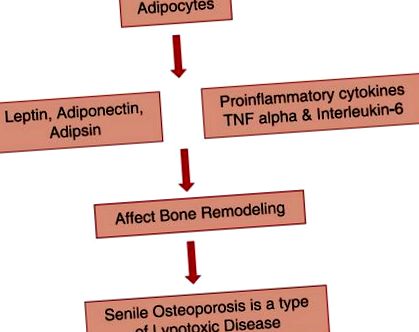
Мезенхимните стромални клетки на костния мозък са често срещаните предшественици както на остеобластите, така и на адипоцитите. Стареенето може да промени състава на костния мозък чрез увеличаване на адипоцитите, активността на остеокластите и намаляването на активността на остеобластите, което води до остеопороза. [1] Факторите, секретирани от адипоцитите, за които е известно, че оказват влияние върху ремоделирането на костите, са лептин, адипонектин и адипсин, както и провъзпалителни цитокини, като фактор на туморна некроза и интерлевкин-6. [6] Следователно адипогенезата на костния мозък изглежда оказва липотоксичен ефект върху остеобласта. Ролята на лептин, адипонектин и адипсин в упражняването на липотоксичен ефект върху костите е обяснена по-долу [Фигура 1].
Показване на ролята на лептин, адипонектин и адипсин в остеопорозата
Доказано е, че лептинът и инсулиновият растежен фактор-1 имат положителни периферни роли в запазването на костната маса по време на постменопаузата. [10] Повече от този серумен лептин е показан като полезен индикатор за риск от остеопороза, свързан с диета, индуцирано затлъстяване. [11] Неотдавнашните данни обаче предполагат, че лептинът контролира образуването на кост чрез хипоталамусно реле, като по този начин се предполага, че централният механизъм също трябва да участва в действието му върху костите. Доказано е, че дефицитът на адренергични рецептори (т.е. без бета) повишава телесното тегло и мастната маса и показва по-голяма обща телесна костна маса, трабекуларен костен обем и размер на напречното сечение на бедрената кост. [12,13] По този начин, което показва, че целостта на симпатиковата сигнализация е необходима за увеличаване на костната резорбция. Което ще означава, че състоянието с дефицит на катехоламин може да има висока костна маса и приложените симпатомиметици могат да намалят костната форма и костната маса. И обратно, бета-блокерите е вероятно да увеличат образуването на кости и костната маса и да притъпят костната загуба, предизвикана от състояние на дефицит на естроген. По този начин лептинът действа подобно на естрогена.
Доказано е, че адипонектинът увеличава образуването на остеокласти и влияе негативно на остеопорозата. Това действие се медиира чрез стимулиране на производството на рецепторен активатор на рецепторен активатор на ядрен фактор капа-В лиганд (RANKL), който стимулира диференциацията на остеокластите. Освен това, адипонектинът може да инхибира производството на остеопротегерин, известен инхибитор на остеокластогенезата, в остеобластите. Въпреки това, нивото му при слаб човек се вижда по-високо, а при по-дебелия човек е от долната страна. По този начин се предполага, че ниските нива на адипонектин при затлъстяване могат да осигурят остеопротекция. [14]
Въпреки това се появиха противоречиви доказателства в полза на адипонектин, отричащ остеопротективния ефект сред затлъстелите лица, от неотдавнашно проучване, при което уникален адипокин, освободен от адипоцити, е показан антиапоптотичен, противовъзпалителен и антиоксидативен. В едно от изследванията се съобщава, че човешките остеобласти експресират адипонектин и неговите рецептори и е показано, че увеличават костната маса чрез потискане на остеокластогенезата и чрез активиране на остеобластогенезата. [15]
Подобно е показано, че адипсин влияе отрицателно на остеопорозата, особено захарният диабет (DM) предизвиква остеопороза. Повишена експресия се наблюдава при пациенти със СД и затлъстяване и е доказано, че намалява образуването на кости. [16]
Други: Освен тези фактори, някои други важни фактори са предложени при генезиса на остеопороза при затлъстяване, т.е. затлъстяването и недостатъчността на витамин D намаляват бионаличността на витамин D3, тъй като в някои проучвания се съобщава, че телесните мазнини в дългосрочен план могат да повлияят негативно с остеопороза. Този фактор става много важен, тъй като вече има голямо разпространение на дефицит на витамин D. [17]
КЛИНИЧНО И ДИАГНОСТИЧНО ОТРАЖЕНИЕ НА КОНЦЕПЦИЯТА - ЗАТЪЛВАНЕ НА КОСТИТЕ
Грешките при определяне на КМП, често наблюдавани при лица със затлъстяване, се дължат на отлагане на мазнини в костния мозък. Двуенергийните рентгенови абсорбциометрични измервания могат да бъдат фалшиво повишени от повишените телесни мазнини; като има предвид, че измерванията на трабекуларна КМП чрез количествена компютърна томография могат да бъдат намалени с по-голяма мастна тъкан в мозъка [6]
Неуспех в растежа, пубертетен арест, водещ до намалена крайна височина на възрастен, и пикова костна маса е обичайното обяснение за лошото здраве на костите при синдрома на Кушинг. [18] Докато инсулиновата резистентност и хипергликемията се считат за причини за вредните ефекти върху функцията на остеобластите при пациенти с DM. [19] По подобен начин е известно, че глюкокортикоидите променят клетъчния състав на костите чрез регулиране на снабдяването и продължителността на живота на остеокластите и остеобластите. [20] Обездвижването, допринасящо за остеопорозата, както при паркинсонизма, се счита за резултат от намалена мускулна сила. [21]
Всички вторични причини за остеопороза, като синдрома на Кушинг, DM, глюкокортикоиди и обездвижване, са свързани със затлъстяването. В миналото беше трудно с предшестващата хипотеза, че затлъстяването е защитно за остеопорозата, да се обясни причината за остеопорозата в такива случаи. Това обаче вече може да бъде обяснено въз основа на свързаното с това увеличаване на затлъстяването на костния мозък, наблюдавано в такива случаи. [6] По същия начин, в екстремни условия на живот, пубертет и старост, инфилтрацията на мазнини в костния мозък може да бъде вредна за здравината на скелета и може да повлияе отрицателно на оптималната функция на костната ремоделираща единица. [6]
ОТРАЖЕНИЕ НА ЛЕЧЕНИЕТО НА ТАЗИ КОНЦЕПЦИЯ
Последиците от лечението ще бъдат огромни. Настоящите възможности за лечение на остеопороза, известни предимно, са или антиостеокластогенеза, или про-остеобластогенеза в природата. Наскоро обаче е доказано, че витамин D действа чрез инхибиране на адипогенезата на костния мозък като допълнителен механизъм покрай известните му действия върху костите. [22] По-нататъшни проучвания в тази посока демонстрират дозозависими ефекти на 1,25 (OH) 2 D3 върху трансдиференциацията на мускулните клетки в мастните клетки. Ниските физиологични концентрации (имитиращи дефицитно състояние) предизвикват адипогенеза; като има предвид, че по-високите (физиологични и супрафизиологични) концентрации смекчават този ефект. [23] Освен това има доказателства, че витамин D влияе върху телесната мастна маса чрез инхибиране на адипогенните транскрипционни фактори и натрупването на липиди по време на диференциацията на адипоцитите. Някои скорошни проучвания показват, че метаболитите на витамин D също влияят върху производството на адипокин и възпалителния отговор в мастната тъкан. [24]
По подобен начин алендронат, широко използван бисфосфонат напоследък се съобщава, че стимулира остеобластичната диференциация, като същевременно инхибира адипогенезата in vitro; като по този начин се предполага анаболен ефект върху костите чрез диференциация на мезенхимни стволови клетки. [25]
В миналото е доказано също, че паратиреоидният хормон (PTH) индуцира диференциация на остеобластите, инхибира адипогенезата и потиска апоптозата на остеобластите. [26] По подобен начин е доказано, че свързаният с паратиреоиден хормон протеин (1-36) (PTHrP (1-36)) предизвиква лек остеогенен ефект и инхибира адипоцитния ефект в човешките мезенхимни стволови клетки и по този начин помага при остеопороза, освен познатото му действие за модулиране на костната форма чрез насърчаване на диференциацията на остеобластите. [27]
Стронциевият ранелат има антирезорбтивно и анаболно действие върху костите. Наскоро обаче беше показано, че адипогенезата се влияе отрицателно в присъствието на стронциев ранелат със съпътстващо дозозависимо намаляване на експресията на адипогенни маркери и промени в адипокиновия профил, като по този начин генерира благоприятен остеогенен ефект в средата на костния мозък. 28]
По същия начин в друго текущо проучване е доказано, че диетичните смеси от изофлавони и техните метаболити, лигнани и техните метаболити, куместрол и смес, съдържаща всички тях, инхибират зависимо от концентрацията диференциация на адипоцитите като техен допълнителен механизъм на действие за предотвратяване на остеопороза. 29]
ЗАКЛЮЧЕНИЕ
Предишната концепция, че затлъстяването е защитно за остеопороза, може да не стои по същия начин и се появи нова концепция за отлагане на мазнини в костния мозък, наблюдавано при затлъстяване, подкрепяща вредния ефект на затлъстяването за здравето на костите. По този начин затлъстяването може да не се счита за защитно за остеопороза. Освен това, изследването на връзката между костите и мазнините на молекулярно и клетъчно ниво вероятно ще доведе до по-добро разбиране на няколко рискови фактора и основите на патогенезата и до разработването на лекарства с двоен механизъм за остеопороза и затлъстяване в бъдеще.
Бележки под линия
Източник на подкрепа: Нил
Конфликт на интереси: Никой не е деклариран.
- Не е годен за борба Как затлъстяването заплашва американската армия
- Метаболитни; Затлъстяване; Отдел по ендокринология; Медицински колеж; Университет на Флорида
- Метаболитно здравословно затлъстяване и риск от намаляване на бъбречната функция - Чанг - 2018 - Затлъстяване - Wiley
- Свързано с пролактинома затлъстяване, лекувано с бупропион и метилфенидат
- Прогресивен характер на затлъстяването и диабета при нечовешки примати - Hansen - 2017 - Затлъстяване - Wiley