Резюме
Нестабилността на повтарящи се последователности на ДНК в генома е свързана с редица човешки заболявания. Разширяването на тринуклеотидни повторения се признава като основна причина за неврологични и нервно-мускулни заболявания и напредъкът в разбирането на мутациите през последните 20 години е значителен. Тук предоставяме кратко резюме на напредъка с акцент върху техническия напредък на различни етапи.
1. Въведение
Нестабилното и динамично предаване на прости повтарящи се елементи в ДНК е нов тип мутация, която е променила лицето на генетиката [1]. Мутацията, наричана „разширяване на тринуклеотидно повторение (TNR)“, възниква, когато броят на триплетите, присъстващи в мутирал ген, е по-голям от броя, открит в нормален ген [1–3]. Освен това броят на тризнаците в гена на болестта продължава да нараства, тъй като генът на болестта се наследява (фиг. 1а). Тъй като броят на TNR нараства, нарастващият триплет тракт променя генната експресия и/или функцията на генния продукт; TNR, пребиваващи в кодираща последователност на ген, обикновено произвеждат дефектен протеин, докато разширяването на TNR в некодиращ генен регион потиска експресията на протеина, променя неговото снаждане или може да повлияе на аспекти на антисенс регулацията (фиг. 1б) [1–3] . Например, при болестта на Хънтингтън (HD), незасегнатите индивиди могат да имат приблизително 6–29 тройки CAG и в двата алела; все пак, при пациенти с HD, алелът на болестта може да съдържа от 36 до стотици CAG тризнаци. Тъй като броят на повторенията на TNR нараства, нарастващият полиглутаминов тракт произвежда HD генен продукт (наречен huntintin) с все по-отклоняващи се свойства, който причинява смърт на мозъчните клетки, контролиращи движението [1–3].
Нарушения на разширяването на тринуклеотидни повторения, причинени от триплетните повторения в кодиращи и некодиращи генни области. (а) Наследяването на гени на болести и предаването от родител на дете води до бързо разширяване на регионите, които се повтарят. (б) Триплетните повторения, пребиваващи в кодиращи и некодиращи последователности на ген, оказват значително влияние върху човешкото здраве и са в основата на много тежки неврологични разстройства
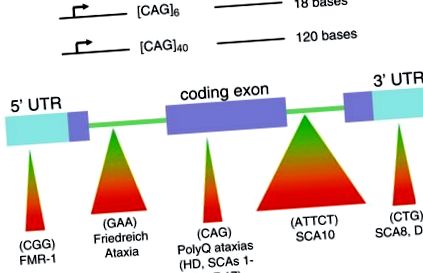
Патофизиология на тринуклеотидни нарушения при повтаряне и ефект от броя на повторенията. Засегнатите области на мозъка и областите на невронална загуба при неврологични разстройства, свързани с разширяване на TNR, са показани вляво. Червените региони показват основните засегнати области и зоните на невронална загуба. При HD пациентите с 36–120 повторения на CAG са засегнати от заболяването и показват невронална загуба в области на мозъка, които контролират движението. Схематичните изображения на засегнатите гени са показани вляво. Повтарящите се области във всеки ген са обозначени с малката лента в кодиращата област на гена. Обърнатият триъгълник представлява нарастващ брой повторения. Основата на триъгълника представлява незасегнати индивиди; пунктирани линии показват незасегнати носители на болести, а червената част на триъгълника показва засегнати индивиди. C/P опашка/путамен, CTX кора, GP globus pallidus, STN субталамично ядро, VL вентролатерално таламусно ядро, SN substantia nigra
Напредъкът в разбирането на експанзионните болести на всяка стъпка от процеса на откриване разчита на разработването на нови методи и подходи. В първото издание на тринуклеотидни протоколи за повторение [12] бяха подчертани методи за генериране на трансгенни животни и клетъчни модели за заболяване, както и методи за количествено определяне на продължителността на триплетните повторения в клетки, хора и при животни. Второто издание на тринуклеотидни повторни протоколи надгражда и разширява тези теми, като включва по-сложни методи за откриване на TNR, нови животински модели за количествено определяне на експанзията и нови експериментални подходи, които се отнасят както до патогенезата на TNR болестта, така и до терапевтичните средства.
2 Ранно клинично откриване на TNR и историческа перспектива
Ефекти от разширяването на CAG в гена на huntintin. Представително родословие от две поколения на HD семейство. Квадратите са мъже; кръгове са жени. Червените кутии показват засегнатите лица. Отворените кръгове са несвързани съпрузи. Черните цифри представляват повторение на CAG във всеки алел на засегнатите членове на семейството. Малки черни букви показват алелите, присъстващи в предаването от баща на син. Числото в скоби представлява размера на разширението на CAG по време на наследяването. Връзката между HD и CAG повторен номер (вляво). В това схематично представяне на HD гена, отворената лента представлява кодиращата област на гена на Хънтингтън (наречен huntintin); малката червена лента показва позицията на повторението на CAG повторение, разположено в N-терминалната част на кодиращата последователност. Обърнатият триъгълник представлява все по-голям брой повторения на CAG. Основата на триъгълника представлява незасегнати индивиди с 6–26 повторения на CAG; линиите показват незасегнати носители на заболяването с 27–35 повторения на CAG; а горната част на триъгълника показва засегнати индивиди с 36–120 повторения на CAG
Ефект от повторното число върху възрастта на началото и очакването. (а) Възрастта на настъпване е обратно свързана с броя на повторенията. Увеличаването на повторенията на CAG в гена на HD болестта намалява възрастта на поява на симптомите на заболяването. Симптомите на ранно начало/младежки HD могат да се наблюдават при повторни числа над 60. (б) Фенотип на предвиждане в семейство от три поколения, показващ повишената тежест при следващи поколения. Дядо (вляво), симптоми на миотония от 50-годишна възраст, но без значително увреждане. Майка (средна), миотония от късните тийнейджърски години. Син (вдясно), вродена миотонична дистрофия
3 генетични модификатори на заболяването: соматично разширяване и хроматин
Способността да се свърже клиничната възраст на появата с точната дължина на тринуклеотидния тракт разкри на бял свят втората ключова характеристика на експанзионната болест (фиг. 4); началото е силно променливо [2, 19–21]. Например при HD наследствената продължителност на повторението може да предскаже средната възраст на началото (Фиг. 4), но началото при отделен пациент с дадена продължителност на повторение може да варира до четири пъти (начало от 18 до 80-годишна възраст) от прогнозираната средна стойност (фиг. 4). Високата степен на вариабилност предполага съществуването на генетични модификатори и ловът на тези фактори е привлякъл значително внимание [25–29]. Към днешна дата обаче най-важният модификатор, повлияващ началото на заболяването, изглежда е променливостта на самата дължина на CAG тракта [30, 31].
През последното десетилетие са измерени соматични вариации в броя на повторните копия при повечето триплетни заболявания на човека [32–39] и в повечето модели на мишки за триплетни заболявания, включително FXS [40, 41], DM-1 [42, 43], SCA1 [44] и HD [45–48], наред с много други. Но дали соматичните вариации в продължителността на повтаряне влияят ли на началото на заболяването? В много случаи соматичните разширения са сравними по размер с тези, които се наследяват. Например в HD патофизиологията е толкова зависима от размера на наследствения повтор, че нарастването с еднократно повторение на CAG може да намали възрастта на настъпване на засегнатия пациент с 5 години. В стриатума, най-уязвимата област на мозъка, се наблюдават хетерогенни и видни експанзии до хиляди [30, 32]. По този начин някои от повторните разширения на CAG в мозъка на HD далеч надхвърлят тези, които се наследяват. По логичен начин, тогава, соматичният растеж на повторението в човешките мозъчни клетки би могъл да причини по-тежък фенотип на заболяването с възрастта, тъй като болестните протеини от по-дългите полиглутаминови пътища се произвеждат постепенно. При животните соматичното разширяване на CAG тракта продължава постепенно през целия живот на животните, тъй като те развиват токсични фенотипове.
Дали соматичната експанзия влияе върху началото на заболяването е трудно да се определи стриктно при хората, тъй като мозъкът им не може да бъде оценен до смъртта. Независимо от това, скорошни доказателства в човешкия мозък след смъртта на HD предполагат, че соматичната дължина на повторение е от значение [48]. Соматичната нестабилност в мозъчната зона на мозъка от кохорта от индивиди с HD показва фенотипни крайности на началото на млади и стари болести, както се прогнозира от дължината на референтен алел, измерен в малкия мозък [48]. След отчитане на референтната продължителност на повторението, по-голямата дължина на повторението се увеличава, свързана с по-ранно начало на заболяването. Много променливи трябва да бъдат сортирани, преди да се направят твърди заключения. Хората се различават по отношение на диетата, начина на живот и начина, по който се справят със стреса. Освен това, ефектите от наследственото повторение и соматичните алели върху началото на заболяването не могат да бъдат ясно разделени в мозъците след смъртта. Данните за хората обаче са в съответствие с хипотезата, че соматичните разширявания на дължина на повторната дължина на CAG в целевите тъкани допринасят за патогенния процес на HD.
Далеч по-малко е известно по отношение на втори генетичен модификатор, ефектите от опаковането на хроматин върху нестабилността на триплетните повторения [49]. Разширяването трябва да действа в контекста на хроматина и нараства интересът към изследването как структурата на хроматина и епигенетичните модификации влияят върху разширяването [49]. Например, изследване на човешкия локус Ataxin-7 при трансгенни мишки установи връзка между свързването на CCCTC свързващ фактор (CTCF, регулаторен протеин, замесен в ДНК конформация и геномно импринтиране) и регулиране на повтарящата се нестабилност [50]. Мутация на CCCTC последователността в Ataxin-7 локуса, CTCF свързващо място до разширена повторна последователност, подобрена нестабилност [50]. Понастоящем връзките между епигенетичните промени и разширяване остават загадъчни, но влиянието на локуса на генома, посттранслационната модификация на хистоните и метилирането на ДНК върху разширяването на TNR ще бъдат ключови въпроси за изследване.
4 Генетичният механизъм на разширяване
Свързването на продължителността и динамиката на мутацията на триплетните повторения лежи в основата на нарушенията на триплетните повторения и интересът към генетичните механизми за разширяване експлодира едновременно с откриването на гените на болестта. Структурните и молекулярни анализи между 1995 и 2005 г. бяха ключови за затвърждаване на хипотезата, че стабилните вторични структури са междинните продукти на разширяването [2, 3, 49]. Честотата на разширение зависи от структурообразуващите последователности и се увеличава с дължината на трактовете CGG [51], CAG [52], CTG [53] и GAA [54]. Визуализирането на структура на фиби in vivo не е възможно при настоящите граници на разделителната способност. Моделът обаче е съобразен с повечето генетични данни и структурообразуващите хетеродуплексни бримки, съдържащи триплетни повторения, са огнеупорни за възстановяване по време на мейоза в дрождите, докато други повторения и произволни последователности са отстранени [55].
5 Протеинова и РНК-медиирана токсичност на триплетните разстройства при повторно разширяване
6 Терапевтични средства
Усилията за скрининг за съединения, които намаляват протеинозависимата токсичност и окислителното увреждане на ДНК, са интензивни, но все още не са се получили терапевтични средства, които ефективно компенсират началото на заболяването [81–83]. Въпреки че търсенето на малки молекули продължава, новите терапевтични стратегии за повтаряне на триплетната болест са напреднали на три фронта: ДНК, РНК и протеин. Ако соматичната експанзия е фактор за началото и прогресирането на заболяването, блокирането на соматичната експанзия трябва да бъде от полза. По този начин терапевтичните подходи за намаляване на експанзията са предизвикали голям интерес, въпреки че все още не са идентифицирани ефективни молекулярни инхибитори на експанзията на ДНК. Протеините за възстановяване на ДНК насърчават разширяването и инхибирането им е възможна стратегия за регулиране на продължителността на повторение на триплета. Въпреки това, възстановяването на ДНК играе съществена роля за избягване на мутации на други места. По този начин предизвикателство в това усилие ще бъде да се идентифицират молекули, които инхибират разширяването, без да променят нормалното ниво на възстановяване на ДНК.
Може би най-бързо развиващите се технологии в триплетната област са терапевтичните средства, насочени към аберантни протеинови продукти или РНК, използващи siRNA [84, 85]. siRNA „нокдаун“ на мутантния белтък на ловджитин показва, че заглушаването на мутантния HD трансген инхибира значително невродегенерацията, подобрява моторния контрол и удължава оцеляването на HD мишки [86, 87]. Продуктът на нормалния ген е необходим за оцеляването и развитието на клетките. Следователно, основно предизвикателство при всеки siRNA подход е да инхибира експресията на мутантния ген, като същевременно позволява експресия на неговия нормален аналог. С бъдещото подобряване на селективността на мутантните алели (запазване на експресията на невропротективния алел от див тип), целевата специфичност, ефикасност и безопасност, както и оптимизиране на методите за доставка, ефикасността на малки некодиращи терапевтични приложения, базирани на РНК, вероятно ще се подобри [88].
Допълнителните стратегии срещу РНК-индуцирана токсичност включват използването на антисенс РНК. CAG повторните антисенс олигонуклеотиди са ефективни при DM1 модели чрез промяна на протеиновите взаимодействия или метаболизма на токсичната РНК [89]. CAG повторните антисмислени олигонуклеотиди са проектирани да се свързват с CUG повторната РНК и да блокират токсичните РНК-протеинови взаимодействия. Освобождаването на разширените CUG транскрипти от ядрени огнища вероятно улеснява транспортирането им до цитоплазмата, където те претърпяват бързо разпадане. Като допълнителна полза, соматичната нестабилност на CTG повторения в DMPK гена се потиска след лечение с антисенс олигонуклеотиди [89]. Тези резултати повишават възможността ранната интервенция с антисенс олигонуклеотиди да намали РНК или протеиновата токсичност и може да има допълнителната полза от стабилизиране на CTG: CAG се повтаря при субпатогенни дължини.
С появата на индуцируеми плурипотентни стволови клетки (iPS), заместващата терапия със стволови клетки е обещаващ път [90, 91]. Стволовите клетки са получени от фетална тъкан, но имат потенциал да се развият в нормални мозъчни клетки, ако се имплантират хирургически в мозъка [92], и се изследват хирургични стратегии за трансплантация на стволови клетки за заместване на загубени неврони в мозъка [90–92] . Индукцията на плурипотентни стволови клетки (iPS) чрез добавяне на транскрипционен фактор „коктейли“ се тества за директно препрограмиране на човешки соматични клетки за заместителна терапия [93, 94]. По този начин, iPS клетките дават надежда, че тежестта на патофизиологията може да бъде намалена или нейното начало да бъде забавено чрез заместване на умиращите неврони с възобновяеми клетки. Тези процедури са експериментални и все още не е ясно дали ще бъдат ефективни. Въпреки това, ембрионалните присадки са подобрили двигателните функции както при животните, така и при хората [90, 93–95].
7 Заключения
Нашето разбиране за патогенните механизми за тринуклеотидно повторение (TNR) се разшири значително през последните години. Докато много аспекти на токсичността и мутационните механизми остават загадъчни, новите модели за ДНК, РНК и протеини осигуряват нарастваща способност да инхибират спада при тези смъртоносни заболявания. Въпреки че все още не е налице ефективна терапия, надеждата за намеса е на хоризонта.
Благодарности
Бих искал да благодаря на Christie A. Canaria, Virginia Platt (NIH/NIA T32-AG00266), Do Yup Lee, Nelson Chan, Ella Xun, James Lim и подкрепата на Националните институти за здравни помощи NS069177, NS40738, NS062384 и NS060115.