Бруно П. Чумпитази
катедра по педиатрия, Медицински колеж Baylor, Хюстън, Тексас, САЩ
b Секция по детска гастроентерология, хепатология и хранене, Детска болница в Тексас, Хюстън, Тексас, САЩ
Робърт Дж. Шулман
катедра по педиатрия, Медицински колеж Baylor, Хюстън, Тексас, САЩ
b Секция по детска гастроентерология, хепатология и хранене, Детска болница в Тексас, Хюстън, Тексас, САЩ
c Детски изследователски център за хранене, Хюстън, Тексас, САЩ
Резюме
Въведение
Функционалните стомашно-чревни разстройства, свързани с детската коремна болка (AP-FGID), засягат до 20% от децата по света и представляват поне 5% от всички посещения на педиатрични кабинети в САЩ [1, 2]. Тези нарушения нямат идентифицируема органична етиология, основана на конвенционални диагностични тестове; въпреки това децата с AP-FGID имат както понижено качество на живот, така и увеличени отсъствия от училище в сравнение с връстниците си [3]. Стомашно-чревните (GI) симптоми (напр. Коремна болка), свързани с тези нарушения, могат да продължат с години и до зряла възраст [4]. Успешните интервенции, които подобряват тези симптоми при AP-FGID в детска възраст, могат да окажат влияние и в зряла възраст [4]. За съжаление, въпреки нарастващия интерес и изследвания, настоящите конвенционални клинични интервенции за тези разстройства често са неефективни.
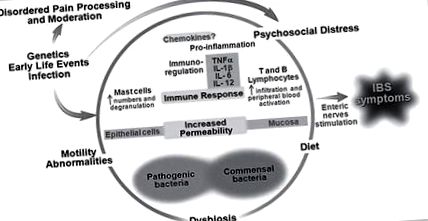
Въпреки че по-рано са дефинирани в широката категория на повтарящи се коремни болки (RAP), използвайки критерии Рим III, AP-FGIDs сега са класифицирани в: синдром на раздразненото черво (IBS), функционална диспепсия, функционална коремна болка и коремна мигрена [5]. Счита се, че етиологията на AP-FGID е многофакторна и най-добре се подхожда с помощта на биопсихосоциалния модел (фиг. 1). Потенциалните фактори включват: психосоциален дистрес (напр. Соматизация, безпокойство); промени в състава и функцията на чревния микробиом; нискостепенно възпаление на червата; повишена пропускливост на червата; висцерална свръхчувствителност; променена двигателна функция на стомашно-чревния тракт и диета. Диетата в частност предизвика интерес като виновник, като се има предвид, че децата с AP-FGIDs често свързват симптомите с приема на определени храни [6].
Биопсихосоциален модел на FGID. Променено от Rodriguez-Fandino et al. [45] с разрешение от Journal of Neurogastroenterology and Motility.
Въглехидратите осигуряват по-голямата част от калориите, консумирани в западната диета [7]. В продължение на много десетилетия отделни въглехидрати (например лактоза) са замесени както като виновници за етиологията на симптомите, така и като потенциални терапевтични агенти (например фибри) при деца с AP-FGID. Този преглед ще разгледа предложената патофизиология на непоносимостта към въглехидрати и настоящите доказателства, които влияят върху отделните въглехидрати и групи от въглехидрати при причиняване или подобряване на симптомите при AP-FGID в детска възраст. Той също така ще разгледа накратко предложената храносмилателна физиология на фибрите и настоящите доказателства, сочещи към използването на фибри при деца с AP-FGID.
Непоносимост към въглехидрати
Предложени общи патофизиологични механизми
При деца с AP-FGIDs, няколко отделни въглехидрати (включително лактоза и фруктоза) са замесени като обострящи GI симптомите [8, 9]. Като група тези отделни въглехидрати в комбинация с фруктани, галактани и полиоли се наричат ферментиращи олигозахариди, дизахариди, монозахариди и полиоли (FODMAP) въглехидрати (таблица 1). Въглехидратите FODMAP бързо се ферментират от бактерии на дебелото черво и са осмотично активни (фиг. 2). Тези физиологични ефекти могат да причинят раздуване на дебелото черво от приток на вода в лумена и могат да доведат до симптоми на коремна болка, плоскост, подуване на корема и разхлабени и/или по-чести изпражнения. Тези неимунологични нежелани реакции към въглехидратите се наричат въглехидратна непоносимост.
Предложен патофизиологичен механизъм на малабсорбираните въглехидрати при FGID. Променено от Barrett et al. [46] с разрешение от Практическа гастроентерология.
маса 1
Списък на въглехидратите и примери за храни, които ги съдържат в групата FODMAP
| Фруктоза | Монозахарид | Определени плодове: ябълки, круши; пчелен мед; сокове |
| Лактоза | Дисахарид | Млечни продукти: краве мляко, сирене |
| Фруктани | Фруктозни полимери | Пшеница, лук, ръж |
| Галактани | Галактозни полимери | Фасул, бобови растения, аспержи |
| Полиоли | Захарни алкохоли | Някои плодове и зеленчуци: кайсии, череши, круши |
Въпреки че са групирани заедно като FODMAP въглехидрати, всеки отделен малабсорбиран въглехидрат може да има различен физиологичен ефект. Оценката на магнитен резонанс при здрави възрастни показва, че фруктозата значително увеличава съдържанието на вода в тънките черва; фруктаните обаче увеличават съдържанието на вода в тънките черва в много по-малка степен [10]. За сравнение, при здрави възрастни, фруктаните значително разширяват лумена на дебелото черво; фруктозата обаче увеличава раздуването на дебелото черво в много по-малка степен [10]. Индивидуалните ефекти на лактозата, галактаните и полиолите върху GI физиологичната функция, измерена чрез ядрено-магнитен резонанс, остават да бъдат изяснени. Освен това, дали същите тези физиологични промени настъпват след поглъщане на въглехидрати FODMAP при деца (или възрастни) с AP-FGIDs, не е известно.
Допълнителни фактори, които могат да играят роля при генерирането на симптоми при пациенти с непоносимост към лактоза, включват нискостепенно възпаление на червата и висцерална свръхчувствителност [11]. Това беше показано от Yang et al. [11] при възрастни с IBS след предизвикване на лактоза и издишване на водородни тестове за идентифициране на лактозни малабсорбери (повишено производство на водород след предизвикване на лактоза). Тези с IBS, които са имали лактозна малабсорбция, са категоризирани в една от двете групи: лактозна малабсорбция с непоносимост към лактоза (съпътстващо увеличаване на симптомите на стомашно-чревния тракт с лактозната провокация) и лактозна малабсорбция без лактозна непоносимост (без увеличаване на симптомите на стомашно-чревния тракт). Yang et al. [11] установи, че възрастни с IBS с лактозна малабсорбция и непоносимост (в сравнение с тези само с малабсорбция) имат както увеличени мастоцити при илеоколонични биопсии, така и повишена висцерална свръхчувствителност. Понастоящем не е известно дали тези фактори играят роля и при непоносимостта към въглехидрати при AP-FGID в детска възраст.
Лактоза
Хипократ за първи път описва непоносимост към лактоза около 400 години пр. Н. Е., Но клиничните симптоми са признати едва през последните 50 години [12]. Лактозата е дизахарид (две съединени захари), който е уникален с това, че присъства само в млякото на бозайници с приблизителни оценки 5,5–8,0 g/100 ml в кърмата и 4,5–5,0 g/100 ml в кравето мляко [13]. За да се използва, лактозата трябва да се разгради (хидролизира) от ензима лактаза. Лактазата се намира по върховете на вилисите на тънките черва и разгражда лактозата до два монозахарида - галактоза и глюкоза. След това тези монозахариди се абсорбират от тънките черва и се метаболизират.
По време на раждането при хората активността на лактазата е в своя пик. Лактазната активност обаче започва да намалява в ранното детство при приблизително 70% от хората; до зряла възраст активността на лактазата е много ниска или неоткриваема [14, 15]. Приблизително 30% от популацията има персистенция на лактаза, при което активността на лактазата остава извън отбиването и до зряла възраст [14, 15]. Устойчивостта на лактазата се среща предимно при хора от северноевропейски произход.
Количеството лактоза, необходимо за предизвикване на симптоми при човек с непоносимост към лактоза, варира в зависимост от множество фактори. Те включват: (1) количеството погълната лактоза; (2) дали поглъщането е придружено от хранене или друга храна; (3) скоростта на изпразване на стомаха (колко бързо храната навлиза в тънките черва); (4) време за преминаване през тънките черва (времето, необходимо на храненето да влезе в дебелото черво след първото навлизане в тънките черва); (5) дали храненето съдържа бактерии с ензими (бета-галактозидаза), способни да разграждат лактазата, и (6) бактериална адаптация на дебелото черво към предишната диета [16, 17]. Например, в едно проучване, единични натоварвания с лактоза от ≥ 15 g са предизвикали симптоми при повечето възрастни с дефицит на лактаза; въпреки това, натоварването с лактоза до 12 g (особено ако се разпространява през целия ден) води до минимални или никакви симптоми [18]. По същия начин, храненето на млечни кисели млека с жизнеспособни микробни култури, които съдържат бактерии с бета-галактозидазна активност, води до по-малко признаци на малабсорбция на лактоза, отколкото храненето им с пастьоризирани кисели млека с малко бета-галактозидазна активност [17]. Понастоящем количеството лактоза, необходимо за предизвикване на симптоми при дете с лактозна малабсорбция (или здраво, или с AP-FGID), е неизвестно.
Две други проучвания поддържат градиент на доза-отговор при експозиция на лактоза и симптоми. Едно проучване предизвика 13 здрави възрастни с нарушено храносмилане с лактоза с различни количества лактоза (0, 2, 6, 12 и 20 g) [16]. Това проучване установи, че дози до 6 g (представляващи 120 ml мляко) се понасят добре, но симптомите започват да се появяват при експозиция от 12 g [16]. Подобни констатации са отбелязани при възрастни, предизвикани с увеличаване на количествата лактоза в лактозно-хидролизиран млечен препарат; тежестта на симптомите зависи главно от количеството лактоза [19].
Изследвания, свързани с лактоза при деца с AP-FGID
При деца с AP-FGIDs са завършени три рандомизирани контролирани проучвания, въпреки че нито едно не е оценило контролирана диета с ограничено количество лактоза (таблица 2). Има по-голям брой наблюдателни или неконтролирани проучвания (таблица 3). Lebenthal et al. [20] използва както рандомизирано контролирано предизвикателство, така и неконтролиран компонент на лечение. По-голямата част от изпитванията използваха или предизвикателство за лактоза, за да се идентифицират тези, които са с непоносимост към лактоза, въз основа на развитието на симптоми на стомашно-чревния тракт след предизвикателството, или тест за дишане с лактозен водород за идентифициране на деца, които абсорбираха лактоза чрез демонстрация на прекомерно количество водород в определено време след поглъщане на лактоза.
Таблица 2
Проспективни рандомизирани контролирани проучвания на лактоза при деца с AP-FGID
- Функционална болка в корема Райли Детско здраве
- Функционална коремна болка при деца в Бостън Деца; s Болница
- Диетичните фибри могат да помогнат за профилактика на детското затлъстяване Dr.
- Спазми по време на бременност - какво означава болка в корема
- Хронична коремна болка и повтаряща се коремна болка - Храносмилателни разстройства - Наръчници на Merck Потребител