От отделите за сърдечна хирургия (A.Z., B.F.B.) и кардиология (A.Z., D.L.H.), Университет в Мелбърн, Остин, здравеопазване, Хайделберг и отдели по фармакология (R.E.W.) и анатомия и клетъчна биология (M.J.B.), Monash University, Clayton, Australia.
От отделите за сърдечна хирургия (A.Z., B.F.B.) и кардиология (A.Z., D.L.H.), Университет в Мелбърн, Остин, здравеопазване, Хайделберг и отдели по фармакология (R.E.W.) и анатомия и клетъчна биология (M.J.B.), Monash University, Clayton, Australia.
От отделите за сърдечна хирургия (A.Z., B.F.B.) и кардиология (A.Z., D.L.H.), Университет в Мелбърн, Остин, здравеопазване, Хайделберг и отдели по фармакология (R.E.W.) и анатомия и клетъчна биология (M.J.B.), Monash University, Clayton, Australia.
От отделите по сърдечна хирургия (A.Z., B.F.B.) и кардиология (A.Z., D.L.H.), Университет в Мелбърн, Остин Здраве, Хайделберг и отдели по фармакология (R.E.W.) и анатомия и клетъчна биология (M.J.B.), Monash University, Clayton, Australia.
От отделите за сърдечна хирургия (A.Z., B.F.B.) и кардиология (A.Z., D.L.H.), Университет в Мелбърн, Остин, здравеопазване, Хайделберг и отдели по фармакология (R.E.W.) и анатомия и клетъчна биология (M.J.B.), Monash University, Clayton, Australia.
Преглеждате най-новата версия на тази статия. Предишни версии:
Резюме
Обективен- Високият плазмен холестерол или хомоцистеин е рисков фактор за атеросклероза. Холестеролът и метионинът, предшественикът на хомоцистеин, рядко се консумират отделно. По този начин целите на това проучване бяха да се определи образуването на неоинтима, аортната реактивност и факторите, участващи в ендотелната функция при зайци, хранени с висок хранителен холестерол, метионин или комбинация от двете в продължение на 12 седмици.
Методи и резултати— Заешките диетични групи бяха рандомизирани в следното: контрол (Con), 0,5% холестерол (Chol), 1% метионин (Meth) и 1% метионин + 0,5% холестерол (MethChol). Аортната реактивност се изследва чрез изометрични техники на опън, аортният обемен анализ се определя чрез стереологични техники, а имунохистохимията се използва за локализиране на ендотелни и индуцируеми NO синтази, супероксиддисмутаза, макрофаги и нитротирозин. Атеросклерозата присъства в групите Chol и MethChol. Зависимата от ендотел релаксация на практика беше премахната в групата на MethChol в сравнение с контрола. Такова намаляване на релаксацията не може да се дължи на дефект на съдови гладкомускулни клетки или на намаляване на съдържанието на ендотелна NO синтаза или супероксиддисмутаза. В групите Chol и MetChol присъстват макрофаги и индуцируема имунореактивност на NO синтаза.
Заключения— Комбинацията от висок хранителен холестерол плюс метионин на практика премахва ендотелиозависимата релаксация, подчертавайки значението на множество рискови фактори за развитието на сърдечно-съдови заболявания.
Високият плазмен холестерол 1 или хомоцистеин 2 са рискови фактори за сърдечно-съдови заболявания. Те могат да бъдат причинени от генетични дефекти в метаболизма на холестерола или хомоцистеина или чрез диетични режими. Холестеролът и метионинът, предшественикът на хомоцистеин, рядко се поглъщат отделно, тъй като животинските продукти като яйца, месо и мляко съдържат както холестерол, така и метионин. В действителност се изчислява, че 30% от населението в Съединените щати може да има високи плазмени нива на хомоцистеин 2 и повече от 50% имат високи плазмени нива на холестерол. По този начин е вероятно да има хора с високи плазмени нива и на двата рискови фактора.
В настоящото проучване тествахме хипотезата, че комбинацията от висок диетичен холестерол и метионин ще изостри развитието на атеросклероза и ендотелна дисфункция в сравнение с всеки един от агентите сам. За тази цел се използва стереологичен подход за количествено определяне на обема на интимата и средата в рамките на определено анатомично място на коремната аорта. Този подход се използва, за да се избегнат грешки в вземането на проби, дължащи се на нехомогенността на плаката. Освен това бяха изследвани ендотелните и гладкомускулните функции на клетките, заедно с имунохистохимичната локализация на ендотелната NO синтаза (eNOS), iNOS, нитротирозин, SOD и макрофаги в аортни пръстени, взети от зайци, лекувани или с контролна диета, с висок хранителен холестерол, метионин или комбинация от двете.
Методи
Животни
Мъжките новозеландски бели зайци на 3-месечна възраст са закупени от Animal Services, Monash University, Gippsland Campus, Виктория, Австралия и са разпределени на случаен принцип в 4 групи и са хранени със съответната им диета в продължение на 12 седмици (n = 8/група). Група 1 (контрола) е хранена с нормална диета от заешки чау; група 2 (Chol) е получавала нормална диета от заешки чау, допълнена с 0,5% холестерол; група 3 (Meth) е получила нормална диета от заешки чау, допълнена с 1% метионин; и група 4 (MethChol) получават нормална диета от заешки чау, допълнена с 1% метионин + 0,5% холестерол. Животните бяха настанени в отделни клетки и се поддържаха при постоянна температура от около 21 ° C. Храната и водата се доставяха по желание. Експериментите са одобрени от Университета Монаш, Департамент по Анатомична комисия по етика и са проведени съгласно Националния съвет за здравни и медицински изследвания Австралийски кодекс за грижа и използване на животните за научни цели (6-то издание, 1997).
За информация относно вземането на проби и анализ на кръвта, събирането на тъкани, количественото определяне на плаката, изследванията на функционалната реактивност, имунохистохимията и анализа на данните, моля, вижте онлайн добавката на адрес http://atvb.ahajournals.org.
Резултати
Плазмени нива на холестерол и хомоцистеин
Общите плазмени нива на хомоцистеин, холестерол, холестерол/HDL и нивата на триглицеридите са показани в таблицата. Хиперхолестеролемията присъства в групите Chol и MethChol, докато хиперхомоцистинемията е налице само в групата Meth. Интересното е, че комбинацията от холестерол плюс метионин не увеличава значително нивата на плазмен хомоцистеин в сравнение с контрола.
Стойности на общия плазмен хомоцистеин, общия плазмен холестерол, триглицеридите и общия холестерол/HDL
Тежести на тялото
Моля, вижте онлайн добавката за данни.
Обеми на атеросклероза, интима и медия
Секции на коремна аорта от групите Chol и MethChol показват голямо количество плака в сравнение с контролните групи и групите Meth. Групата Meth не показва образуване на плаки през целия изследван участък на коремната аорта; обаче, удебеляването на интимата е преобладаващо в целия съд (Фигура 1). Общият обем на интимата е значително увеличен в групата на холестерола (7,54 ± 1,00 mm 3, P 3) и допълнително се увеличава в комбинираната група (8,42 ± 1,99 mm 3, P 3) нито между групите Chol и MethChol. Обемът на средата на коремните аортни секции не показва значителна разлика между групите, въпреки че изглежда е имало увеличение на обемите на среда на Chol (13,71 ± 1,23 mm 3) и MethChol групи (11,06 ± 0,92 mm 3) в сравнение с контрола (7,56 ± 1,06 mm 3) и Meth групи (9,03 ± 1,07 mm 3). 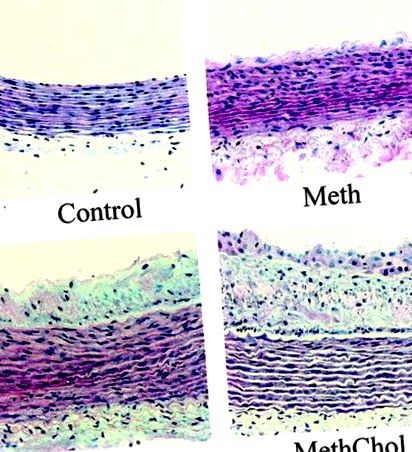
Фигура 1. Представително напречно сечение, оцветено с H&E през коремната аорта на контролните, Meth, Chol и MethChol групи. Обърнете внимание на наличието на атеросклероза в групите Chol и MethChol, пролиферация на интимата в групата Meth и липсата на патология в контролната група (× 200).
Съотношение Intima към Media
Съотношението интима и среда при животните, хранени с висок хранителен холестерол, е значително увеличено в сравнение с контрола (съответно 0,54 ± 0,05 срещу 0,18 ± 0,02), P
Фигура 2. A, Ефект от диетата за контрол (n = 5), висок диетичен холестерол (n = 5), метионин (n = 5) или комбинация от двете (n = 5) върху релаксация, зависима от ендотел до ацетилхолин. Данните са изразени като процентна релаксация на предконтракцията, предизвикана от фенилефрин. Обърнете внимание на почти пълното елиминиране на ендотел-зависимата релаксация в групата MethChol. Нивото на преконтракция с фенилефрин е показано в хистограмите над графиките. Вижте онлайн таблица I за статистическа значимост. B, Ефект от контролната диета (n = 4), висок диетичен холестерол (n = 5), метионин (n = 5) или комбинация от двете (n = 5) върху независима от ендотел релаксация до натриев нитропрусид. Данните са изразени като процентна релаксация на предконтракцията, предизвикана от фенилефрин. Обърнете внимание на значителното увеличение на максималното отпускане на SNP в групата на MethChol в сравнение с контрола. Нивото на преконтракция с фенилефрин е показано в хистограмите над графиките. Вижте таблицата за статистическа значимост. C, Ефект от контролната диета (n = 5), висок хранителен холестерол (n = 5), метионин (n = 5) или комбинация от двете (n = 5) върху аортната контракция с фенилефрин. Данните са изразени като процентно свиване на KPSS (P
Независима от ендотел релаксация
Независимата от ендотел аортна релаксация беше оценена чрез конструиране на крива на реакция на концентрация към натриев нитропрусид на донора на NO (Фигура 2В). Стойностите на -logEC50 показват, че чувствителността на гладките мускулни клетки към вазодилататора натриев нитропрусид не е повлияна от нито едно от леченията, въпреки че има тенденция за повишена чувствителност и максимални отговори в групата на MethChol в сравнение с контрола. Всички −logEC50 и максималните отговори са показани в онлайн таблица I.
Контрактилна функция
За да се определи дали диетичните режими повлияват чувствителността на гладкомускулните клетки към вазоконстриктори, аортната контракция се оценява чрез изграждане на крива на реакция на концентрация към агониста на α1-адренергичния рецептор фенилефрин. Всички -logEC50 и максималните отговори са показани в онлайн таблица I. Максималните контракции на фенилефрин не се различават значително между групите, въпреки че фенилефринът е по-малко чувствителен както в групите Meth, така и в MethChol в сравнение с контрола, което показва паралелни десни отмествания на CR кривите към фенилефрин в тези групи (Фигура 2C). По този начин тези резултати показват, че има намаляване на чувствителността на гладките мускулни клетки към вазоконстрикторния фенилефрин.
За информация относно имунолокализацията на eNOS, iNOS, SOD, нитротирозин и макрофаги, моля, вижте онлайн добавката за данни.
Дискусия
Основните констатации на настоящото проучване са, че комбинацията от висок диетичен холестерол плюс метионин на практика премахва ендотелиозависимата релаксация, което не се дължи на намаляване на протеина eNOS или протеина SOD и че комбинацията от висок хранителен холестерол плюс метионин не допълнително влошават нивото на атеросклероза в сравнение с всяка отделна хранителна добавка.
В това проучване храненето с висок хранителен прием на метионин в продължение на 12 седмици не е довело до образуване на атеросклероза в коремната аорта; обаче интимно удебеляване е изразено по целия съд, което може да показва ранните патологични промени в атеросклеротичната каскада. Тези резултати са в съответствие с предишно проучване на Toborek et al., Където удебеляването на интимата на аортата е единствената патологична промяна при 8 от 10 зайци, хранени с 0,5% метионинова диета в продължение на 6 или 9 месеца, докато атеросклероза е налице при другите 2 зайци учил.
Вазоконстрикцията към ацетилхолин, наблюдавана в коремната аорта на зайците, хранени с комбинацията от висок диетичен холестерол плюс метионин, е подобна на вазоконстрикцията, описана в артериите от хора с коронарна артериална болест. 8 Например, в разследване на Ludmer et al., 8 вазоконстрикция, а не вазорелаксация, се предизвиква от ацетилхолин във всички изследвани човешки атеросклеротични коронарни артерии. Тези проучвания показват, че пълна ендотелна дисфункция може да се появи и при хора.
Малко вероятно е обаче намаляването на зависимата от ендотел релаксация, наблюдавано в коремната аорта на животни, хранени с висок хранителен холестерол или метионин, да се дължи на намаляване на протеина eNOS или ензима SOD. В това проучване високите нива на eNOS протеин са очевидни имунохистохимично през ендотелния слой на коремната аорта и в двата региона, свободни от плака и тези, усложнени с плака, включително доказателства за eNOS в самата плака. Интересното е, че eNOS изглежда изобилен в заешкия модел на атеросклероза 24, но намалява в човешки съдове с атеросклероза 25 и в човешки ендотелни клетки, инкубирани с окислен LDL. 26 Причината за наблюдаваното несъответствие между eNOS имунореактивността в тези проучвания при хора и тези, описани в заек, остава неясна. Това може да се отнася до разликите във времевия ход на заболяването. Възможно е eNOS да присъства в ранните стадии на заболяването, но в дългосрочен план (много десетилетия живот при човека) нивата на eNOS могат да намалят.
В допълнение, няма доказателства, които да показват, че намаляването на ендотелната функция, наблюдавано в експерименталните групи, се дължи на намаляване на ензима SOD, тъй като имунореактивността на SOD е интензивна в целия ендотелен слой и в плаките на коремната аорта, което също е съобщени преди това от други. 27 Интересното е, че се предполага, че ензимът SOD в плаките може да е неактивен 28; други проучвания обаче показват увеличение на аортната активност на СОД след висок хранителен холестерол 29 или метионин. 30 Нещо повече, Miller et al 31 не успяха да подобрят релаксацията, зависима от аортния ендотел при хиперлипидемични зайци, когато нивата на ендотелния O2 - бяха намалени със 130% от генния трансфер на CuZn SOD или извънклетъчен SOD. Взети заедно, тези проучвания показват, че намалената ендотелна зависимост-релаксация не изглежда да се дължи на липсата на ензима SOD.
Като се има предвид, че нямаме доказателства, които да предполагат, че eNOS или SOD протеините са намалени в този модел, защо релаксацията на аортата е нарушена при животни, изложени на висок хранителен холестерол или метионин и на практика се премахва, когато двете диети се комбинират? Отговорът на този въпрос е несъмнено сложен и може да се отнася до скорошни доказателства, които предполагат, че eNOS може да произвежда O2 - вместо NO в стресираща среда. 32 В допълнение, други предполагат, че самият ензим eNOS може да е нефункционален, 33 и допълнителни доказателства за дисфункционален протеин eNOS произтичат от проучвания на генния трансфер, при което генетичният трансфер на eNOS към атеросклеротични съдове значително подобрява вазодилатацията 34, докато генетичният трансфер на SOD към атеросклеротичните съдове нямат ефект. 31
Както беше споменато по-горе, реакцията на излишък O2 - с излишък на NO образува пероксинитрит (ONOO -), който може да нитрира остатъка от тирозин на протеини, образувайки нитротирозин. 14 По този начин идентифицирането на нитротирозин в аортната стена чрез имунохистохимия е маркер за нитративен стрес. 15 Тъй като образуването на нитротирозин в атеросклеротичните плаки не се дължи единствено на реакцията на остатъка от тирозин в протеини с ONOO -, но също и на реакцията на тирозилови радикали, NO · 2, NO - 3, NO2Cl и HOCl с тирозин, 15 образуването на нитротирозин е точен маркер за нитративен стрес. По този начин нитративният стрес изглежда присъства в аортите на животни, хранени с висок хранителен холестерол, метионин или комбинация от двете, което е в съответствие с предишни доклади при хора 35, но не и с други субекти. 36 Дали нитротирозинът, присъстващ в съдовете в това проучване, се дължи на излишък от ONOO - или други нитратни съединения, остава несигурно.
В подкрепа на резултатите, представени в това проучване, Eberhardt et al 9 показват, че при миши модел на лека хиперхомоцистинемия мишките показват нарушена ендотелна релаксация до метахолин без видимо намаление на eNOS имунореактивността, повишена нитротирозинова имунореактивност и повишено генериране на O2 в аортата в сравнение с мишки от див тип. Освен това, Lentz et al 10 показват в същия модел на животни, че ниският хранителен фолат също повишава плазмените нива на хомоцистеин и това води до ендотелна дисфункция.
Доказано е, че макрофагите в плаките произвеждат цитокини, които могат да стимулират производството на iNOS, производството на O2 и различни биологично активни вещества в тяхната местна среда. Нашите резултати подкрепят тази идея, тъй като макрофагите са локализирани в плаки във връзка с iNOS, eNOS, SOD и нитротирозин. Освен това, идентифицирането на iNOS в атеросклеротичните плаки показва, че може да има високи нива на NO, образувани в тези области. 13 Всъщност такива високи нива на NO могат да доведат до образуването на нитротирозин, който също е идентифициран в тези плаки. Възможно е тези токсични, цитолитични ефекти на излишния NO да допринесат за клетъчна смърт и тъканна некроза, често наблюдавани при напреднали атеросклеротични лезии. 38 В това отношение излишното производство на NO в атеросклеротичните лезии може да бъде по-скоро вредно, отколкото полезно за функцията на съдовата стена. Взети заедно, нашите резултати и други показват, че ендотелната дисфункция, наблюдавана при хиперхомоцистинемия или хиперхолестеролемия, е многофакторен процес и са необходими допълнителни изследвания на механизмите на ендотелната дисфункция.
Интересна констатация в това проучване е, че плазменото ниво на хомоцистеин е повишено с висок диетичен метионин, но когато и двете диети се комбинират (в групата на MethChol), плазмените нива на хомоцистеин при тези животни са по-ниски от тези, хранени само с висок диетичен метионин, и макар и леко повишени в сравнение с контрола, тези нива не се различават значително. Това може да представлява нов път на метаболизъм на хомоцистеин. Всъщност метаболизмът на холестерола и хомоцистеина може да бъде взаимосвързан, тъй като in vitro проучванията показват, че хомоцистеинът стимулира производството на холестерол в хепатоцитите 39, а проучване при хора показва, че плазмените нива на хомоцистеин са свързани с нивата на холестерола в плазмата. 40 Взети заедно с нашите резултати, изглежда, че in vivo при заека повишенията в плазмения холестерол може да повлияят нивата на хомоцистеин. Въпреки че не можем да изключим възможността плазмените нива на хомоцистеин да бъдат повишени в комбинираната група в ранните етапи на диетичната интервенция, която след това намалява в края на диетичния режим, са необходими допълнителни проучвания за потвърждаване на тази хипотеза.
В заключение, нашите резултати показват, че комбинацията от висок хранителен холестерол плюс метионин, прилаган на зайци в продължение на 12 седмици, практически премахва ендотелната функция. Тези резултати предполагат, че комбинацията от висок хранителен холестерол и метионин може да влоши появата на атеросклероза и подчертава значението на множество рискови фактори за прогресирането на сърдечно-съдовите заболявания.
- Здравословна диета за високо кръвно налягане и холестерол - Medlife Blog Health and Wellness Tips
- Диета с висок холестерол; Уелнес решения за храненето
- Съвети за висок холестерол, насоки Яжте здравословна диета
- Диета с висок холестерол Ефективни съвети, храни и здравословни рецепти за управление на вашия висок холестерол
- Дългосрочни ефекти на кетогенната диета при затлъстели лица с високо ниво на холестерол - PubMed
