Аменорея (отсъствие на менструация) е пълно отсъствие на менструация след пубертета, което се нарича „първична аменорея“ и причината обикновено е ендокринна аномалия.
Свързани термини:
- Естроген
- Пролактин
- Лутеинизиращ хормон
- Хиперпролактинемия
- Фоликулостимулиращ хормон
- Гонадотропин-освобождаващ хормон
- Гонадотропин
- Галакторея
- Тестостерон
- Диуретик
Изтеглете като PDF
За тази страница
Хипоталамусна ановулация, функционална
Боаз Вайс, Ариел Хурвиц, в Енциклопедия на ендокринните болести, 2004 г.
Въведение
Аменореята, отсъствието на менструално кървене, не е необичайно през репродуктивните години. Ановулацията и съответно аменорея при небременни жени в репродуктивна възраст е патологична. Критериите, използвани за определяне на аменорея, не са еднакви. Често използваните критерии определят жените без менструация на възраст от 14 години (без вторични полови характеристики) до 16 (с появата на вторични полови характеристики) като жени с първична аменорея. Жените, които редовно менструират и след това изпитват отсъствие на менструация в продължение на 6 месеца (или три цикъла за пациенти с олигоменорея), се характеризират като вторична аменорея. Разпространението на аменореята е 1,5–3% от женското население през репродуктивните години. Докато първичната аменорея е доста рядка, вторичната аменорея не е рядкост при жени в репродуктивна възраст.
Ановулацията и последващата аменорея могат да бъдат класифицирани по различна етиология. Причините за аменорея включват анатомични аномалии на гениталната система, генетични дефекти, ендокринопатии, яйчникова недостатъчност, дисфункция на хипофизата и хипоталамусна дисфункция. Относителната честота на всяка етиология зависи от популацията. Въпреки че някои изследователи установяват, че синдромът на поликистозните яйчници (СПКЯ) е най-честата причина за ановулация, други установяват, че свързаната със загуба на тегло аменорея е водещата причина за спиране на менструацията. В повечето проучвания обаче приблизително две трети от всички пациенти с аменорея са хипоестрогенни поради дисфункция на хипоталамус-хипофизата или резистентност на крайните органи към гонадотропини. Приблизително една трета от пациентите са диагностицирани с нормогонадотропна ановулаторна аменорея (най-вече СПКЯ).
Аменорея ☆
Определение
Аменореята може да бъде първична, което означава, че никога не е настъпила или вторична, което показва, че е възникнала и впоследствие е спряна. Причините за аменорея вероятно са промени в хипоталамуса, яйчниците или матката. Строго определение за първична аменорея е липсата на маточно кървене до 16-годишна възраст (Schlaff and Kletzky, 1998; Lobo, 2012; Klein and Poth, 2013). Вторичната аменорея се определя като отсъствие на мензис за период от шест месеца при жени, които преди това са имали редовни менструални цикли. При жените с олигоменорея липсата на мензис за период от 12 месеца се класифицира като аменорея.
РАЗРУШЕНО ПОВЕДЕНИЕ ПРИ ХРАНЕНЕ
Аменорея
Хранителни разстройства и репродуктивната ос
Мишел П. Уорън, Дженифър Е. Домингес, в Енциклопедия на ендокринните болести, 2004
Аменорея
Аменореята, липсата на менструални периоди, е основният ефект от хранителните разстройства върху репродуктивната система. Той може да бъде класифициран като първичен или вторичен, в зависимост от времето на настъпване. Първичната аменорея е забавяне на менархе над 16-годишна възраст. Вторичната аменорея се появява, когато периодите отсъстват повече от 3 до 6 месеца при жени, които преди това са имали редовно менструация. Дисфункциите, които водят до аменорея, са многобройни и могат да бъдат резултат от ендокринни или физически смущения при различни стъпки по репродуктивната ос. Обаче видът на аменорея, който обикновено се наблюдава при хранителни разстройства, е обратима хипоталамусна аменорея. Той може да бъде първичен или вторичен по характер, в зависимост от това дали хранителното разстройство е започнало преди пубертета, като по този начин се забавя менархе.
Физиологичната основа на хипоталамусната аменорея е нарушаването на пулсиращата секреция на хипоталамуса на GnRH. Редица проучвания показват депресия в пулсирането на GnRH, свързана с глад. Това предполага, че генераторът на импулси GnRH може да бъде повлиян от метаболитни горива и/или е в състояние да усети спад в теглото под определена зададена точка. Когато разходът на енергия е по-голям от приема на храна, възниква инхибиране на GnRH, като по този начин се намалява освобождаването на LH и FSH от предната част на хипофизата и се изключва или ограничава стимулацията на яйчниците и производството на естрадиол.
Въпреки че действителните нива на LH и FSH може да не изглеждат значително променени, 24-часовите модели на хормоналните импулси по-скоро приличат на предпубертетни модели от тези на зряла жена. Препуберталните модели на LH и FSH се характеризират с намалени и ниско амплитудни пулсации. Проучванията обаче показват, че фоликуларното съзряване и дори менструацията могат да бъдат предизвикани при много пациенти чрез пулсиращо приложение на екзогенен GnRH. Следователно, както се вижда при пациенти, които възстановяват теглото си, аменореята може да бъде обратима, когато се възстанови нормалната пулсативност на хормоните.
Затлъстяване, метаболитен синдром и нарушения на енергийния баланс
Д-р Рам Вайс, д-р Робърт Х. Лустиг, магистърска степен по детска ендокринология (четвърто издание), 2014 г.
Оста на хипоталамус-хипофиза-гонада. U
Урогенитална система
Нарушения на менструацията
Приматите от Стария свят имат менструални цикли, за разлика от естрозните цикли, наблюдавани в Новия свят и просимианските примати. Менструалната цикличност определя периода от време между началото на вагинално кървене от един цикъл до следващия. При повечето видове менструалният цикъл е приблизително 28–30 дни, като овулацията настъпва на 12–15 дни. Видовете, показващи вагинално кървене, свързани с менструация, притежават маточни спирални артерии, които са способни да отговорят на хормонално оттегляне в края на лутеалната фаза. Често други външни признаци, включително промяна в цвета на кожата, сексуално поведение и/или подуване на перинеума, могат да предоставят възможности за откриване на стадия на цикъла, в зависимост от вида. (Читателят е посочен и към том 1, глава 9 за по-подробна информация относно физиологията на нормалния менструален цикъл.) Менструалната дисфункция е симптом на основната патология на репродуктивната система. Аномалията може да бъде развитие, ендокринологична или придобита в резултат на анатомична лезия. Нарушенията на менструацията могат да бъдат разделени на две категории, включително липсата на менструация (аменорея) и абнормно маточно кървене.
Ненормалното маточно кървене отразява значителна промяна в модела на менструация, която трябва да се характеризира точно, тъй като терапията зависи от специфична етиология. Таблица 10.3 предоставя определения, които са полезни при описването и характеризирането на анормални маточни кръвоизливи при небременни животни (Severino, 1995). Многобройни менструални нарушения са разпознати при нечовешките примати (Van Pelt, 1974).
ТАБЛИЦА 10.3. Термини, дефиниращи анормални маточни кръвоизливи
| Олигоменорея | Кървене на интервали по-големи от 40 дни, което обикновено е нередовно |
| Полименорея | Кървене на интервали под 22 дни, които могат да бъдат редовни или нередовни |
| Менорагия | Кървене, което е прекомерно както по количество, така и по продължителност на редовни интервали |
| Метрорагия | Кървене от обикновено нормално количество, но на нередовни интервали |
| Менометрорагия | Кървенето с прекомерно количество, продължително и може да се появи на равни или нередовни интервали |
| Хипоменорея | Редовно маточно кървене в намалено количество |
| Интерменструално кървене | Кървене, което се случва между това, което иначе е редовно менструално кървене |
| Дисменорея | Болезнена менструация, която може да се прояви като изолирано разстройство или във връзка с други състояния |
Аменорея
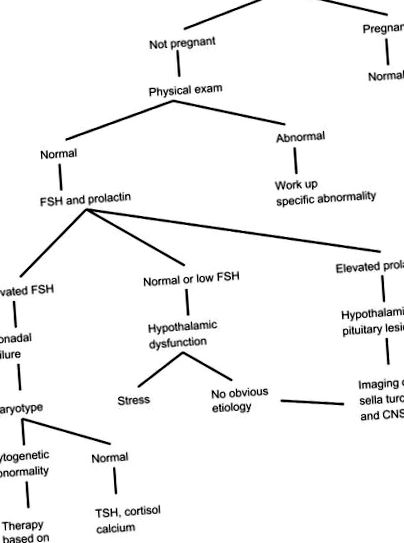
По-нататък аменореята се класифицира като първична, ако менархе не се появи, и вторична, ако менструацията престане за поне 6 месеца при постменархално животно. Аменореята може да бъде резултат от хипоталамусна или хипофизна дисфункция, яйчникова недостатъчност или анатомична аномалия. Диагностичен алгоритъм за оценка на аменорея е показан на фигура 10.18 .
ФИГУРА 10.18. Диагностичен алгоритъм за аменорея.
Дисменорея
Менорагия
Менорагията или менструацията, която е прекомерна както по количество, така и по продължителност, е често срещана клинична находка при нечовешките примати. Има много възможни причини, включително вътрематочни маси, като ендометриални полипи и лейомиоми, ранни аборти, но това състояние често е идиопатично без очевидна причина. Диагностиката трябва да бъде насочена както към откриване на основното клинично състояние, като се използват ултразвукови и хормонални анализи, но също така трябва да включва кръвна работа за оценка на вторичните анемии и основните коагулопатии. Лечението трябва да бъде насочено към отстраняване на основната причина, като хирургично отстраняване на маса. При идиопатичната менорагия авторите са постигнали известен успех с краткосрочната терапия с прогестерон.
Гинекологична заболеваемост
Аменорея
Аменореята е състоянието да нямате менструални периоди. Първичната аменорея описва отсъствието на мензис (преди менархе), а вторичната аменорея описва спирането на менструацията (след менархе). Олигоменореята е състоянието на редки менструални периоди.
Настоящите препоръки за определяне на времето за оценка на първичната аменорея отчитат тенденцията към по-ранна възраст при менархе и следователно се посочват, когато е имало неуспех да се менструира до 15-годишна възраст при наличие на нормално вторично полово развитие или в рамките на 5 години след развитието на гърдата ако това се случи преди 10-годишна възраст.
Липсата на развитие на вторични сексуални характеристики до 13-годишна възраст също изисква разследване.
Препоръчително е да се изследва вторична аменорея с продължителност три месеца и олигоменорея, включваща по-малко от девет цикъла годишно (Практически комитет на Американското общество за репродуктивна медицина, 2006).
Съществува широк спектър от причинни фактори за аменорея (вж Фигура 1 ), но често не може да се определи ясна причина. Винаги трябва да се има предвид възможността за бременност и трябва да се извърши цялостна анамнеза и задълбочен преглед. Подходяща за възрастта аменорея на възраст над 45 години съответства на менопаузата (средна възраст 51 години).
Фигура 1 . Предложена диаграма на потока, подпомагаща оценката на жени с аменорея. Адаптиран от Практическия комитет на Американското общество по репродуктивна медицина (2006) Текуща оценка на аменореята. Плодовитост и стерилност 86 (добавка 5): S148–155.
Могат да бъдат показани лабораторни тестове (включително гонадотропини, пролактин и стимулиращ хормона на щитовидната жлеза) и образна диагностика (таза или sella turcica). Ако има данни за хиперпролактинемия или дисфункция на щитовидната жлеза, подходящото изследване и лечение трябва да възстановят менструацията.
Ниските нива на гонадотропин (т.е. хипогонадотропният хипогонадизъм) предполагат аномалия на хипофизата или хипоталамуса, но често срещана причина при тийнейджърите е конституционното забавяне, което често е фамилно. Други редки причини включват тумори на централната нервна система, черепно облъчване, разрушаване на хипоталамуса или хипофизата, синдром на Sheehan и синдром на Kallmann (който е свързан с аносмия). Хипоталамичната аменорея често се причинява от прекомерна загуба на тегло, тежки упражнения, стрес или хронично заболяване. Младите спортисти могат да развият комбинация от състояния, наречена „триада на женски спортисти“, която включва хранително разстройство, аменорея и остеопороза. Мензисът обикновено се връща, след като се постигне здравословно телесно тегло с умерено увеличаване на приема на калории и/или намаляване на тренировката. Важно е за юношите и младите жени да избягват загуба на костна маса през този период на пиково развитие на костната маса.
Повишените нива на гонадотропин (фоликулостимулиращ хормон (FSH) и лутеинизиращ хормон (LH)) предполагат аномалия на яйчниците (хипергонадотропен хипогонадизъм). Многократно повишените нива на гонадотропин при жени на възраст под 40 години се определят като преждевременна яйчникова недостатъчност (POF), която засяга 0,1% от жените до 30 години и 1% от жените до 40-годишна възраст. Може да бъде причинено от химиотерапия, лъчетерапия, галактоземия и заушка оофорит или да бъде свързано с автоимунни нарушения (хипотиреоидизъм, захарен диабет, болест на Адисон/надбъбречна недостатъчност) и генетични нарушения (включително дисгенезия на гонадите, като синдром на Търнър (45, XO кариотип) и крехък X синдром). Жените под 30 години трябва да имат анализ на кариотипа. Около 5–10% от жените с ПОФ могат да постигнат естествено зачеване, но жените трябва да бъдат запознати с възможностите за асистирано зачеване, включително донорство на яйцеклетки. Жените с POF могат да бъдат изложени на повишен риск от остеопороза и сърдечни заболявания.
Причините за хиперандрогенна ановулация включват синдром на поликистозните яйчници (PCOS), андроген-секретиращи яйчникови или надбъбречни тумори, болест на Кушинг, акромегалия, некласична вродена надбъбречна хиперплазия и приложение на екзогенни андрогени.
Ендокринология на ХИВ/СПИН
Дисфункция на женските полови жлези
Аменореята се наблюдава при приблизително 25% от заразените с ХИВ жени и може да бъде причинена от намаляването на производството на гонадотропин, свързано със стреса от заболяване. За разлика от това, ановулация може да се наблюдава при до 50% от заразените с HIV жени във връзка с намален брой на CD4. Сред ановулаторните ХИВ-заразени жени промените в менструалната функция са три пъти по-вероятни в сравнение с нормално овулиращите пациенти. Ранна менопауза се съобщава при до 8% от заразените с ХИВ жени. 18.
Нивата на андроген често се намаляват при заразени с ХИВ жени. В едно проучване, нивата на андроген, оценени с помощта на безплатен тест за тестостерон, са намалени под нивото, наблюдавано при здрави жени, съответстващи на възрастта, при над 50% от заразените с ХИВ жени със значителна загуба на тегло и при над една трета от ХИВ- заразени жени без загуба на тегло. 19 Механизмите на андрогенния дефицит при ХИВ заболяване могат да бъдат причинени отчасти от интра-надбъбречното шунтиране към производството на кортизол и далеч от производството на андроген, особено при жени със значителна загуба на тегло 6 (вж. „Надбъбречна функция“).
Менструални цикли и стрес *
Биологични ефекти на стреса върху менструацията
Аменореята се определя от отсъствието на мензис в продължение на 3 или повече месеца. Неуспехът на менархе да се назове се нарича първична аменорея; вторична аменорея се отнася до прекратяване на менструацията след началото на менархе. Процентът на разпространение на вторичната аменорея варира от 8,5% при жените на възраст 13–18 години, 7,6% при жените на възраст 15–24 години и 3% при жените на възраст 25–34 години.
Възможен механизъм, който може да свърже генератора на импулси GnRH и стреса, включва хипоталамо-хипофизарно-надбъбречната ос (HPA), която се активира от стреса. Жените с вторична аменорея често проявяват хиперкортизолизъм, а при маймуни и плъхове приложението на кортикотропин освобождаващ хормон (CRH) води до остро намаляване на пулсиращото освобождаване на GnRH и гонадотропин. CRH също инхибира LH чрез централни ефекти, частично медиирани от централните ендогенни опиати. Стресът стимулира експресията на CRH и вазопресин. При маймуни е доказано, че вазопресинът намалява остро секрецията на LH, когато се прилага интрацеребровентрикуларно.
Допълнителни доказателства, предполагащи участието на оста HPA, са предоставени от Berga, който демонстрира, че концентрациите на кортизол, които отразяват активността на HPA, са повишени при жени с FHA. Установено е, че при жени с други причини за ановулация концентрациите на кортизол са сравними с тези, наблюдавани при жени, които са били евмонореи с биохимични данни за овулация. Жените с FHA, които възобновяват овулацията, са имали концентрации на кортизол, подобни на тези при еуменореи и по-ниски от жените с персистираща FHA.