Марлон Е. Серф * и Йохан Лу
Южноафрикански съвет за медицински изследвания, Кейптаун, Южна Африка
* Автор-кореспондент: Marlon E Cerf
Платформа за откриване на диабет
Южноафрикански съвет за медицински изследвания
P. O. Box 19070; Тигерберг
7505, Кейптаун; Южна Африка
Тел +27-21. 938. 0304
Факс +27 - 21. 938. 0456
Електронна поща Марлон. [имейл защитен] ac. za
Получено 16 април 2013 г. - Прието 3 март 2014 г.
Резюме
Ключови думи
Клетъчно разпространение; Захарен диабет, тип 2; Клетки, секретиращи глюкагон; Хиперлипидемии; Клетки, секретиращи инсулин; Островчета Лангерханс
Съкращения
ANOVA: дисперсионен анализ; FFA: свободна мастна киселина; GSIS: стимулирана от глюкоза секреция на инсулин; СН: високо съдържание на мазнини; HFD: диета с високо съдържание на мазнини; HOMA-B: оценка на модела на хомеостазата бета клетъчна функция; HOMA-IR: оценка на модела на хомеостазата инсулинова резистентност
ВЪВЕДЕНИЕ
Островните клетки се развиват през целия живот и демонстрират пластичност в отговор на метаболитното търсене за поддържане на глюкозната хомеостаза. При мишки пъпката на панкреаса се образува при
e9. 5 по време на първичния преход, включващ клетки, които могат да доведат до трите основни линии на панкреаса при възрастни: ендокринни, екзокринни и канал [1]. Мезенхимът е необходим за правилното моделиране, растеж и диференциация на ембрионалния панкреас [2]. При гризачите повечето островчета се развиват преди раждането и през непосредствения период след раждането, докато се подлагат на значително преустройство. Критичните периоди на развитие на островчета при гризачи са морфогенезата на островчета в e17-19 [3] и първата седмица от живота, когато настъпва неогенезата [4]. Всяко нарушение в околната среда на островните клетки в определен момент от развитието може да наруши баланса на контролиращите фактори, като по този начин допринесе за дисфункция на бета-клетките и диабет по-късно в живота [5].
Променено метаболитно състояние на повишено търсене на инсулин, като затлъстяване, което е силно свързано с инсулинова резистентност, дава податливост за развитие на метаболитно заболяване. Хроничното хранене с високо съдържание на мазнини (HF) е свързано с патогенезата на затлъстяването, инсулиновата резистентност и дисфункцията на бета-клетките. Повишеният приток на свободни мастни киселини (FFA) или наситени мастни киселини от диета с високо съдържание на мазнини (HFD) може да индуцира адипогенеза и метаболитен синдром, също модулирайки възпалителния отговор [2, 3]. Гризачите при хронични HFD са били със затлъстяване, хиперлипидемия, непоносимост към глюкоза и нечувствителност към инсулин с нарушена инсулинова сигнализация, отразяваща инсулиновата резистентност [6]. В друго проучване мишки, хранени с хронични HFD, показват бета-клетъчна дисфункция, нарушена глюкозо-стимулирана секреция на инсулин (GSIS) и глюкозна непоносимост като последица от инсулиновата резистентност [7].
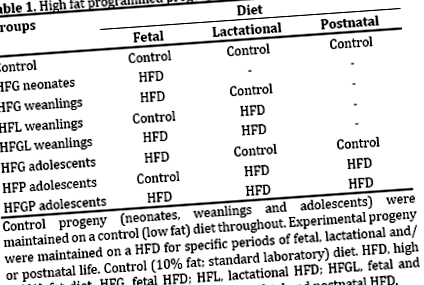
Програмирането е излагане на стимули или обиди (т.е. събития) по време на критични етапи на живот, особено по време на фетален и лактационен живот, които оформят метаболизма и физиологията на потомството незабавно, преходно и/или постоянно. Програмирането с високо наситени мазнини (по-нататък HF програмиране) е излагането на HFD (≥40% от предимно наситените мазнини като енергия) по време на критичните етапи на живота. По-рано демонстрирахме, че HF програмирането променя развитието и физиологията на островните клетки, като по-специално компрометира целостта и функцията на бета клетките, при новородени [8, 9], отбиване [10, 11, 12] и подрастващи плъхове [13].
Неотдавнашното ни проучване при подрастващи плъхове [13] се фокусира върху специфичните за пола ефекти, а не върху глобалните представителни ефекти на комбинираните полове, както в предишните проучвания за новородени и отбиване. Следователно настоящото проучване ще оцени реакциите на островчетата към програмирането на СН при тези подрастващи потомства (комбинирани полови фенотипове). Ще бъдат представени промените в метаболитните параметри (телесно тегло, лептинемия, гликемия, инсулинемия, HOMA и липидемия) и морфометрия на островчетата (брой на островните клетки, размер, обем, съотношения и пролиферация) на тези подрастващи потомци.
МАТЕРИАЛИ И МЕТОДИ
Експериментален дизайн
Метаболитни параметри
Оценените метаболитни параметри са телесно тегло (предварително определено при новородени и отбиващи), тегло на панкреаса (също коригирано спрямо телесното тегло: тегло на панкреаса/телесно тегло X 100), серумен лептин на гладно (комплект RIA лептин RIA, Linco Research, St. Charles, MO, САЩ; не е определена при новородени поради недостатъчни серумни обеми), кръвна глюкоза (глюкомер, Precision QID, MediSense, Oxfordshire, UK) и серумни концентрации на инсулин (инсулин за плъх RIA, Linco Research; предварително определено при новородени и отбиване), HOMA-инсулинова резистентност (IR) ([кръвна глюкоза на гладно (mmol/L) X серумен инсулин на гладно (mU/L)]/22. 5)) и функция на HOMA-бета клетки (B) ([20 X инсулин на гладно (mU/L)]/глюкоза (mmol/L) - 3. 5)). HOMA индексите бяха адаптирани за новородени, тъй като серумите бяха обединени за измерване на инсулин; следователно няма налични индивидуални концентрации на инсулин. Въпреки това, инсулинът беше съобразен с концентрациите на глюкоза за група за оценка. При юноши (не е определено при новородени или отбиване) серумните триглицериди на гладно (метод GPO-PAP, автохумализатор A5, Human Diagnostics, Wiesbaden, Германия) са общо LDL и HDL холестерол (бърза тънкослойна хроматографско-течна процедура) определено, както е описано по-рано [14]. Освен това се определят съотношенията общ холестерол към HDL холестерол.
За телесно тегло n = 44 за контрол, n = 9 за HFG, n = 20 за HFP и n = 10 за HFGP юноши. За тежести на панкреаса, n = 6 за контрол и n = 18 за новородени HFG; n = 14 за контрол и n = 6 за HFG, HFL и HFGL отбивания; n = 40 за контрол, n = 3 за HFG, n = 6 за HFP и n = 4 за HFGP юноши. За лептин, n = 8 за контрол, n = 5 за HFG, n = 8 за HFL и n = 6 за HFGL отбивания; n = 16 за контрол, n = 6 за HFG, n = 14 за HFP и n = 5 за HFGP юноши. За концентрациите на глюкоза n = 46 за контрола, n = 13 за HFG, n = 24 за HFP и n = 10 за юноши с HFGP. За концентрациите на инсулин n = 34 за контрол, n = 8 за HFG, n = 20 за HFP и n = 5 за юноши с HFGP. За HOMA-IR и HOMA-B, n = 10 за контрол и n = 6 за HFG новородени; n = 25 за контрол, n = 6 за HFG, n = 9 за HFL и n = 5 за HFGL отбиване; n = 22 за контрол, n = 7 за HFG, n = 14 за HFP (за HOMA-IR, но n = 13 за HOMA-B) и n = 5 за HFGP юноши. За липидни профили n = 6 за контролни и HFG юноши и n = 4 за HFGP, докато HFP юношите са изключени поради n = 2.
Морфометрия на островчета
Панкреатите бяха двойно имуномаркирани с инсулин и глюкагон, последвано от анализ на изображението, както беше описано по-рано [8]. Изчислени са бета и алфа клетъчни номера, размери и обеми, съотношения на бета към алфа клетки (предварително определени при новородени и HFG отбивания), съотношения на алфа към бета клетки, индекси на пролиферация на островни и ацинарни клетки [8, 11, 13].
Цели панкреати се събират с 4 μm2 серийни секции, избрани за експерименти с имуномаркиране. Алфа клетките първо бяха имуномаркирани с поликлонално глюкагоново антитяло (Dako, Carpinteria, СА, САЩ), последвано от имуномаркиране на бета клетките с моноклонално инсулиново антитяло (Sigma ImmunoChemicals, St Louis, MO, USA) [13]. За анализ на изображения е използван цифров фотоапарат Canon Powershot S40 (Canon, Tochigi, Япония), монтиран на светлинен микроскоп Olympus BX60 (Olympus, Токио, Япония), прикрепен към персонален компютър [13]. Окончателните цифровизирани изображения са 768 X 1024 пиксела [13].
Индексите на пролиферация на островни и ацинарни клетки са изчислени след имунооцветяване с пролиферационен маркер, Ki67 (MIB5; DakoCytomation, Glostrup, Дания) [13]. Бяха преброени петстотин ядра от всеки клетъчен тип (островни и ацинарни клетки) [13]. Броят на пролиферативните клетки беше разделен на общия брой клетки, за да се определят индексите на пролиферация на островчетата и ацинарните клетки [13]. За пролиферация на островни и ацинарни клетки n = 6 за контрол и n = 12 за HFG новородени; n = 8 за контрол, n = 6 за HFG и HFGL и n = 8 за HFL отбивания; n = 6 за контрола и n = 5 за HFG, HFP и HFGP юноши.
СТАТИСТИКА
За новородените беше приложен тест на несдвоения студент за анализ на двете групи. За отбитите и юношите четири групи бяха сравнени, използвайки еднопосочен ANOVA, последван от post-hoc тест на Bonferroni. Данните се отчитат като средни стойности ± SEM със значимост, установена на стр
- Как да получите по-голямо дупе с висок метаболизъм Живей здравословно
- Живот с хипопротеинемия (ниско съдържание на протеини) Високопротеинова диета за хипопротеинемия - ниско съдържание на протеини -
- Някой някога опитвал ли е диета с ниско съдържание на въглехидрати и високо протеини - BikeRadar
- Производство на газ, метан и въглероден диоксид in vitro на високо влакнеста диета, инкубирана с фекалии
- Пълномаслено органично високо протеиново хоризонт