Егидио Дел Фабро
Ключови думи: Мултимодална терапия; рак; кахексия
Подадено на 27 юни 2018 г. Прието за публикуване на 6 август 2018 г.
Въведение
Кен Феарон призна, че определящите характеристики на кахексията при хората (загуба на тегло, намален прием на храна и хронично възпаление) могат да осигурят рамка за класификация на кахексията и обосновка за идентифициране на множество терапевтични цели (1). Чрез комбиниране на фармакологични и нефармакологични интервенции, многостранните механизми на този сложен синдром могат да бъдат решени едновременно, което води до подобрен прием на протеини и калории, повишаване на мускулите и мазнините и по-добра физическа функция. Освен това беше оценена ролята на съпътстващите заболявания, като свързана с възрастта саркопения и обездвижване, допринасящи за загуба на мускули, осигурявайки оправдание за включване на физическа активност и хранителна подкрепа при формулирането на цялостна терапия на кахексия за „целия пациент“. Предклиничните изследвания, изясняващи сложните молекулярни механизми на кахексията на рака, разкриват допълнителна подкрепа за включването на специфични индивидуални интервенции в мултимодални стратегии за лечение и повишена чувствителност към кахексия поради генетични вариации.
Въпреки това, в продължение на повече от две десетилетия, въпреки повтарящите се проблясъци на успех, сериозните доказателства за тази концепция за „мултимодална терапия за многоизмерен проблем“ се оказаха неуловими. Този преглед ще подчертае изследванията, които осигуряват подкрепа за използването на променлива комбинация от хранителни, физически упражнения и фармакологични интервенции. Прегледът се фокусира и върху минали клинични проучвания, включващи нестероидни противовъзпалителни лекарства (НСПВС) и омега-3 добавки в комбинирана терапия - две от основните агенти, заедно с поддържащи грижи, които са включени в MENAC (Мултимодални упражнения, хранене и анти -възпалително лекарство за кахексия), многоцентрово проучване, разработено от покойния Кен Ферън (2).
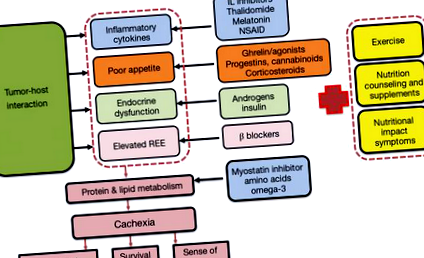
Теоретичен модел на мултимодална терапия за кахексия е показан на фигура 1. Въпреки че може да има дебат относно състава или относителната важност на конкретни индивидуални интервенции, моделът илюстрира обосновката на мултимодалното лечение, насочено към различните механизми на кахексия.
Индивидуализиран мултимодален модел
Въз основа на предпочитанията на пациента
Необходими са допълнителни клинични и биологични маркери, за да се идентифицират по-добре индивидите, които могат да реагират на специфични интервенции. Биомаркерите за кахексия са в ранна детска възраст, но в бъдеще могат да улеснят по-ранна интервенция, по-ефективни индивидуализирани терапевтични режими и по-малко ненужни странични ефекти. Провъзпалителните цитокини, реактивните кислородни видове (ROS) (8,9) и еднонуклеотидните полиморфизми (10,11) са примери за маркери, които могат да помогнат за създаването на биологични профили на кахектичните пациенти.
Фармакологични комбинации
Само монотерапията е малко вероятно да коригира множествените аномалии, свързани с кахексия като загуба на мускули, мазнини и физическа функция поради отрицателния протеинов и енергиен баланс, обусловен от намаления прием на храна и метаболитната дисфункция. Дори един ефективен фармакологичен агент би трябвало да се комбинира с диетични консултации, добавки, управление на симптомите и упражнения. Комбинираната терапия в идеалния случай трябва да има адитивни или дори синергични ефекти. За съжаление, някои съвременни лекарства като мегестрол ацетат (МА) или медроксипрогестерон могат да модулират благоприятно един път, като същевременно насърчават други потенциално вредни механизми. Например, въпреки че прогестините могат да намалят провъзпалителните цитокини и да подобрят апетита, те са свързани с ендокринни аномалии като хипогонадизъм и хипоадренализъм (12). Други лекарства като кортикостероиди са ефективни стимуланти на апетита, но имат вредни ефекти върху мускулната функция, включително миопатия. Някои единични интервенции за разследвана кахексия, като грелин, агонисти на грелин, бета-блокери и упражнения, изглеждат особено обещаващи, тъй като могат да повлияят благоприятно на повече от един механизъм (например възпалителни, както и неврохормонални пътища).
НСПВС
Много НСПВС, включително целекоксиб, ибупрофен, индометацин и етодолак (13), са били използвани самостоятелно или в комбинация с други агенти за различни клинични резултати, свързани с ракова кахексия. Систематичен преглед на литературата идентифицира 11 от 13 проучвания, показващи подобрение или стабилизиране на теглото или чистата телесна маса (LBM) (14). Авторите обаче стигнаха до заключението, че доказателствата са недостатъчни, за да препоръчат НСПВС за кахексия извън клинични изпитвания, тъй като седем са без сравнителен апарат, повечето имат малък размер на пробата, а някои са с методологически недостатъци. Опитите с използване на НСПВС в комбинация с други агенти включват две опити, комбиниращи НСПВС с МА и НСПВС с рибено масло, които са сравнени съответно с МА и рибено масло, съответно.
Проспективно рандомизирано проучване на ибупрофен (1200 mg/ден) в комбинация с МА, установява значително подобрено качество на живот (QoL) и средно повишение на теглото от 2,3 kg в сравнение със загуба от 2,8 kg само при пациенти с МА, със стомашно-чревни ( GI) рак (15). Забележително е, че хората на комбинирана терапия с ибупрофен не изглежда да са изложени на по-голям риск от големи кръвоизливи от тези на MA само (480 mg дневно). Проучване във фаза III при 104 пациенти в напреднал стадий на гинекологичен рак установи, че MA плюс L-карнитин, целекоксиб и антиоксиданти подобряват LBM, измерено чрез двуенергийна рентгенова абсорбциометрия (DEXA), REE, умора и QoL в сравнение само с MA (16 ). Мерките за възпаление и оксидативен стрес, включително IL-6, TNF-α, CRP и ROS, намаляват значително при комбинирана терапия.
6-седмично проспективно проучване на 22 пациенти с напреднал рак на белия дроб сравнява целекоксиб (200 mg два пъти дневно) в комбинация с рибено масло само с рибено масло (6 g дневно в разделени дози). Тези, които получават комбинирани терапии, имат значително по-ниски нива на CRP (17) (21,3 mg/L; стандартна грешка 7) и по-голяма сила на ръкохватката (3,12; 0,98), отколкото пациентите, получаващи монотерапия (6,7 mg/L; 4,5 и 1,16; 0,3), съответно. И двете групи са получили хранителна добавка, еквивалентна на 20% от базалния метаболизъм (BMR), в допълнение към диетичните съвети, насочени към поддържане на калориен прием, еквивалентен на BMR.
И накрая, шведски център с история на използване на комбинирана терапия за ракова кахексия сравнява стандартните грижи (SC) за кахексия в техния център с SC плюс ниски дози инсулин при 138 пациенти с напреднали GI злокачествени заболявания (18). SC, включва индометацин за пациенти с повишен CRP, плюс еритропоетин за анемия и ентерално или парентерално хранене за намален прием на храна (
Ролята на лечението на симптомите и поддържащите грижи е основополагаща при справянето с много участници в намаляването на приема през устата. Те включват ранно насищане, промени в вкуса и обонянието, мукозит, гадене, запек, болка, дисфагия, умора и депресия (32). Тези симптоми са често срещани (33), намаляват енергийния прием (34) и реагират на лесно достъпни, евтини лекарства, увеличавайки приема през устата и наддаване на тегло при до една трета от пациентите (32). Други метаболитни аномалии, като хипогонадизъм, дефицит на витамин В12, хипотиреоидизъм и хипоадренализъм, също могат да допринесат за анорексия и загуба на мускулна маса при пациентите; обаче ниският тестостерон при мъжете и дефицитът на витамин D (35) изглежда са най-чести. Значението на NIS беше подчертано от проучване, оценяващо въздействието на 17 симптома върху клиничните резултати при пациенти с рак на главата и шията. Съвкупната тежест на симптомите е важен независим предиктор за намален прием, загуба на тегло и оцеляване (36). Важно е, че тези НИС могат да повлияят приема през устата по цялата траектория на заболяването, възникващи в резултат на симптомите и усложненията при напреднал рак, противораково лечение или дори медицински съпътстващи заболявания.
Психосоциални интервенции
Хранителни добавки и диетични консултации
Мултимодален подход, подчертаващ необходимостта от повишен прием на калории и протеини, се подкрепя от проучвания, които включват ONS като компонент на интервенцията и проучвания, съобщаващи, че по-голямата част от пациентите с напреднал рак и загуба на тегло консумират диети, недостатъчни за поддържане на тегло дори при здрави физически лица. Систематичен преглед установява, че възрастните пациенти могат да бъдат особено податливи, като до 90% изпитват загуба на тегло по време на химиотерапия. Диетичното консултиране, което включва увеличаване на енергийно гъстите храни, честотата на хранене и използването на орални течни хранителни добавки, може да подобри енергийния прием и телесното тегло. Въпреки това, има малко публикувани проучвания и систематичен преглед заключава, че няма достатъчно доказателства за полза при пациенти, за които е установено, че имат ракова кахексия (42-44). Въпреки това, систематичен преглед (45) и мета-анализ (46) на хранителни интервенции при онкологично болни установиха, че консултирането с/без ONS е свързано с подобрения в теглото, ИТМ, енергийния прием и PG-SGA резултат.
Упражнение
Упражнението има потенциал да подобри мускулната маса и сила, физическата функция (47), умората и QoL при пациенти с ракова кахексия. Упражнението може да окаже своите ефекти чрез модулация на мускулния метаболизъм, инсулинова чувствителност, смекчаване на растежа на тумора и намаляване на нивата на възпаление (48). Въпреки силната обосновка за използването на тренировки за резистентност и аеробни упражнения (49), систематичен преглед установи недостатъчни доказателства за определяне на безопасността и ефективността при пациенти с ракова кахексия (50). Упражнението се комбинира успешно с други модалности в малки опити. Упражненията за резистентност в комбинация с тестостерон имат по-голямо анаболно действие от самостоятелната интервенция при свързана с възрастта кахексия и демонстрират подобни ползи при ХИВ и ХОББ (51). При свързано с ХИВ загуба, комбинацията от тренировки за устойчивост и тестостерон при мъже с евгонадално увеличава мускулната маса (52). Упражненията обещават да бъдат важен компонент на мултимодалната терапия чрез модулиране на експресията на цитокини и може би действайки заедно с анаболни хормони за подобряване на силата, функцията и QoL (53).
Текущи мултимодални изследвания
Описаната по-горе рамка за мултимодална интервенция е включена в дизайна на две рандомизирани проучвания. Мултимодално проучване на фаза II на упражнения, хранене и противовъзпалително лечение на кахексия демонстрира осъществимост и безопасност при пациенти, получаващи химиотерапия за нелечим рак на белия дроб или панкреаса. Проследяващата фаза III на MENAC интервенция е мултимодално проучване на много места, включващо ибупрофен (1200 mg/ден), омега-3 мастни киселини (2 g EPA и 1 g DHA), ONS, допринасящ за 542 kcal и 30 g протеин, и програма за домашни упражнения, състояща се от тренировки за съпротива три пъти седмично в допълнение към аеробни тренировки 2 пъти седмично. Тъй като пациентите в ранната фаза на кахексия са по-склонни да реагират на терапията, интервенциите ще започват заедно с химиотерапията и съпътстващото лечение на симптомите (54).
Заключения
Благодарности
Бележка под линия
Конфликт на интереси: Авторът няма конфликт на интереси, който да декларира.
- Опит в клиничното използване на нормобакт l синбиотик в комбинирана терапия на остри чревни заболявания
- Ендоскопска бариатрична терапия (EBT) Мичиганска медицина
- Дебел; s Функция като протекторна изолация срещу емоционален дистрес - блог за терапия
- Специалист по програма за загуба на мазнини - Сан Хосе, Калифорния Excel Medicine Вътрешни болести
- Дебел; Отслабване; Терапия с червена светлина Какво трябва да знаете Уелнес център Greenspan