Алма Фулурия
1 Cytos Biotechnology AG, Schlieren, Швейцария,
Томас А. Луц
2 Институт по ветеринарна физиология и Център по интегративна физиология на човека, Факултет Vetsuisse, Университет в Цюрих, Цюрих, Швейцария,
Катя Сладко
1 Cytos Biotechnology AG, Schlieren, Швейцария,
Мелания Осто
2 Институт по ветеринарна физиология и Център по интегративна физиология на човека, Факултет Vetsuisse, Университет в Цюрих, Цюрих, Швейцария,
Питър Й. Вилинга
2 Институт по ветеринарна физиология и Център по интегративна физиология на човека, Факултет Vetsuisse, Университет в Цюрих, Цюрих, Швейцария,
Мартин Ф. Бахман
1 Cytos Biotechnology AG, Schlieren, Швейцария,
Филип Саудан
1 Cytos Biotechnology AG, Schlieren, Швейцария,
Замислени и проектирани експерименти: AF TAL MO PYW MFB PS. Изпълнява експериментите: AF KS MO. Анализирани данни: AF TAL KS MO PYW MFB PS. Написа хартията: AF TAL PYW MFB PS.
Свързани данни
Резюме
Заден план
Според СЗО над 1 милиард души по света са с наднормено тегло и са изложени на риск от развитие на хронични заболявания, включително сърдечно-съдови заболявания, диабет тип 2, хипертония и инсулт. Настоящите терапии показват ограничена ефикасност и често са свързани с неприятни профили на странични ефекти, поради което има медицинска нужда от нови терапевтични интервенции в областта на затлъстяването. Наскоро се предполага, че стомашният инхибиторен пептид (GIP, известен също като глюкозозависим инсулинотропен полипептид) свързва прекомерното хранене със затлъстяването. Всъщност мишките с дефицит на GIP рецептор (GIPR -/-) бяха напълно защитени от затлъстяване, предизвикано от диета. По този начин нарушаването на GIP сигнализирането представлява обещаваща нова терапевтична стратегия за лечение на затлъстяване.
Методология/Основни констатации
За да блокираме GIP сигнализирането, избрахме активен подход на ваксинация, използвайки GIP пептиди, ковалентно прикрепени към вирусоподобни частици (VLP-GIP). Ваксинирането на мишки с VLP-GIP индуцира високи титри на специфични антитела и ефективно намалява наддаването на телесно тегло при животни, хранени с диета с високо съдържание на мазнини. Намаляването на наддаването на телесно тегло може да се дължи на намаленото натрупване на мазнини. Освен това се наблюдава повишена загуба на тегло при затлъстели мишки, ваксинирани с VLP-GIP. Важно е, че въпреки инкретиновото действие на GIP, третирани с VLP-GIP мишки не показват признаци на непоносимост към глюкоза.
Заключения/Значение
Това проучване показва, че ваксинацията срещу GIP е била безопасна и ефективна. По този начин активната ваксинация може да представлява ново, дълготрайно лечение на затлъстяването. Въпреки това ще са необходими допълнителни предклинични проучвания за безопасност/токсикология, преди терапевтичната концепция да може да бъде адресирана при хората.
Въведение
Стомашен инхибиторен пептид, известен също като глюкозозависим инсулинотропен полипептид (GIP) е един от тези пептидни хормони. GIP е 42-аминокиселинен, стомашно-чревен полипептид, освободен от дуоденални и йеюнални К-клетки след поглъщане на хранителни вещества и е доказано, че улеснява изхвърлянето както на глюкоза, така и на мазнини [12]. GIP действа бързо върху β-клетките на панкреаса, за да стимулира отделянето на инсулин, като по този начин осигурява бързо усвояване на глюкозата в тъканта. В допълнение, GIP подпомага отлагането на мазнини и натрупването на триглицериди в адипоцитите. По-конкретно е показано, че GIP насърчава изчистването на триглицеридите от циркулацията [13], [14], процес, частично опосредстван от способността му да стимулира липопротеин липазната активност [15]. Освен това, GIP рецепторите се експресират върху адипоцитите [16] в съответствие с пряката роля на GIP върху тези клетки. Наскоро бе показано, че мишките с дефицит на GIP рецептор (GIPR -/-) са напълно защитени от индуцирано от диетата затлъстяване [17]. По същия начин, скорошни проучвания демонстрират, че лечението с антагонист на GIP-рецептора води до намалено наддаване на тегло при мишки, хранени с диета с високо съдържание на мазнини и загуба на тегло при затлъстели мишки [18] - [20]. Следователно нарушаването на GIP сигнализирането представлява обещаваща, нова терапевтична стратегия за лечение на затлъстяване.
Индукцията на специфични за GIP, неутрализиращи антитела чрез ваксинация е особено привлекателна възможност, като се има предвид, че блокадата на GIP би била дълготрайна. По-рано показахме, че антигените, показани на силно повтарящи се вирусни повърхности, могат да нарушат толерантността на В-клетките [21] и епитопите, показани на повърхността на вирусоподобни частици (VLP), са в състояние ефективно да индуцират самоспецифични отговори на антитела при мишки и хора [22]. ] - [26]. В това проучване ние показваме, че ваксинацията срещу GIP предотвратява прекомерното наддаване на телесно тегло при гризачи, хранени с високомаслена диета и предизвиква повишена загуба на тегло при затлъстели мишки. Следователно активната ваксинация може да представлява привлекателна и удобна нова терапия за лечение на затлъстяване.
Резултати
Ваксинацията срещу GIP води до високи нива на GIP-специфични антитела
Ваксинацията срещу GIP предпазва от затлъстяване, предизвикано от диета
(А) Наддаване на телесно тегло при имунизирани мишки. Женските мишки се имунизират (дни 0, 14, 28, 42 и 133) със 100 ug Qβ-GIP или Qβ VLP и се поставят на диета с високо съдържание на мазнини (35% мазнини w/v). Показано е средното телесно тегло +/− SEM (n = 6). Повишаването на телесното тегло беше значително намалено при Qβ-GIP- в сравнение с Qβ VLP имунизирани животни от ден 70 нататък (двупосочен ANOVA F (1,80) = 18,55, p Фигура 3A-B е показана. (D) Повишаване на телесното тегло при имунизирани мишки на стандартна диета за гризачи. Женските мишки бяха имунизирани (дни 0, 14, 28, 42 и 112) с Qβ-GIP или Qβ VLP и хранени със стандартна диета (4% мазнини w/v) по време на целия експеримент. Показани са средни телесни тегла +/− SEM (n = 5) Не се наблюдава значителна разлика между двете експериментални групи, както е определено (двупосочен ANOVA F (1/88) = 0,81, p = 0,6751).
Ваксинацията срещу GIP увеличава енергийните разходи
За по-нататъшно изясняване защо животните, ваксинирани срещу GIP, са натрупали по-малко телесно тегло, приемът на храна, физическата активност и енергийните разходи са измерени след 4 месеца на диета с високо съдържание на мазнини. Qβ-GIP-ваксинираните мишки показват значително по-високи енергийни разходи в сравнение с контролните мишки както в тъмната, така и в светлата фаза (Фигура 3А). Това може да се обясни най-добре с увеличаване на основния метаболизъм, тъй като скоростта на метаболизма в покой е значително по-висока при Qβ-GIP ваксинирани животни (Фигура 3B) и не се наблюдава значително увеличение на физическата активност (Фигура 3C). Освен това, Qβ-GIP-ваксинираните животни показват по-нисък коефициент на дишане (RQ) през целия експериментален период, което показва преференциално изгаряне на мазнини в третираната група. Наблюдаваната разлика в RQ обаче не достига статистическа значимост (Фигура 3D). Не се наблюдават разлики в приема на храна между експерименталните групи, определени през три последователни дни след експеримента с енергийни разходи (Фигура 3Е). Взети заедно, тези данни показват, че намаленото наддаване на телесно тегло при мишки, ваксинирани с Qβ-GIP, хранени с диета с високо съдържание на мазнини, се дължи по-скоро на по-високи енергийни разходи, отколкото на по-нисък енергиен прием или повишена активност.
Непряка калориметрия при имунизирани мишки. Женските мишки бяха имунизирани (дни 0, 14, 28, 42 и 125) с Qβ-GIP (n = 8) или Qβ VLP (n = 10) и поставени на диета с високо съдържание на мазнини. Индиректната калориметрия е извършена на половината от групата на 128-ия ден и на другата половина на 139.-ия ден са показани комбинирани данни от тези измервания. (A) Консумация на кислород (VO2). В левия панел е показана средната консумация на кислород +/− SEM. Qβ-GIP-ваксинираните животни показват статистически значимо повишено VO2 (р 0,05). Всички статистически анализи бяха извършени чрез двустранни t-тестове.
Глюкозната хомеостаза не се влияе след ваксинация срещу GIP
Ваксинацията срещу GIP не пречи на липидния метаболизъм
За да се изяснят ефектите от ваксинацията срещу GIP върху липидния метаболизъм, се определят серумните липидни профили при ваксинирани животни, хранени с високомаслена диета 4 месеца след първата инжекция. Не се наблюдават значителни разлики в общия холестерол, HDL, LDL или vLDL при Qβ-GIP имунизирани мишки в сравнение с контролните мишки (Фигура 5А). По същия начин профилите на триглицеридите и свободните мастни киселини се наблюдават на редовни интервали при ваксинирани и контролни животни, поставени на диета с високо съдържание на мазнини. Както е показано на Фигура 5В, не се наблюдава значителна разлика между двете експериментални групи. Тъй като е известно, че GIP подпомага изчистването на триглицеридите от кръвообращението [13], [14], ние изследвахме дали постпрандиалният липиден клирънс е бил повлиян при ваксинирани животни. Тестове за орален липиден толеранс (OLTT) се провеждат при ваксинирани мишки, хранени с високомаслена диета на 36, 93 и 163. ден. Зехтинът се прилага чрез орален сонда и концентрацията на TGL в кръвта се определя в посочените часови точки. Липидите се елиминират с подобна кинетика и в двете експериментални групи, което показва, че елиминирането на TGL не е нарушено при ваксиниране срещу GIP (Фигура 5С)
(A – C) Женските мишки бяха имунизирани (дни 0, 14, 28, 42) с Qβ-GIP или Qβ VLP и поставени на диета с високо съдържание на мазнини. (А) Серумен липиден профил при мишки на ден 122. Измерван е общ, vLDL, LDL и HDL холестерол. Показани са средни стойности ± SEM (n = 10). Не са наблюдавани значими разлики между групите (p> 0,05). (B) Серумни TGL и FFA профили при мишки. Показан е процентът на контролните животни, имунизирани с Qβ VLPs ± SEM (n = 5) в посочения момент от време за триглицериди и свободни мастни киселини. Не са наблюдавани значителни разлики в нивата на TGL или FFA между групите (p> 0,05). (C) Липиден клирънс след хранене при мишки. Женските мишки бяха имунизирани (дни 0, 14, 28, 41 и 126) с Qβ-GIP или Qβ VLP и поставени на диета с високо съдържание на мазнини. OLTT бяха извършени в посочените часови точки. В левия панел е показан OLTT, извършен на ден 36. AUC за всички изследвани времеви точки е показан вдясно. Средните нива на триглицеридите или AUC ± SEM (n = 5) са показани за всяка група. Не са наблюдавани значими разлики между групите (p> 0,05). Всички статистически анализи бяха извършени чрез двустранни t-тестове.
Дискусия
Макар да е полезно за намаляване на наддаването на телесно тегло, ваксинацията срещу GIP, самоантиген, може да породи опасения, свързани с индуцирането на автоимунни реакции. Рискът от нежелани авто-възпалителни реакции е сведен до минимум с нашата ваксина [33]. Първо, разтворимата молекула е насочена към минимизиране на зависимата от антитела цитотоксичност. Второ, Т-хелперните клетъчни епитопи се осигуряват от носителя и къс GIP целеви пептид силно намалява вероятността автоактивните Т-клетки да бъдат индуцирани от ваксината. Независимо от това, е извършена подробна хистопатология при ваксинирани животни и не са наблюдавани признаци на специфично възпаление на червата или увреждане, свързано с ваксината, в други висцерални органи.
Изследванията на липидния метаболизъм не показват промени в концентрациите на vLDL-, LDL- и HDL-холестерол в серума на Qβ-GIP-ваксинирани мишки. По същия начин нивата на триглицеридите и свободните мастни киселини, както и постпрандиалният липиден клирънс не се променят при ваксинирани животни. Взети заедно, това проучване показва, че активната имунизация срещу GIP води до силно намаляване на наддаването на телесно тегло при мишки с високо съдържание на мазнини и без влошаване на кръвната захар или липидната хомеостаза.
Освен това в предварителен експеримент, проведен при затлъстели мъжки мишки, се предполага, че активната ваксинация срещу GIP не само предотвратява прекомерното наддаване на тегло при животни, хранени с диета с високо съдържание на мазнини, но може също да увеличи загубата на тегло при затлъстели мишки (Фигура S3).
Материали и методи
Животни
8-седмични мишки C57BL/6 (~ 20 g) са закупени от Harlan Netherlands (Horst, Холандия). Животните бяха настанени в съоръжение без патогени и им беше позволено да се аклиматизират за 2 седмици преди имунизацията. Във всички експерименти мишките бяха поставени в клетки в групи с изключение на периода, през който се определяше енергийният разход и приема на храна. Терапевтичният експеримент, показан на фигура S3, е извършен с мъжки мишки, всички останали експерименти са проведени с женски мишки. Освен ако не е посочено друго, животните са били хранени с високо съдържание на мазнини (35% мазнини w/v (Diet 2127), Provimi Kliba, Швейцария), ad libitum, по време на експерименталния период и са имали свободен достъп до вода. Експериментите бяха в съответствие с насоките на Швейцарската федерална ветеринарна служба (BVET).
Производство на ваксини
Имунизация и in vitro анализи
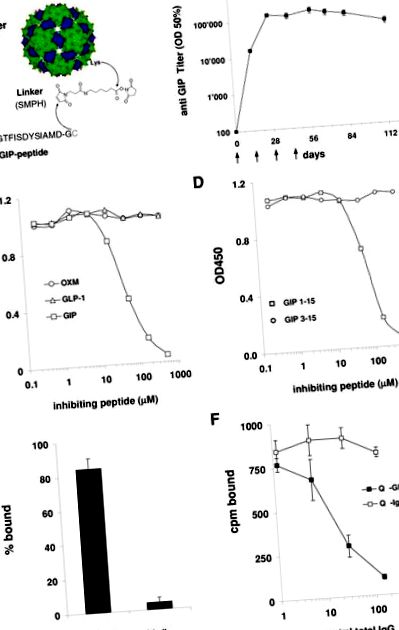
Животните се имунизират подкожно със 100 ug (мишки) или 300 ug (плъхове) Qβ-GIP или Qβ VLP, разредени в 200 ul PBS, в посочените часови точки. Титрите на GIP-специфичните антитела се определят чрез ELISA съгласно стандартни протоколи, използвайки свински GIP (Bachem # H-6220) при концентрация от 2.5 ug/ml за покритие. ELISA титърът се определя като реципрочните стойности на серумното разреждане, необходимо за достигане на половината от максималната оптична плътност при насищане. За съревнователни ELISA серумен пул от Qβ-GIP-имунизирани мишки се разрежда 1∶2500 и се инкубира с нарастващи концентрации на свински GIP (Bachem # H-6220), миши GLP-1 (Bachem # H6795) или миши оксинтомодулин (Bachem # H6058). След инкубация през нощта количеството на свободното антитяло се определя количествено в GIP-специфичен ELISA. За експерименти с in vivo свързване, Qβ-GIP-имунизирани и наивни мишки бяха предизвикани интравенозно с 1 ng I 125 -GIP (Bachem H-5016) и 30 минути след предизвикване на животните бяха умъртвени и серумът бе събран чрез сърдечна пункция. Общият IgG беше изтеглен от серумни проби с мъниста от протеин G (Amersham, # 17-0618-02). Измерва се свързана с протеин G мъниста и свободна радиоактивност и се изчислява процентният GIP, свързан с антитела.
Генериране на CHOK1 клетки, свръхекспресиращи GIP рецептора и проучвания за свързване
Анализ на телесното тегло и телесния състав
Животните се претеглят с помощта на високоточна скала. Съставът на тялото беше определен чрез двуенергийно рентгеново абсорбционно сканиране (Piximus Series Densitometer, GE Medical Systems, Madison, USA) в ICS (Illkirch, Франция).
Глюкозна и липидна хомеостаза
Общите нива на глюкоза в кръвта, холестерол, TGL, HDL, LDL, vLDL и FFA бяха измерени след 16 часа бързо. BGL се определят с помощта на глюкомер (Accu-Chek Aviva, Roche). Нивата на холестерола, TGL и FFA се определят чрез ензимни анализи на автоматизирана лабораторна работна станция Olympus AU400 в ICS (Illkirch, Франция). Липидните профили са определени от F.P.L.C. (Dionex). Нивата на HbA1c се определят от пълноценна кръв с помощта на мониторинговия комплект A1cNow (Metrika # 0520105). За OGTT, мишките бяха на гладно в продължение на 16 часа и след това 2 g/kg телесно тегло глюкоза във вода се прилага чрез орален сондаж. BGL бяха определени в посочените часови точки. За OLTT, мишките са гладували в продължение на 16 часа и след това са прилагани 8,35 µl/g зехтин чрез орален сондаж. Нивата на TGL са измерени от пълна кръв с помощта на CardioChek P.A. анализатор (PTS Inc.).
Експерименти с енергийни разходи
Енергийните разходи, активността и дихателният коефициент (RQ) бяха измерени за 24 часа (тъмна и светла фаза) чрез използване на две системи с калориметрия с отворен кръг (система Integra, AccuScan Instruments Inc., Columbus OH). Мишките бяха оставени да се адаптират към метаболитните клетки в продължение на 5 дни. За измерване на консумацията на кислород (VO2) и производството на въглероден диоксид (VCO2), мишките бяха поставени в херметически затворени дихателни клетки, които бяха непрекъснато проветрявани със скорост на потока около 1 l/min. За всяка клетка се взема проба от въздух за 20 секунди на интервали от 2 минути. RQ се дефинира като VCO2 (L)/VO2 (L). RMR се изчислява, като се взема средното от 3-те най-ниски показания на VO2 във всяка експериментална група по време на светлинната фаза. Физическата активност се определя чрез измерване на прекъсвания на лъча за период от 24 часа. Физическата активност се наблюдава чрез 3 масива от 16 инфрачервени сензора за светлинен лъч и след това се преобразува в изминато разстояние в cm. Данните бяха анализирани със софтуера AccuScan Integra ME.
Хистопатология
Пробите от тъкани се фиксират в 4% параформалдехид, разделят се и се оцветяват с H&E по стандартни методи. Хистологичната оценка е направена от квалифициран ветеринарен патолог.
Статистически анализ
За анализ на телесното тегло са използвани данни за двупосочна ANOVA в кръвната глюкоза и фруктозамин. Всички останали статистически анализи са направени с помощта на двустранен студентски t-тест. Площите под кривата за OGTT бяха определени с помощта на софтуера Prism Graphpad.
подкрепяща информация
Фигура S1
Няма кръстосана реакция на Qβ-GIP индуцирани антитела с GLP1 и OXM in vivo. Qβ-GIP имунизирани мишки. мишки бяха предизвикани i.v. с 1 ng I125-GIP, I125OXM или I125 GLP1. Като контролни наивни мишки бяха предизвикани с 1 ng I125-GIP. 30 минути по-късно се определя количеството на GIP, OXM или GLP1, свързано с антитела. Показан е процентът на GIP, OXM или GLP-1 ± SEM, свързан с антитела (n = 4). Докато по-голямата част от инжектирания GIP е установено, че е свързан с антитела, са установени само фонови нива на OXM или GLP1, свързани с фракцията на антителата при Qβ-GIP имунизирани мишки.
Фигура S2
Ваксинацията срещу GIP не предизвиква възпаление в GIT. Женски мишки C57BL/6 бяха имунизирани подкожно със 100 µg Qβ-GIP или Qβ VLP в дни 0, 14, 28 и 42. Животните бяха хранени с диета с високо съдържание на мазнини (35% мазнини w/v) от началото на експеримента . Мишките бяха умъртвени на ден 99. Пробите от тъкани бяха фиксирани, разделени и оцветени с H&E, съгласно стандартни методи. Показва се една представителна мишка от всяка група. Хистологичният анализ на пробата от патолог не разкрива никакви признаци на възпаление в червата при Qβ-GIP имунизирани животни в сравнение с Qβ третирани контролни животни. Подобни резултати се получават, когато животните се избиват на 36 или 142 ден и се анализират от патолог.
Фигура S3
Ваксинацията срещу GIP води до загуба на тегло при затлъстели мъжки мишки. Мъжките мишки са били хранени с високо съдържание на мазнини в продължение на 4 месеца. По това време всички животни са били силно затлъстели и са достигнали тегло между 45-50 g. След това животните бяха имунизирани (дни 0, 14, 36, 50 и 119) с Qβ-GIP или Qβ VLP и държани на диета с високо съдържание на мазнини (35% мазнини w/v). Съдържанието на мазнини в диетата е намалено до 20% мазнини (w/v) от 42-ия ден нататък. Показани са средни промени в телесното тегло ± SEM (n = 10). Qβ-GIP третираните животни са загубили значително повече тегло от Qβ VLP имунизираните животни от 70-ия ден нататък (двупосочен ANOVA F (1,162) = 9,82, p = 0,0057).
Благодарности
Благодарим на д-р Паула Грест (Институт по ветеринарна патология, Университет в Цюрих) за хистопатологичната оценка на тъканни проби и образи и на д-р Йенс Холст за предоставената 3T3 клетъчна линия, експресираща човешкия GIP рецептор, и на д-р Лидия Иванова за помощта при клонирането на GIP рецептора.
Бележки под линия
Конкуриращи се интереси: А. Фулурия, К. Сладко, П. Саудан и М.Ф. Бахман са служители на Cytos Biotechnology AG и притежават акции или опции за акции в компанията.
Финансиране: По-голямата част от работата е извършена и финансирана от Cytos Biotechnology AG.
- Насочване към родители за лечение на детско затлъстяване при момчета с мускулна дистрофия на Дюшен А
- Все още има само едно ефективно лечение на затлъстяването и то е животоспасяващо
- Text2bHealthy Използване на иновативни методи за лечение на детско затлъстяване - Изглед в пълен текст
- Съдово насочен нанотерапевтичен подход за лечение на затлъстяване IJN
- Центрове за лечение на затлъстяване във Вирджиния - центрове за лечение на затлъстяване и рехабилитация Вирджиния - затлъстяване