От отдел по сърдечно-съдови заболявания, Медицински факултет (T.I., Y.S., R.K., T.K., N.S., D.X., N.M., K.A.) и Катедра по медицински науки (YK), Университет на Цукуба, Цукуба, Япония.
От отдел по сърдечно-съдови заболявания, Медицински факултет (T.I., Y.S., R.K., T.K., N.S., D.X., N.M., K.A.) и Катедра по медицински науки (YK), Университет на Цукуба, Цукуба, Япония.
От отдел по сърдечно-съдови заболявания, Медицински факултет (T.I., Y.S., R.K., T.K., N.S., D.X., N.M., K.A.) и Катедра по медицински науки (YK), Университет на Цукуба, Цукуба, Япония.
От отдел по сърдечно-съдови заболявания, Медицински факултет (T.I., Y.S., R.K., T.K., N.S., D.X., N.M., K.A.) и Катедра по медицински науки (YK), Университет на Цукуба, Цукуба, Япония.
От отдел по сърдечно-съдови заболявания, Медицински факултет (T.I., Y.S., R.K., T.K., N.S., D.X., N.M., K.A.) и Катедра по медицински науки (YK), Университет на Цукуба, Цукуба, Япония.
От отдел по сърдечно-съдови заболявания, Медицински факултет (T.I., Y.S., R.K., T.K., N.S., D.X., N.M., K.A.) и Катедра по медицински науки (YK), Университет на Цукуба, Цукуба, Япония.
От отдел по сърдечно-съдови заболявания, Медицински факултет (T.I., Y.S., R.K., T.K., N.S., D.X., N.M., K.A.) и Катедра по медицински науки (YK), Университет на Цукуба, Цукуба, Япония.
От отдел по сърдечно-съдови заболявания, Медицински факултет (T.I., Y.S., R.K., T.K., N.S., D.X., N.M., K.A.) и Катедра по медицински науки (YK), Университет на Цукуба, Цукуба, Япония.
От отдел по сърдечно-съдови заболявания, Медицински факултет (T.I., Y.S., R.K., T.K., N.S., D.X., N.M., K.A.) и Катедра по медицински науки (YK), Университет на Цукуба, Цукуба, Япония.
Преглеждате най-новата версия на тази статия. Предишни версии:
Резюме
Целта на това проучване е да се изследва следното в съответствие с неравномерната структура на стената на ЛН: (1) трансмурално разпределение на миоцитите и извънклетъчно ремоделиране в проучване с времеви ход, при което ремоделирането на миокарда е свързано с развитието на хипертонично сърце болест; (2) връзката между щама на миокарда и характеристиките на трансмуралната тъкан; и (3) влиянието на щама върху функцията на глобалната камера.
Методи
Експериментални животни
В това проучване бяха използвани 68 мъжки плъхове, чувствителни към сол на Dahl, добре валидиран модел на сърдечна недостатъчност със запазен EF, дължащ се на хипертония (DIS/Eis; Eisai, Токио, Япония). Контролната група (n = 35) е хранена с ниско съдържание на сол 0,3% NaCl, а групата с хипертония (НТ, n = 33) е хранена с високо съдържание на сол 8% NaCl чау от 6 седмици.
Допълнителни методи
Разширеният раздел "Методи" в онлайн добавката за данни съдържа информация за хемодинамичните измервания, ехокардиографски анализи, тъканни анализи, количествено определяне на генната експресия чрез полимеразна верижна реакция в реално време и статистически методи.
Резултати
Първоначалните измервания бяха получени от всички 68 плъхове. Един контролен плъх и 1 плъх в групата с НТ умряха спонтанно на 13 седмици и не завършиха експерименталния протокол. Причината за смъртта не е разследвана.
Кръвно налягане, сърдечна честота и тегло на органите
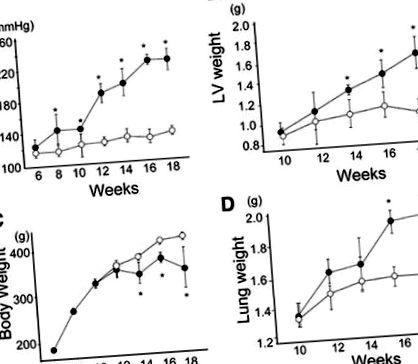
Диетата с високо съдържание на сол предизвиква значително и трайно повишаване на кръвното налягане в сравнение с това в контролната група във всеки момент от време след седмица 8 (Фигура 1). Сърдечната честота не показва значителна разлика между НТ групата и възрастово съвпадащата контролна група, с изключение на тази на 18 седмици (Таблица 1), по това време се наблюдава по-висока сърдечна честота в НТ групата, отколкото в контролната група. Теглото на ЛН също постепенно се повишава с повишаването на кръвното налягане, докато загубата на тегло настъпва от 14 седмици, последвано от повишаване на теглото на белите дробове, което предполага декомпенсирана сърдечна недостатъчност с белодробна конгестия.
маса 1. Пулс и стандартни ехокардиографски измервания
E/A показва съотношението на скоростта на предаване на ранен към късен диастоличен поток; E ′, септална скорост на митралния пръстен в началото на диастолата; EF, фракция на изтласкване; HR, сърдечен ритъм; HT, хипертония; LAD, ляво предсърдно измерение; LV, лява камера; LVWT, дебелина на стената на лявата камера; LVDd, крайно-диастоличен диаметър на лявата камера; RWT, относителна дебелина на стената; и W, седмици.
Фигура 1. Промяна в систолното кръвно налягане (A), тегло на лявата камера (LV) (Б.), телесно тегло (° С) и белодробно тегло (д) при плъхове в групите с хипертония (НТ, червени кръгове и контролни, сини кръгове). *P
Ехокардиографски изследвания
Измерванията на стандартните ехокардиографски параметри са показани в Таблица 1. HT групата показва прогресивно нарастване на дебелината на стената и масата на НН от 6 до 18 седмици (Таблица 1). Диаметърът на лявото предсърдие се увеличава и E/A и E 'намаляват с остаряването при плъховете от НТ групата. За сравнение, EF не показва промяна с времето до 16 седмици и лек, но значителен спад на EF се наблюдава на 18 седмици при плъховете от групата HT.
Функция на систолната и диастолната камера
В сравнение с контролната група, НТ групата не показва разлика в ESPVR през целия период на изследване (Фигура 2). Установено е, че τ е значително по-голяма от 10 седмици до 18 седмици в групата с НТ и че сковаността на камерата е повишена на 18 седмици.
Фигура 2. Функция на камерата на лявата камера (LV) при плъхове с хипертония (HT). Горна част показва представителни вълнови форми на налягане и обем по време на манипулации (компресия на долната куха вена) за намаляване на предварителното натоварване, извършено на 10, 14 и 18 седмици. Emax не се различава значително по време на експериментите (долу, вляво), докато константата за време на релаксация τ се удължава от ранния период (долу вдясно), а твърдостта на камерата се повиши значително на 18 седмици (отдолу, средата). EDPVR показва връзката крайно диастолично налягане-обем; и ESPVR, съотношение крайно систолично налягане-обем. *P
Трансмурален стрес и разпределение на ъгъла на влакното
Напреженията на систоличната стена са по-големи в субендокардиалния слой, отколкото в субепикардиалния слой и в двете групи, и по-високи напрежения на субендокардиална стена са наблюдавани в НТ групата, отколкото в съответния слой в контролната група (Фигура S2 в онлайн само Допълнение за данни). Трансмуралното разпределение на ориентацията на миокардното влакно е било идентично във 2-те групи през всички периоди на изследване и е било на 69 ± 19 ° от хоризонталната равнина в субендокарда. Стресът на систоличната стена се увеличава последователно, тъй като животните с НТ порастват, без да се засягат ъглите на миокардните влакна.
Измервания на щама на миокарда
Ехокардиографията за проследяване на петна беше приложена успешно към надлъжните и късите оси (Фигура 3А). Въпреки че параметрите на 3 щама не се променят с времето в контролната група, глобалният щам в надлъжна посока (GLS) в групата НТ показва значително увреждане от седмица 10 и прогресивно се влошава с възрастта (Фигура 3В, отгоре и 3С). Глобалното напрежение в радиалната посока (GRS) намалява от 16-та седмица (Фигура 3B, средна и 3D), а глобалното напрежение в периферната посока (GCS) намалява на 18 седмици в групата HT (Фигура 3B, отдолу и 3E).
Фигура 3. Миокарден щам при плъхове с хипертония (HT). Ехокардиография за проследяване на петна е приложена към надлъжната (Горна част) и къса ос (отдолу) парастернални възгледи (A) и след това бяха получени измервания на деформация (Б.), при които всеки цвят представлява 6 сегмента на лявата камера, а черната линия показва средното напрежение. Глобалният надлъжен щам (GLS) значително намаля от 10 на 18 седмици (B, отгоре; ° С), като има предвид, че глобалната радиална деформация (GRS; B, средна; д) и глобално периферно напрежение (GCS; (B, отдолу; Е.) са запазени до късната фаза на експерименталния курс. *P
Трансмурално разпределение на фиброза и хипертрофия в патологични проби
На 14-та седмица общата тежест на процентната фиброза на площта беше значително по-голяма в групата с НТ, отколкото в контролната група (4,9 ± 1,4% срещу 2,2 ± 0,4%; P
Фигура 4. Разпределение на трансмуралната фиброза при плъхове с хипертония (НТ). Областите на фиброза (оцветени в синьо) преобладават в субендокардиалния слой на 14 седмици и се разпространяват в средния слой до 18 седмици в групата с НТ (A). Процентът фиброза на площ (Б.) е значително по-голям в субендокардиалния слой на 14 седмици и субендокарда до средния миокард на 18 седмици в групата с НТ. Съотношение на колаген I/III (° С) се е увеличил значително в субендокардиалния слой на 18 седмици в групата с НТ. *P
Фигура 5. Трансмурална ширина на миоцитите и фетална изоформа на контрактилен протеин при плъхове с хипертония (НТ). Широчината на миоцитите (A) е значително по-голям в субендокардиалния слой на 14 седмици и субендокарда до средния миокард до 18 седмици. β-миозин тежка верига (MHC) пратеник РНК (Б.) значително се увеличава в субендокардиалната и средната стена на 14 и 18 седмици в сравнение с контролната група. β-MHC/α-MHC (° С) също се увеличава значително в субендокардиалния до средния слой на 14 и 18 седмици в групата с НТ. *P
Специфична за слоя промяна във фиброзата и хипертрофията чрез анализ на верижната реакция на полимеразната реакция в реално време
Миокардната експресия на колаген тип I/III се увеличава на 18 седмици с преобладаване в субендокардиалната област (Фигура 4С, отдолу). Миокардната β-миозинова тежка верига (MHC; Фигура 5В) и β-MHC/α-MHC изоформите (Фигура 5С) са значително увеличени в субендокардиалния и средния стенен слой на 14 и 18 седмици в групата НТ.
Връзка между щам и патологични находки
Надлъжният щам корелира значително със субендокардиална (Фигура 6А) и фиброза на средната прослойна площ (R= 0,59, P= 0,004 и R= 0,51, P= 0,0018, съответно) и широчината на миоцитите на всички слоеве (R= 0,61, P= 0,001). Съществува значителна отрицателна връзка между напрежението на стената и деформациите (Фигура 6B), както се очакваше от резултатите от първоначалните проучвания на връзката стрес-деформация. Следователно беше извършено регулиране чрез съответното напрежение на стената, специфично за слоя (Таблица 2). След като коригирахме стреса, субендокардиалната процентна площ фиброза, но не и субендокардиалната ширина на миоцитите, беше избрана като независим детерминант на GLS. Установено е, че фиброзата на средната стена и епикардния слой и ширината на миокардната клетка са значимите детерминанти на GRS и общата и субендокардиална хипертрофия на миокарда, но не и степента на отлагане на колаген, значително свързана с GCS.
Таблица 2. Корелация между деформация и трансмурални патологични находки след корекция за съответния стрес на стената на слоя *
Фигура 6. Връзки на глобалното надлъжно напрежение (GLS) с ендокардиалната процентна фиброза, стрес на ендокардната стена и скованост на камерата. GLS показа значителни положителни връзки с фиброза на ендокарден процент (A), стрес на ендокардната стена (Б.) и твърдостта на камерата, получена от връзката крайно диастолично налягане-обем (° С).
Връзка между деформацията и функцията на камерата
Въпреки че GLS не показва връзка с Emax, съществува значителна връзка между GLS и твърдостта на камерата (Фигура 6C) и τ (R= 0,58, P 13,14 Извънклетъчната колагенова мрежа, която поддържа подравняването на миоцитите помежду си и осигурява предаването на сила, генерирана от контракция на миоцитите, към камерата на вентрикуларната камера, 13 става слята и удебелена във взаимосвързващия слой в хипертоничното сърце. 15 Фиброзата в настоящото изследване се натрупва предимно в субендокардиалния слой, където ъгълът на миокардното влакно е ориентиран надлъжно. В допълнение, максималното срязване настъпва в субендокарда, в сравнение с това в други слоеве, чрез плъзгане на миокардни пластини една спрямо друга. 16 Това предполага, че самата фиброза може пряко да инхибира пренареждането на миокардните листове във всеки слой и може да доведе до аномалия на деформация на систолната стена.
На молекулярно ниво колагенът I/III е повишен в субендокарда в НТ групата. Съобщава се също, че повишеното съотношение на колаген I/III води до скованост на камерата 17, което предполага установена фиброза. 13 В няколко клинични проучвания надлъжната систолна дисфункция е свързана с неблагоприятен клиничен резултат. 18–20 По този начин, резултатите от това проучване показват, че измерването на GLS позволява оценка на степента на фиброзни промени и използване на тази информация за прогностично стратифициране на риска при хипертонична сърдечна недостатъчност.
Миоцитен хипертрофичен градиент през вентрикуларната стена и щам
Систолична дисфункция на вентрикуларната стена и камарно диастолно увреждане
GLS не корелира със систоличната камера, но корелира значително с диастолната хемодинамика. Миокардната хипертрофия и повишената фиброза могат да играят важна роля за поддържане на скованост както на систоличната, така и на диастоличната камера при наличие на хронично претоварване под налягане. 23 По-специално, прекомерните количества миокарден твърд колаген са основният определящ фактор за скованост на пасивната камера в хипертоничното сърце. 24 С оглед на факта, че деформацията на камерата започва от надлъжната посока в ранния диастол, 5 е разумно да се предположи, че бавната скорост на релаксация е свързана с надлъжната дисфункция. В допълнение, увеличаването на бавната β-MHC изоформа в надлъжно ориентирани влакна в субендокардиалния слой може да причини забавяне на релаксацията на камерата.
Ограничения
В настоящото проучване трансмуралният стрес на стената е оценен въз основа на предварително съобщено изчисление; измерването на систоличния стрес на стената в епикардиалния слой беше фундаментално трудно, тъй като епикардният слой беше прикрепен към перикарда и гръдния кош.
Ние не изследвахме сегментни разлики в хипертрофията или фиброзата, както и не беше оценена специфичната за слоя миоцитна или микроваскуларна функция. Въпреки че бяха оценени много фактори, причинно-следствените връзки на факторите не бяха напълно демонстрирани. Патогенезата на повишената субендокардиална фиброза не е оценена; обаче, повишеният стрес на субендокардиалната стена, оксидативният стрес, 25 и системата ренин-алдостерон са обещаващи кандидати като причиняващи фактори на субендокардиалната фиброза. 26–28 И накрая, не се извършват интервенции за наблюдение на ефектите от терапията върху хипертрофия или фиброза на миоцитите. Всички тези въпроси са от значение и трябва да бъдат предмет на допълнителни проучвания.
Перспективи
Благодарности
Признаваме Еми Шиомицу, Катедра по медицински науки, Медицински факултет, Университет на Цукуба, за помощта при измерванията на патологичните проби.
Източници на финансиране
T. Ishizu и Y. Seo са финансирани от Японското общество за насърчаване на науката, безвъзмездна помощ за научни изследвания (24591035).
- Диетата с високо съдържание на мазнини влошава предсърдното и камерно ремоделиране на хипертонични сърдечни заболявания при стареене
- Видове хипертонични сърдечни заболявания, симптоми и диагностика
- Масивна лявокамерна аневризма CTSNet
- Изтръпване на лявата ръка Това е сърдечен удар или нещо друго 19 причини
- ЛЯВА ВЕНТРИКУЛЯРНА ХИПЕРТРОФИЯ И ГЕОМЕТРИЯ ПРИ ДЕЦА С ПЪТНО И НЕТОЛНО ПЪТЕ С АРТЕРИАЛ
- Оформяне на тялото, намаляване на мазнините, Бостън - HCG диета, Ultrashape, Velashape в кантон, Brookline, MA
- Защо „Ако отговаря на вашите макроси“ не работи OPEX Fitness
- Какво; s Сделката с млечни продукти и плодородие Блог за плодовитост - Др
- Хълм; s Diet Diet Kd Early Support Котешки пилета, зеленчуци; Преглед на котешка храна за оризова яхния
- Съдия осъжда родители след смъртта на бебето от веганска диета - VICE
- Успех за отслабване на знаменитости Как Перес Хилтън е загубил 70 лири форма
- Fat to Fit Отслабнах с 16 килограма за 2 месеца и половина
- Спортните напитки ви дебели ли са; PodiumRunner
- Цветята са отровни за децата Здравейте майчинство
- Жени; s Истории за успех с Total Gym Total Gym
- Кленово безумие на Наоми Кембъл Модели The Guardian
- Мастен черен дроб и слабо функционираща щитовидна жлеза; BOOST Щитовидна жлеза Хашимото; s и приложението Hypothyroid
- Най-добрите ястия преди и след тренировка Изкуството на мъжествеността
- Описване на диетичен прием Диетичен оценяващ материал
- 8 храни, които карат вашата пикня да мирише различно от аспержи